百奥赛图拥有丰富的临床前药代动力学(Pharmacokinetics,PK)检测和生物分析经验,可提供基于抗体药物的专业药代动力学分析服务。PK生物分析平台包括ELISA和ECL。
虽然与传统的化学药物有很大的不同,抗体的药代动力学研究仍然基于经典的药代动力学研究方法,但更多的是关注其靶向性以及受抗体特性影响的药代动力学特性。我们有两种实验类型:抗体血清/血浆浓度检测和抗药物抗体(ADA)筛选试验。







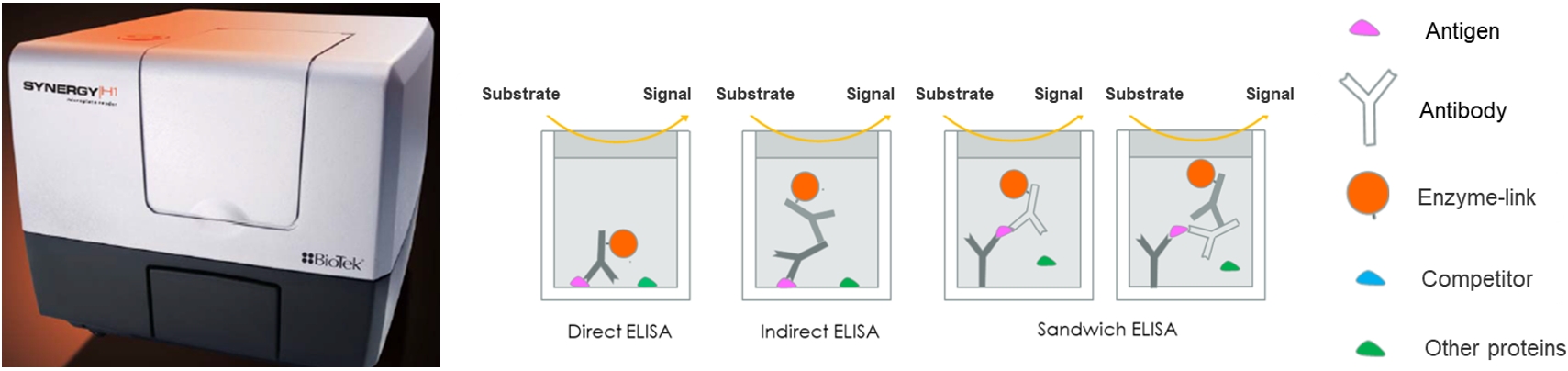
ELISA

Electrochemiluminescence (ECL)
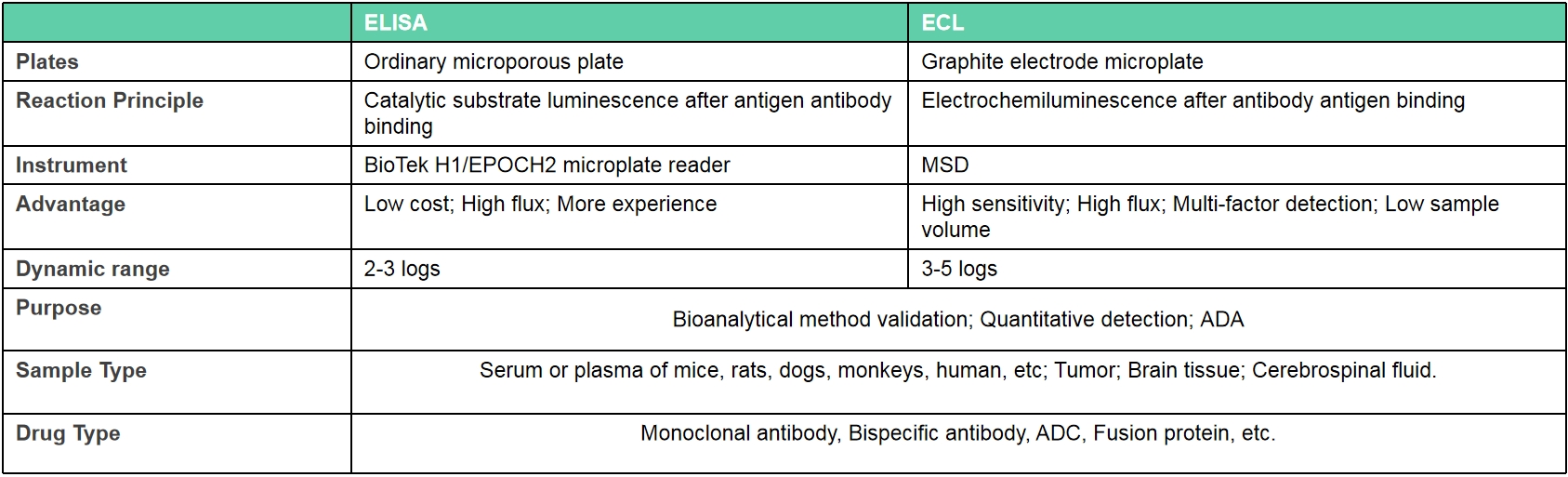
人源(化)单克隆抗体小鼠血药浓度分析
药物浓度检测是药代动力学研究的重要指标,开发可以准确稳定地检测血液样本中药物浓度的检测方法非常重要,目前应用最为广泛的抗体药物浓度检测方法是ELISA法,通过使用不同种类的ELISA方法可以对单抗,双抗浓度进行分析。
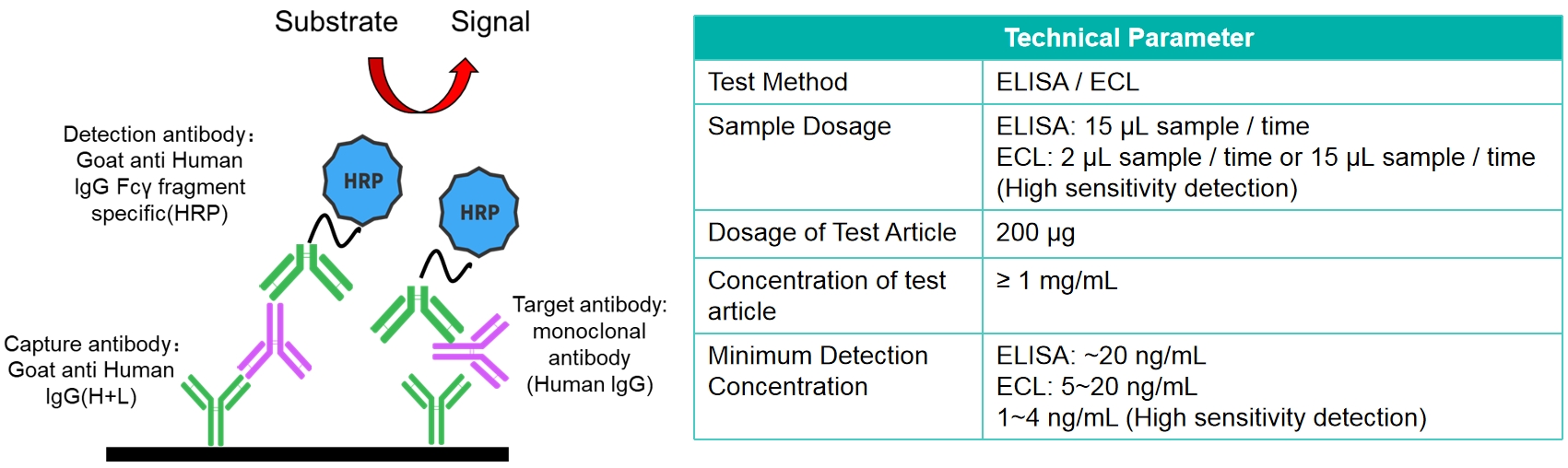
基于双抗体夹心法,使用抗人的抗体对血清中的人源化抗体进行捕获,再加入标记有HRP的可特异性结合人源化抗体的Fcγ fragment的抗体作为检测抗体,检测血清中药物浓度
特点:
基于双抗夹心法ELISA的药物浓度检测方法,可以检测IgG1,IgG2,IgG4亚型的单克隆抗体和具有完整抗体结构的融合蛋白和双特异性抗体。
有固定的实验条件,可以快速进行样本检测,可支持方法学验证。
主要检测血清中人源化抗体的总量,包括已经和可溶性靶点结合的抗体。
非特异性结合抗体药物,不能在联合给药情况下分析目标抗体浓度。
本方法仅限于检测非人动物样本中的药物浓度检测。
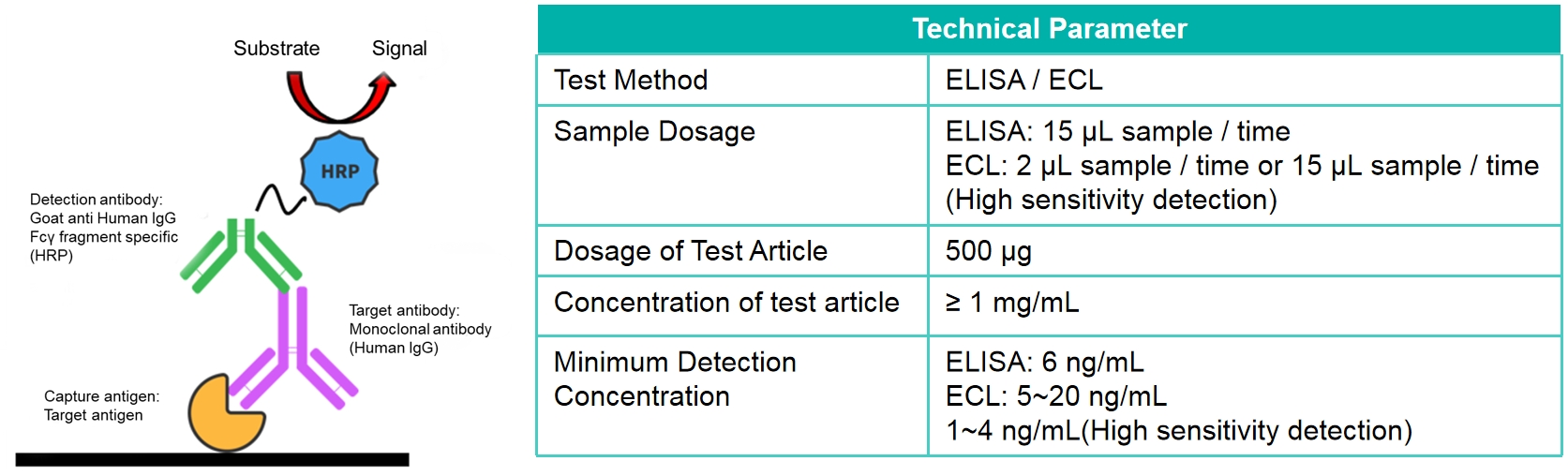
根据药物靶点开发方法,捕获试剂为人源化抗体的靶蛋白,可以特异性与抗体的CDR区结合。再加入标记有HRP的可特异性结合人源化抗体的Fcγ fragment的抗体作为检测抗体,检测血清中药物浓度
特点:
根据抗体靶点开发的特异性检测方法,针对受试品具有高度特异性,可以在联合用药情况下检测目标抗体。
一般根据需求开发方法或进行方法转移,可支持方法学验证。
严格意义上讲,此类方法主要检测血清中游离的人源化抗体量,无法检测已经与靶点结合的抗体。
人双特异性抗体小鼠血药浓度分析
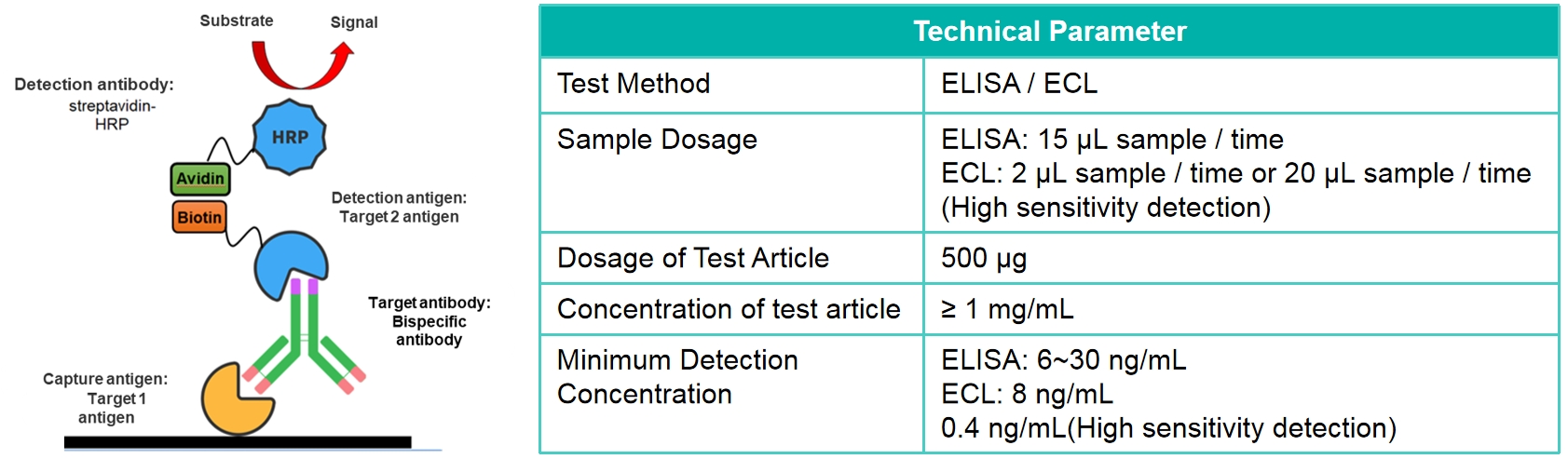
根据药物靶点开发方法,用于检测血清中具有完整结构的双特异性抗体,捕获试剂为人源化抗体的靶蛋白,可以特异性与抗体的CDR区结合,加入双特异性抗体另一特异性靶点蛋白(带有Biotin或His标记)完成整个检测体系的建立。加入Streptavidin-HRP或Anti-His Antibody-HRP产生检测信号
特点:
根据抗体靶点开发的特异性检测方法,针对受试品具有高度特异性,可以检测血清中具有完整结构的双抗,可以用于临床前申报方法。
ELISA-交替采血策略(抗体T1/2为5~10天)
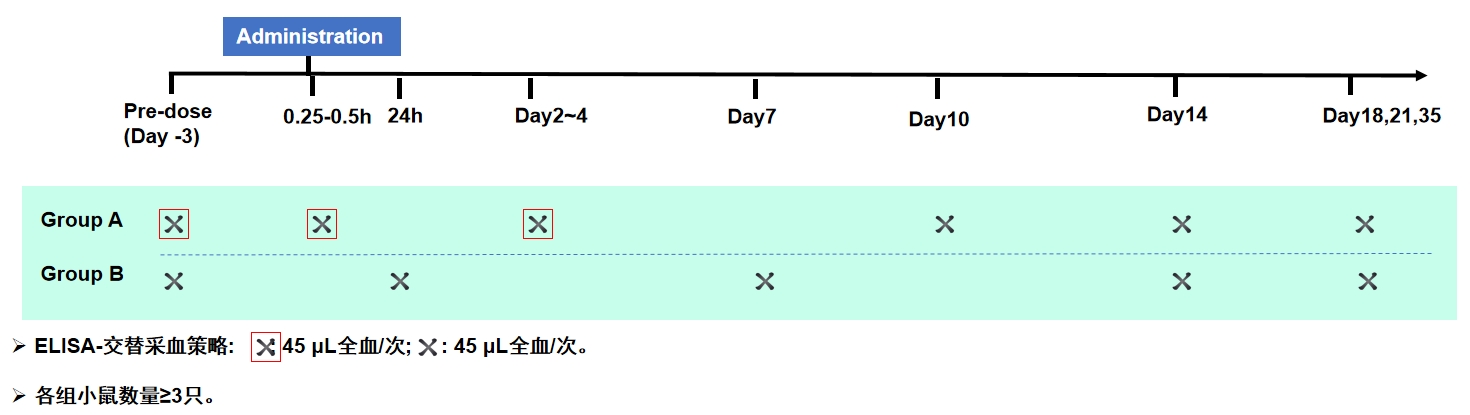
ECL微采样策略(抗体T1/2为5~10天)

数据分析
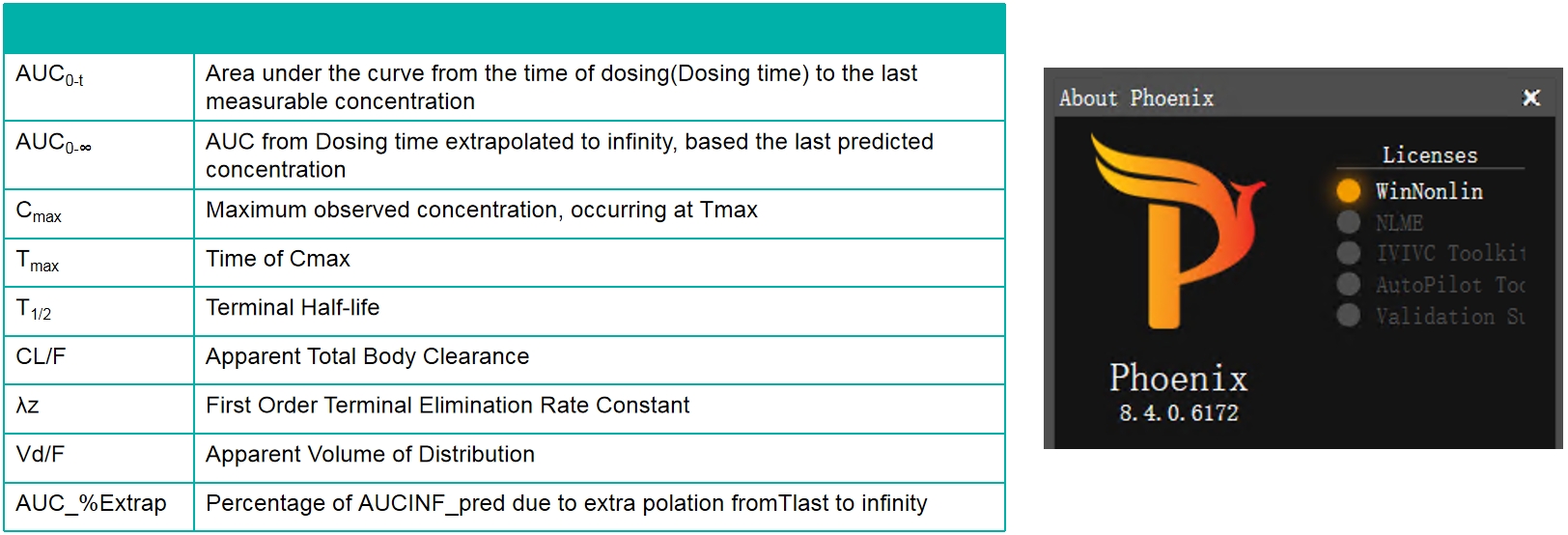
PK研究的研究设计
- 建议采用血清进行PK检测。
- 肝素钠有时会影响结果。血浆采集建议使用EDTA.2Na和EDTA.2K等抗凝血剂。
- 提出符合临床实际的给药方法。
- 建议静脉给药。
- 推荐9-10周龄小鼠。
抽样方法的比较
不同采样方法检测结果的比较
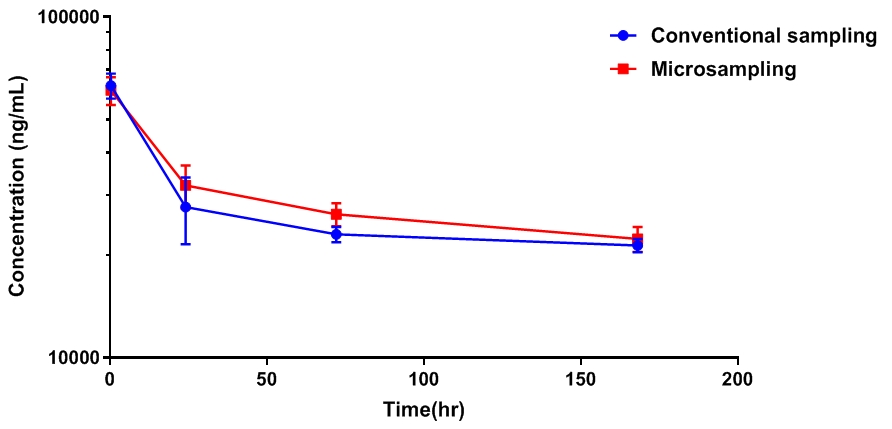
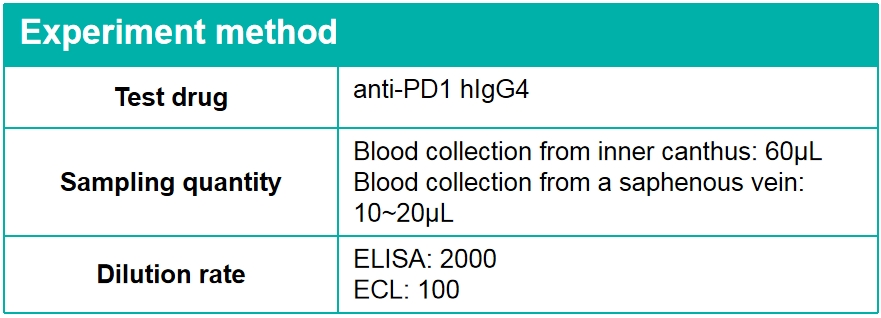
数据表明,两种采样方法的实验结果没有明显差异。
人、猴、B-hFcRn和WT小鼠抗体半衰期的相关性研究
表1.抗体在人、猴、B-hFcRn和野生型小鼠体内的半衰期(天)
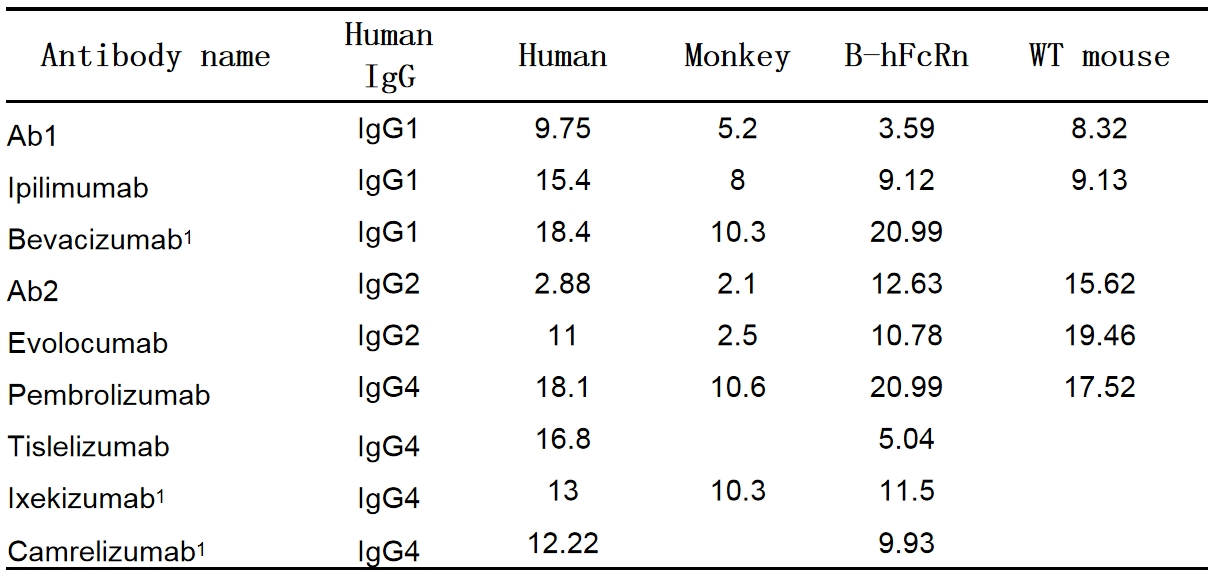
1贝伐单抗样本数量相对较少。
图1.人与猴(A)、B- hfcrn小鼠(B)的半衰期相关性(仅包括人IgG1单抗)
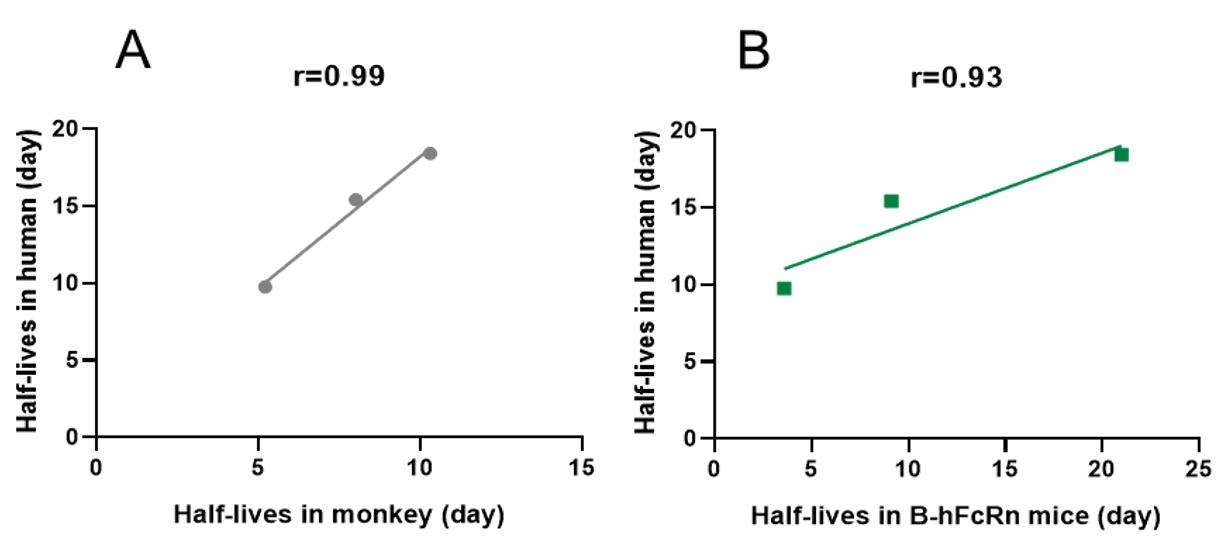
*更多的抗体正在接受测试。
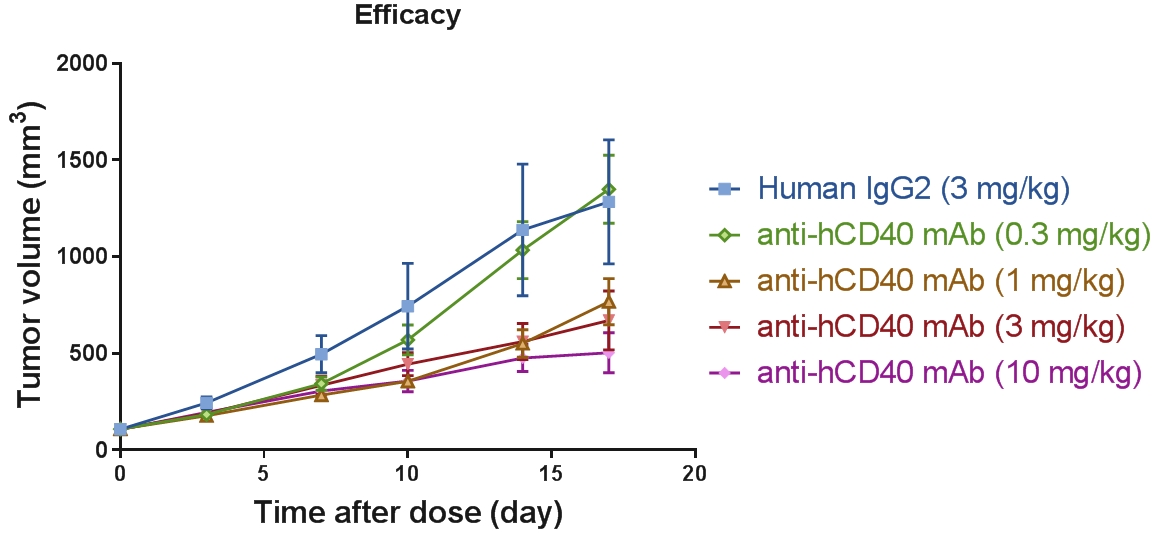
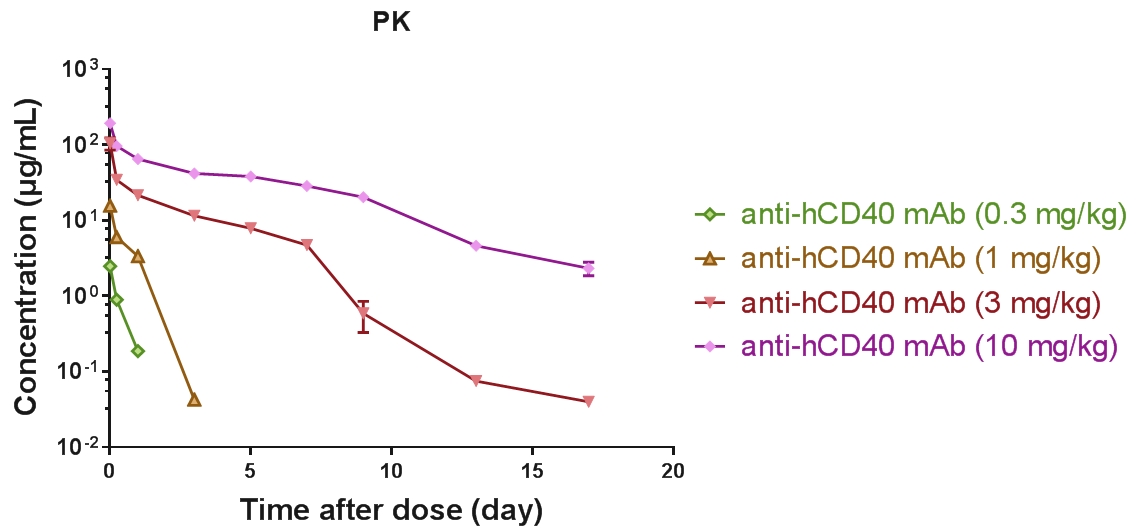
B-hCD40小鼠可用于抗人CD40抗体PK / PD /功效检测
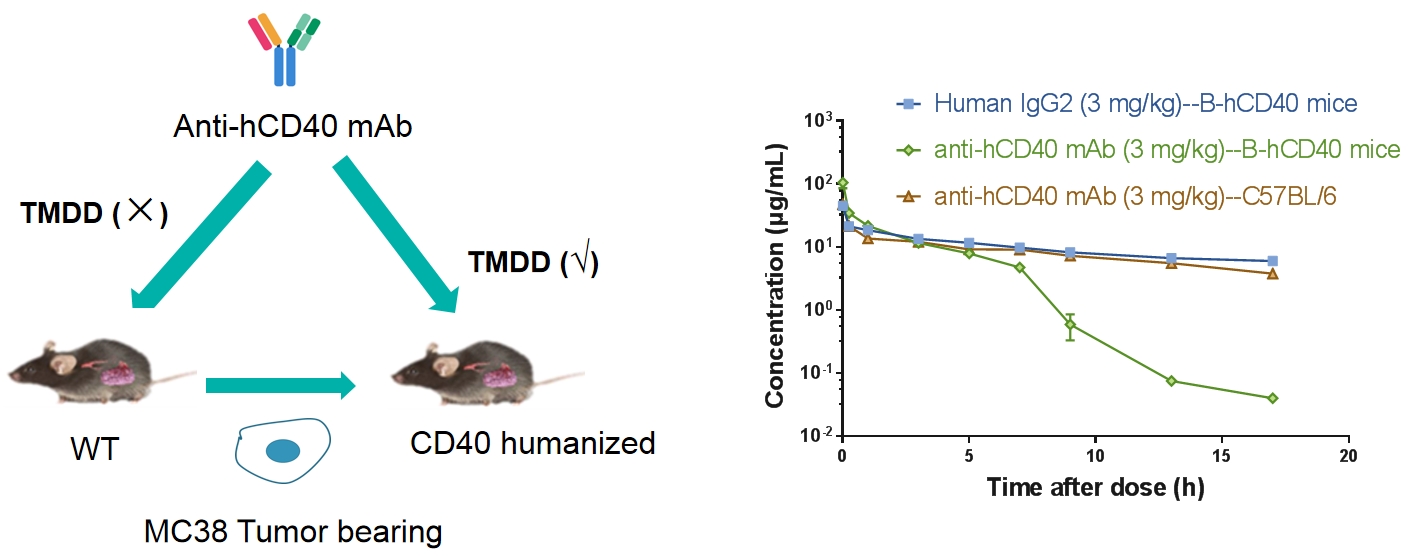
受体占用分析

体内药效学评价
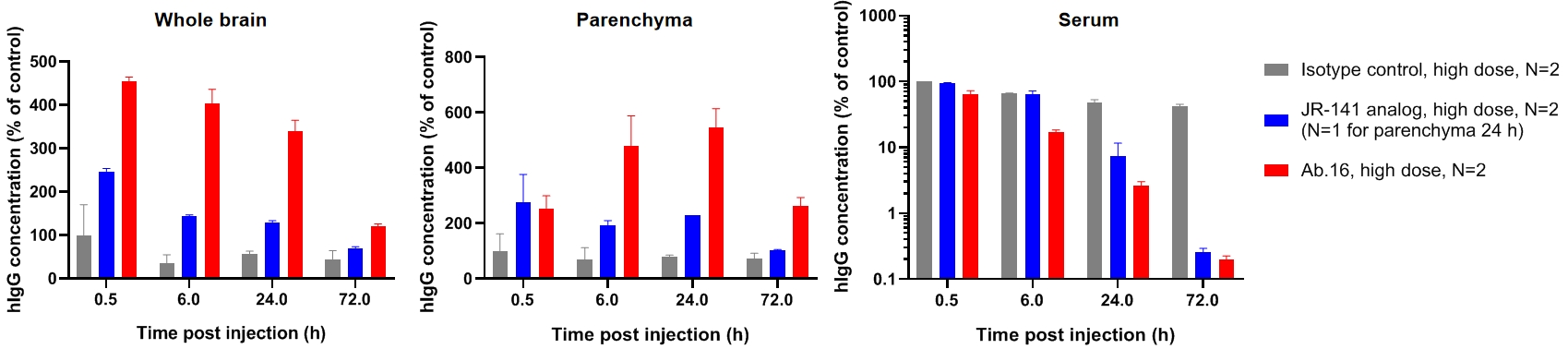
抗人TFR1 HCAb穿透血脑屏障

CD40-PD-1双特异性抗体
B-hPD1/hCD40 mice
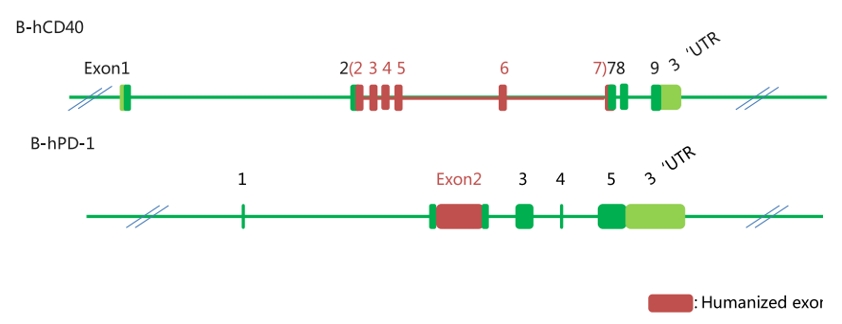
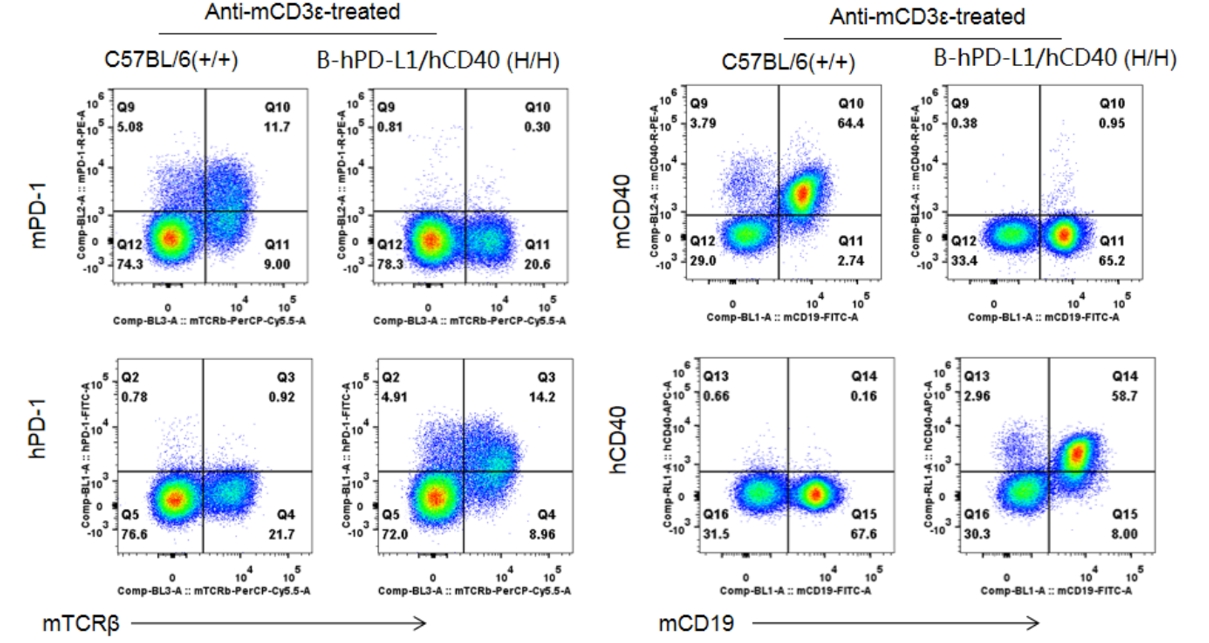
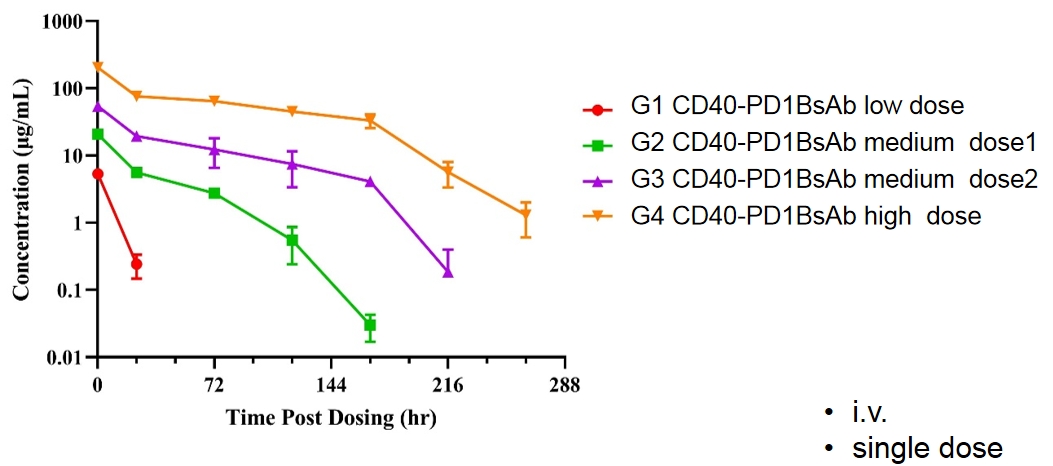
CD40-PD-1双特异性抗体在B - hPD-1/hCD40小鼠中的PK检测
HER2×TROP2 BsADC在NCI-H1975异种移植模型中的药动学分析
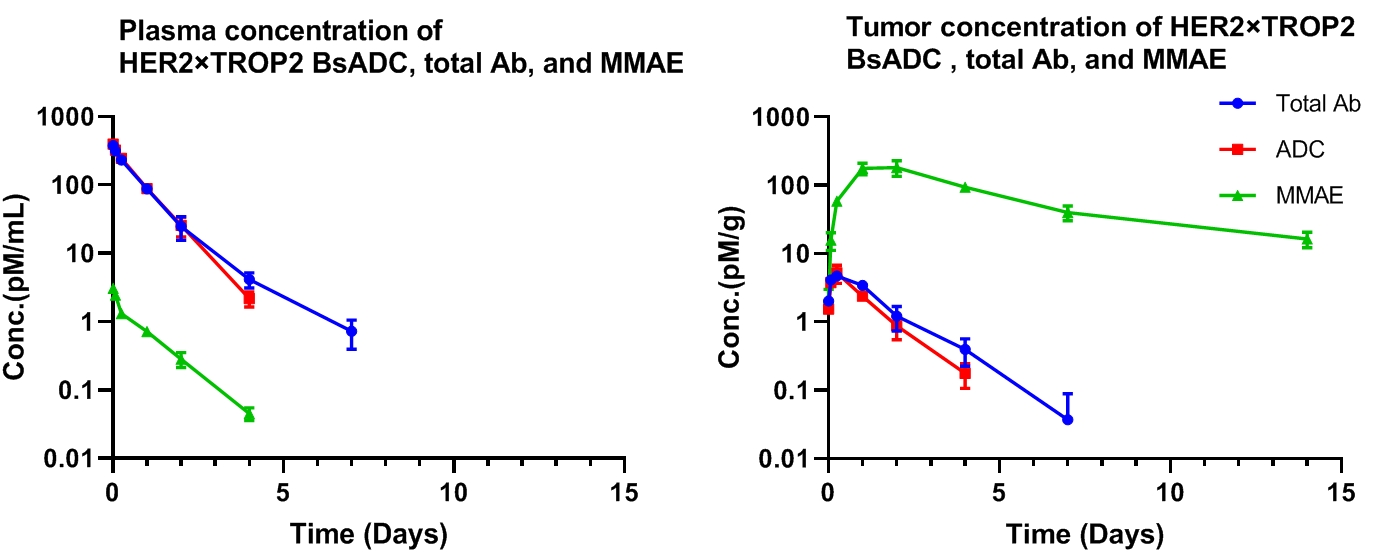
单次给药3mg /kg HER2×TROP2 BsADC后,发现有效载荷MMAE在肿瘤中积累,但在血浆中含量较低。这表明HER2×TROP2 BsADC已经达到了MMAE的有效肿瘤靶向递送,并且可能具有更好的抗肿瘤活性。
在使用生物药进行治疗的过程中,一些生物体会产生免疫反应,其中最显著的是抗药物抗体(ADA)。免疫原性是一种特殊物质引起免疫反应的能力。ADA-mAb免疫复合物的形成是单克隆抗体的额外清除途径,对体内单克隆抗体的治疗和消除具有重要影响。
常用的ADA检测方法利用ADA与药物特异性结合的特点,检测小鼠体内产生的抗药物抗体(本质上是小鼠抗人IgG)。
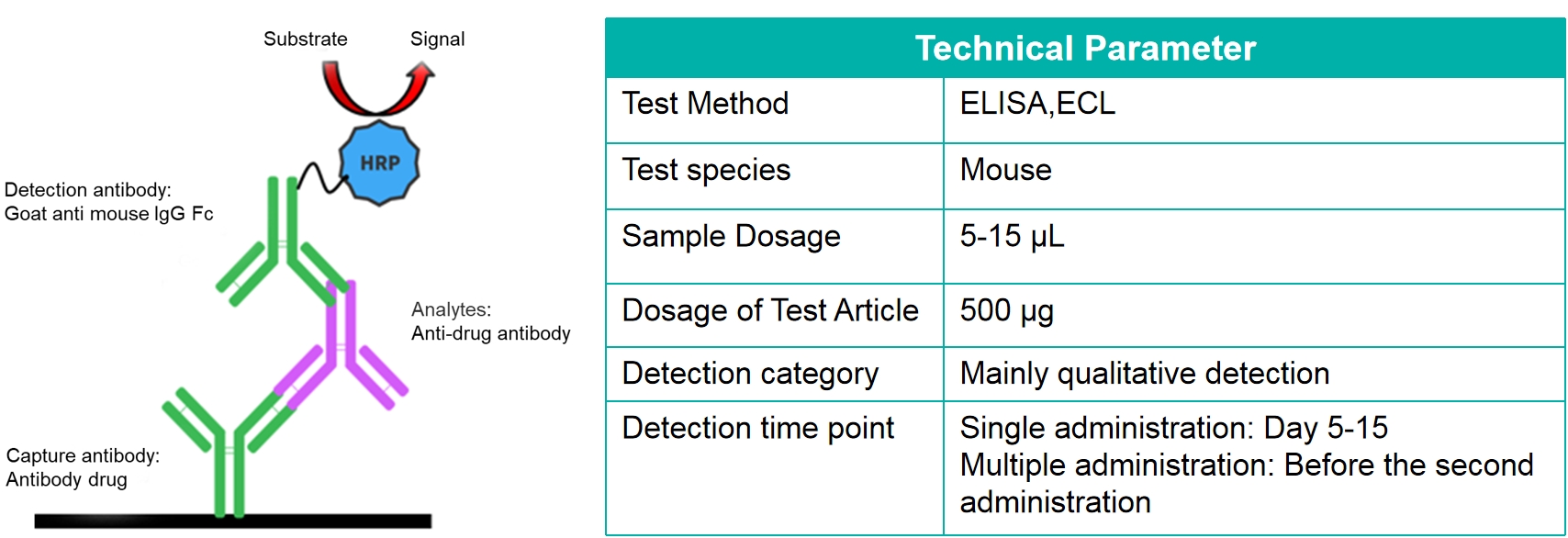
研究案例-小鼠血清中ADA的检测
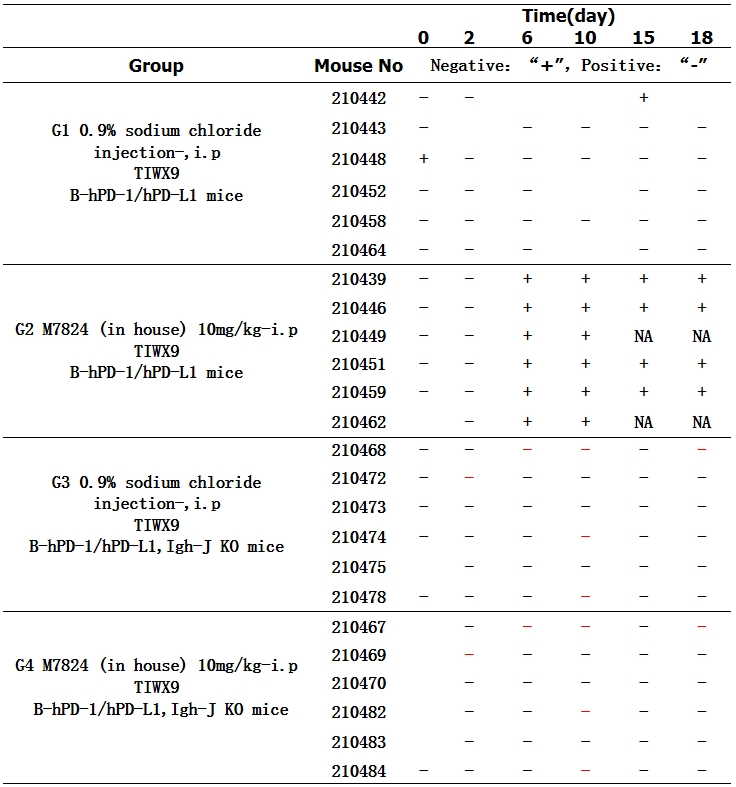
计算生理盐水组和给药前样本的信噪比值(SNR=单样本信号值/池串联信号值)。排除异常值后,利用剩余样本的信噪比计算筛选阈值1.24。将所有样本的信噪比值与筛选阈值进行比较,高于筛选阈值的记录为正“+”,低于筛选阈值的记录为“-”。NA:由于小鼠死亡无法取样。
参考资料
1. Guidelines for the survival bleeding of mice and rats.(2010).
2. Diehl K. H. A good practice guide to the administration of substances and removal of blood, including routes and volumes. J.Appl.Toxicol.21,15-23(2001).
3. Janet H, et al. Methods of Blood Collection in the Mouse.Lab Animal.29 (10):47-53.(2010).
4. Bioanalytical Method Validation Guidance for Industry (FDA 2018)
 苏公网安备:32068402320845号
网站建设:北京分形科技
苏公网安备:32068402320845号
网站建设:北京分形科技






 010-56967680
010-56967680 info@bbctg.com.cn
info@bbctg.com.cn