斑秃(alopecia areata,AA)是一种发生于毛囊的自身免疫性炎症性疾病,临床表现为非瘢痕性脱发。该疾病会对患者的情绪和精神产生不同程度的影响,而导致的焦虑和压力又会使斑秃病情加重或反复,形成恶性循环。[1]
根据毛发脱落的部位和程度,斑秃大致可分为2种。若头发全部脱落称为全秃(AT),全身毛发均脱落则称普秃(AU)。AA的特点是突然出现圆形或椭圆形的非瘢痕性脱发斑块,并伴有自发性缓解和恶化。最常见的临床表现是斑片状脱发。

斑秃的表现[2]
01、斑秃的发病机制
免疫豁免(immune privilege,IP)失效被认为是斑秃主要的驱动因素。与其他自身免疫性疾病一样,IFN-γ和IL-15的上调与AA的发病密切相关,NKG2D及其配体MICA也参与了该过程。正常毛囊(HF)上皮区域不表达MHC I类和II类分子,许多免疫抑制细胞因子和神经肽的存在也有利于创造正常HF部位的免疫抑制环境。但斑秃患者的HF区域的免疫抑制状态则会因为不同的原因被打破。
斑秃的发生涉及到2种不同的情形:(a)免疫豁免从毛囊开始崩溃:应激源刺激角质形成细胞上MICA蛋白的表达,导致NK细胞的激活和IFN-γ的分泌。进而MHC的活性增加,将自身抗原呈递给 CD8+T细胞、CD4+T细胞和自然杀伤 (NK) 细胞。(b)免疫豁免的崩溃也可能是由于大量的CD8+ NKG2D+效应记忆T细胞在区域淋巴结中上调,然后侵入毛囊。这些细胞同样会产生IL-15和IFNγ。IL-15 激活 JAK-CD8+T细胞中的 STAT 通路,导致它们产生更多的 IFN-γ 并形成正反馈回路。
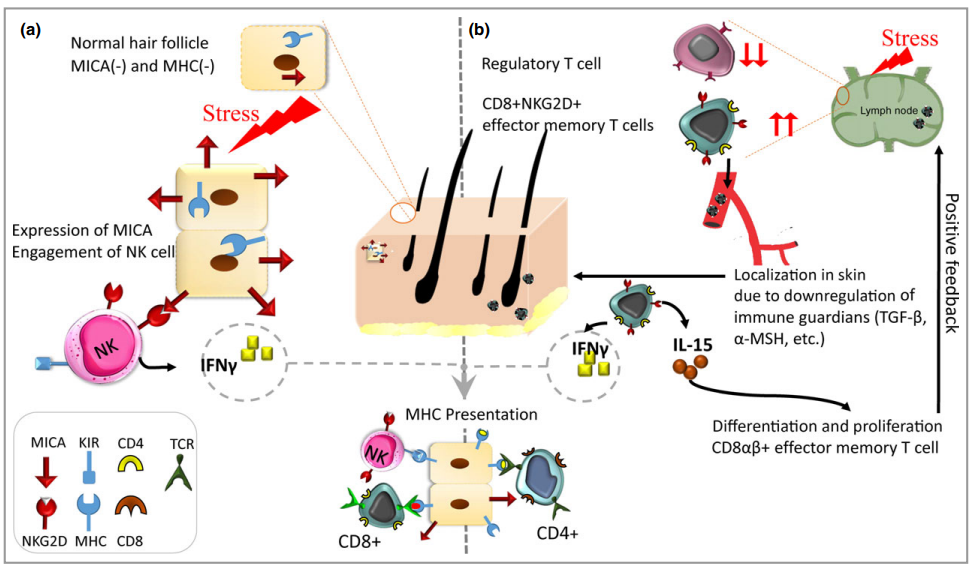
斑秃的发病机制[3]
由此可见,AA是一种T细胞依赖、抗原和器官特异性的自身免疫性疾病,会选择性地攻击生长期HFs、指甲和(很少)视网膜色素上皮。但它不局限于人类,也会发生在许多不同的哺乳动物物种中,包括小鼠和大鼠等。
02、动物模型
AA的人源化小鼠模型已被用于证明先前假设的CD8+T细胞和NKG2D+细胞在AA发病机制中的关键作用。为了进一步阐明人类AA的发病机制,即IP崩溃是如何被诱导的,以及CD8+相对于其他NKG2D+细胞、Treg细胞和其他潜在参与者在这一过程中的相对重要性,适当的动物模型是不可或缺的。现有研究中,可以通过化学诱导和皮肤移植的两类方式构建AA动物模型。化学诱导建模主要可通过咪喹莫特,环磷腺苷,IFNγ + poly(I:C)(多聚胞苷酸),IL6胚胎诱导等方式完成。移植诱导的模型中,可以通过移植小鼠皮肤,免疫细胞,病人皮肤到SCID小鼠中等方式完成造模。
1、药物模型:咪喹莫特背部涂抹
通过调整咪喹莫特使用的剂量和频率,可以摸索多种不同的造模方法,如:将咪喹莫特连续涂抹小鼠背部15天,有1cm 直径的圆形斑秃,停药后观察30天,无毛发生长,则说明造模成功;或咪喹莫特连续涂抹小鼠背部4周,每周3次,有1cm 直径的圆形斑秃形成,说明造模成功。
2、药物模型:环磷酰胺诱导
6~8周龄C57BL/6小鼠用乙醚麻醉后,将松香与石蜡1:1加热融化涂抹于背部,凝固变硬后揭去,8~9天后,诱导生长期毛囊产生。后腹腔注射环磷酰胺,4~5天后毛发开始脱落,说明造模成功。
3、药物模型:IFNγ+多聚胞苷酸(poly[I:C])
在C3H/HeJ小鼠体内每周注射一次IFNγ ,注射两次poly[I:C],约4周开始发病,8周发病率可达 80%。
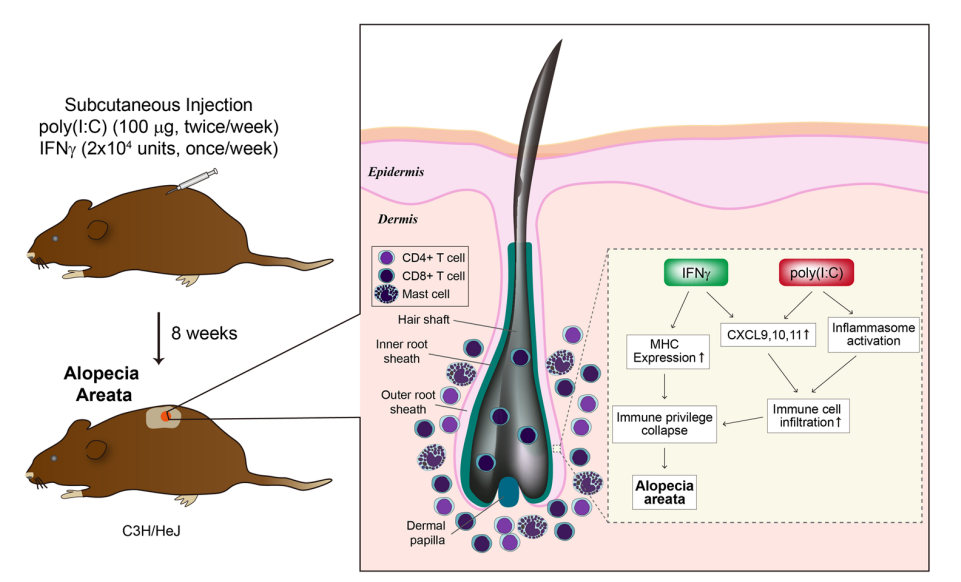
IFNγ+多聚胞苷酸诱导的AA模型[4]
4、移植模型:皮肤移植 + T细胞移植[5]
皮肤移植:5 weeks快速发病;8周后发病率达100%。皮肤移植2周后给予IL7c,会加速诱导AA的发生,给予IL7R抗体则会抑制AA的发生。

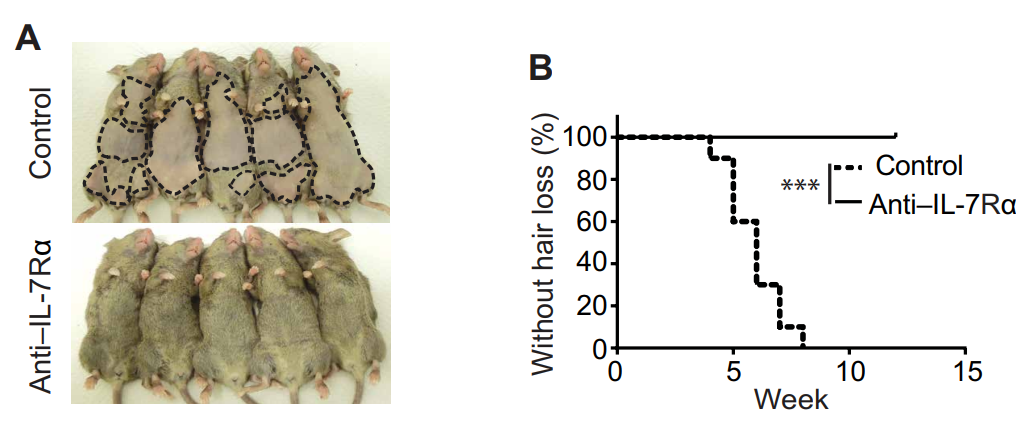
T细胞移植:给正常C3H/HeJ小鼠体内移植1E6数量活化的CD8+T细胞,7 周快速发病,10周后发病率达100%。
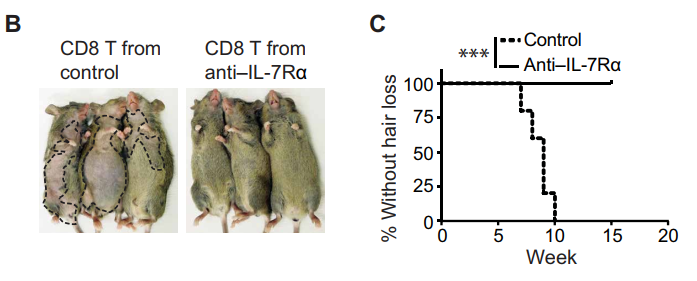
5、移植模型:淋巴结细胞移植[6]
从携带 AA 病变的 C3H/HeJ 小鼠制备淋巴结细胞,并与细胞因子混合物(IL2,IL7,IL15等)一起培养7天。受体小鼠静脉注射培养的淋巴结来源的细胞,会使得AA高频发生。
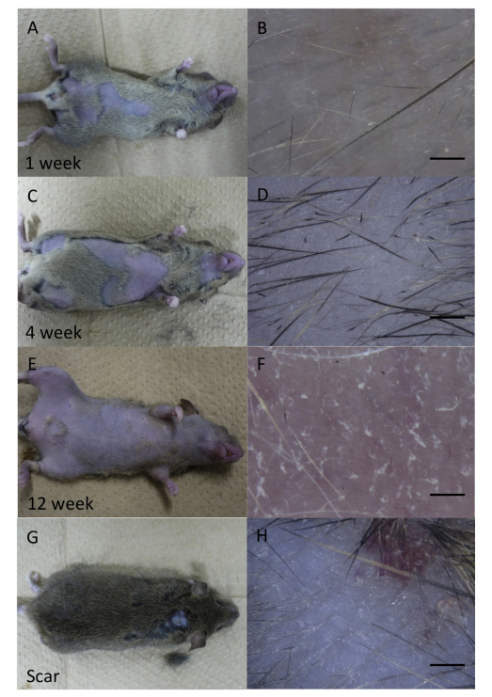
造模不同时期小鼠毛发情况[6]

不同时期造模成功率[6]
6、移植模型:人头皮移植
将正常人头皮的皮肤移植到SCID小鼠中,移植后2-4周会出现预期脱发(静止期脱发),之后用minoxidil治疗,促进毛发再生。从捐赠者的外周血中提取PBMC与高剂量IL2一起培养,期间会产生CD56+和NKG2D+的细胞。将富集物一起注射到全层皮肤移植物的下层,会观察到毛发的脱落。造模周期约为6个月。

人头皮移植造模过程[7]
03、模型特征
目前两类主要AA小鼠模型(C3H/HeJ与移植的SCID小鼠)中,每一种具体的模型都有明确的优缺点。在制定实验的过程中,应该根据具体的实验要求选择合适的模型。在自身免疫性疾病研究中更广泛地使用这些有趣的临床前模型会促进这一行业的迅速发展,并将推动该领域的创新和进步。[7]
表1 AA动物模型的主要特征[7]
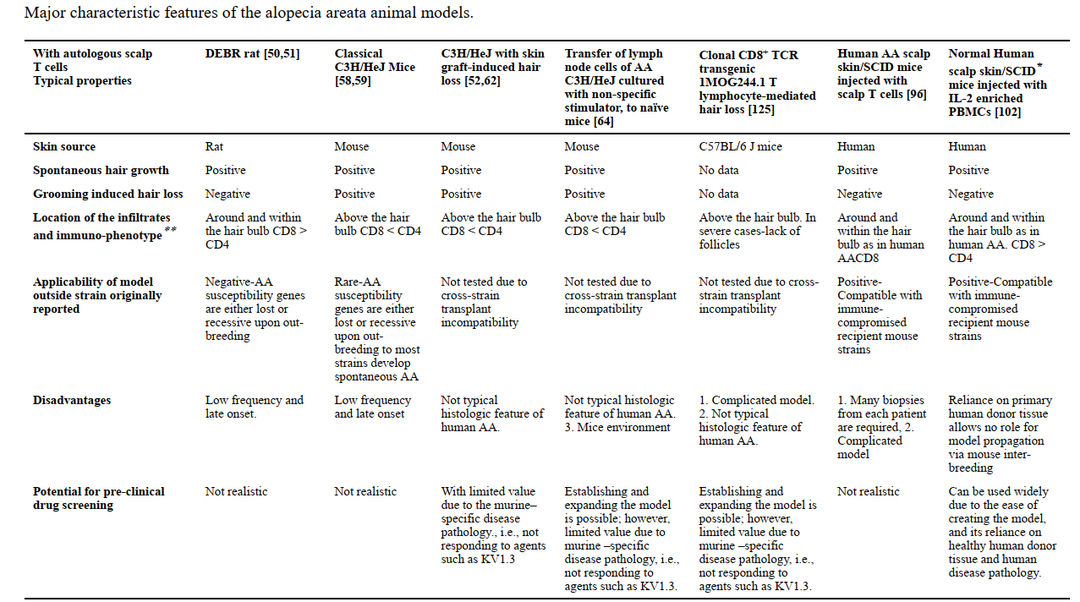
百奥赛图正在构建不同条件诱导的AA模型,欢迎大家与我们联系,作进一步了解与探讨。
参考文献
[1] Gilhar A, Kalish RS. Alopecia areata: a tissue specific autoimmune disease of the hair follicle. Autoimmun Rev. 2006 Jan;5(1):64-9.
[2] Rajabi F, et al. Alopecia areata: a review of disease pathogenesis. Br J Dermatol. 2018 Nov;179(5):1033-1048.
[3] Shin JM,et al. Induction of alopecia areata in C3H/HeJ mice using polyinosinic-polycytidylic acid (poly[I:C]) and interferon-gamma. Sci Rep. 2018 Aug 21;8(1):12518.
[4] Dai Z, et al. Blockade of IL-7 signaling suppresses inflammatory responses and reverses alopecia areata in C3H/HeJ mice. Sci Adv. 2021 Apr 2;7(14):eabd1866.
[5] Suzuki T, et al. Similarities of dermoscopic findings in alopecia areata between human and C3H/HeJ mouse. J Dermatol Sci. 2016 Aug;83(2):154-7.
[6] Gilhar A, et al. Autoimmune disease induction in a healthy human organ: a humanized mouse model of alopecia areata. J Invest Dermatol. 2013 Mar;133(3):844-847.
[7] Gilhar A,et al. Alopecia areata: Animal models illuminate autoimmune pathogenesis and novel immunotherapeutic strategies. Autoimmun Rev. 2016 Jul;15(7):726-35.






 010-56967680
010-56967680 info@bbctg.com.cn
info@bbctg.com.cn 苏公网安备:32068402320845号
苏公网安备:32068402320845号