新药研发具有耗资大,时间长,失败风险高的特点。临床前分子、细胞及小型实验动物水平的试验可以为药物作用机制阐述、药效验证等提供基础支撑。但由于人和小型实验动物的巨大差异与生物个体的复杂性,在基础研究到临床药物开发的转化上存在“死亡之谷”。如何实现从基础研究到临床的转化成为了新药研发中需要面对的巨大挑战。

图1. 生物医学研究中的死亡谷
犬与人的生活环境一致,饮食相似,身体结构、免疫系统和人的相似性也非常高,与实验环境下的小鼠相比具有良好的临床转化性。利用犬的自发疾病模型进行药物药效、安全性研究,可以架起一座桥梁,跨越新药研发的“死亡之谷”,实现从基础研究到临床的转化。
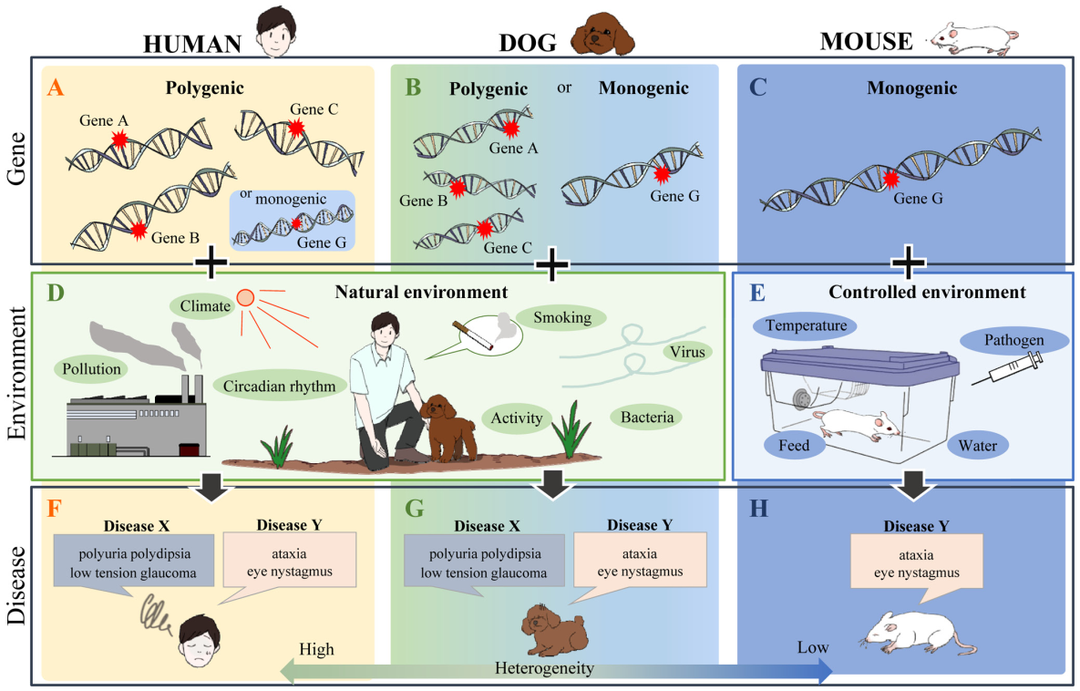
图2. 遗传和环境影响对人类、犬和小鼠疾病的影响
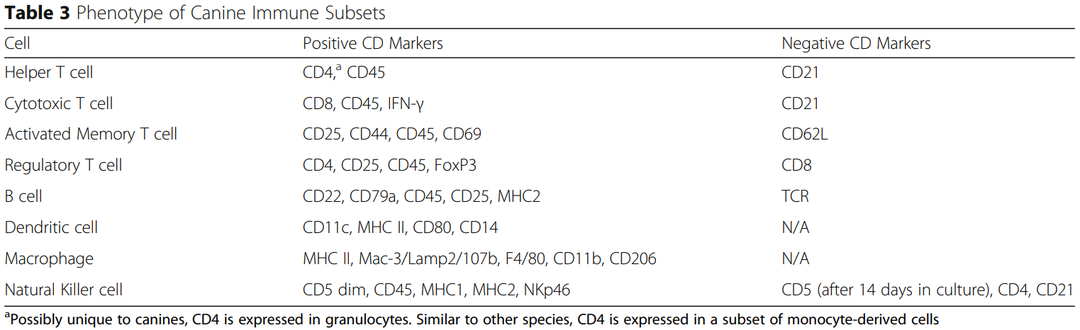
犬的免疫系统与人的免疫系统基本一致,免疫细胞亚型均包括细胞毒性T细胞,辅助T细胞,调节T细胞,B细胞,树突细胞,巨噬细胞,NK细胞等。疾病状态下,免疫应答也保持一致。
表1 犬免疫细胞分型
在肿瘤领域,犬自发肿瘤与人类有相似的药物治疗靶点,相似的信号传导通路,对常规疗法的反应或耐药机制以及转移和复发均具有相似性;组织病理学方面,犬和人中许多特定的癌症具有相同的特征(骨肉瘤,粘膜黑色素瘤,非霍奇金淋巴瘤,膀胱癌等);基因表达方面,犬和人的相应癌症之间的基因表达量相似,在转录水平上也表现出相似性。在临床治疗上,对人类有效的多种药物,对犬也同样有效。
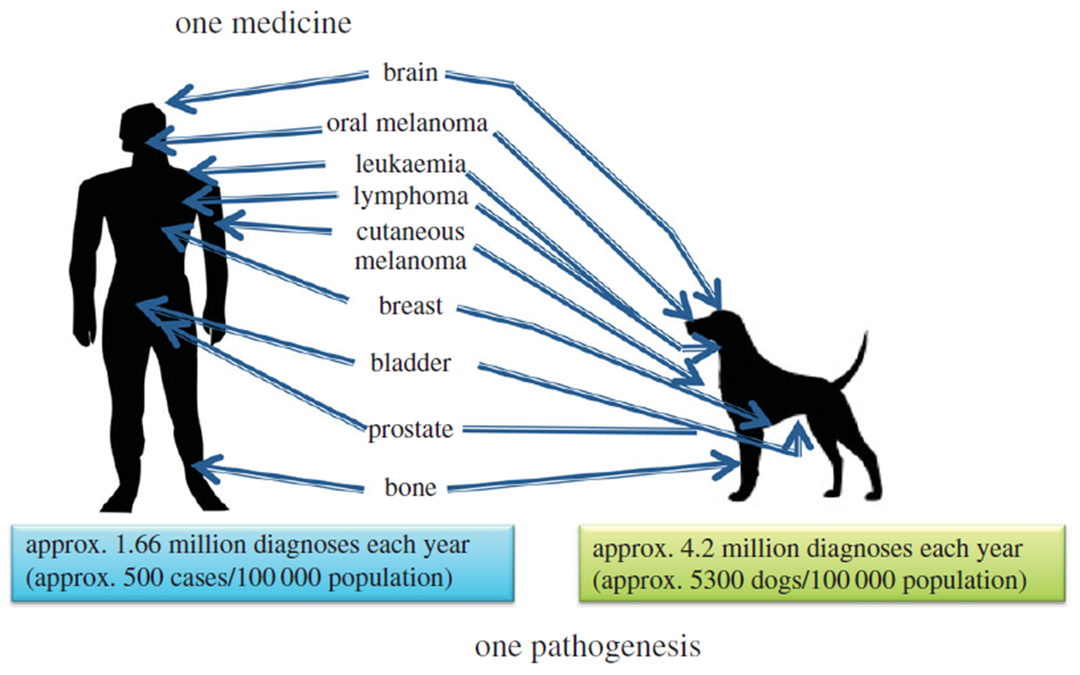
图3. 人类和犬的癌症相似性示意图
犬在新药研发的临床前及临床阶段均具有很高的应用价值。在肿瘤疾病领域,开展临床试验前,可以通过药物在自发肿瘤犬体内的药效研究,确定药物的生物活性、安全性、PK、 PD等情况,以用于指导I期临床试验设计。自发肿瘤犬的临床前研究非常适合于循环生物标记物的开发,验证和测试。使用肿瘤犬可进行用药前后的组织活检评估,同时快速分析多点采集的肿瘤组织。在药效研究中,通过影像学技术手段在治疗之前、期间和治疗后进行影像检查,可准确监测肿瘤的变化及转移情况。肿瘤犬的研究可以长期临床随访,而这在早期人体试验中通常是做不到的。在I期临床确定了药物的安全性之后,可以使用肿瘤犬进行给药剂量、给药周期和生物标记等的探索研究,指导II, III期临床试验。
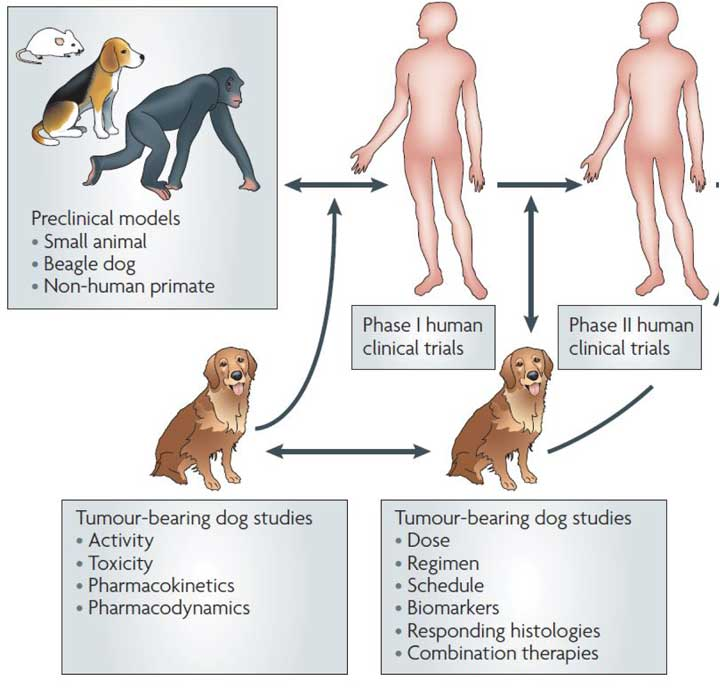
图4. 整合小鼠,实验犬,癌症犬的综合药物开发路径
由美国国立癌症研究所(National Cancer Institute,NCI)开发的靶向DNA组蛋白复合体的抗体偶联IL-12的NHS-IL12,在18只犬中进行了PK、PD和安全性测试。NHS-IL12在肿瘤犬体内展示出积极的响应,给药后外周血IL-10、IFN-γ明显升高,两只达到部分缓解(PR),其中一只犬口腔的肿瘤完全消退。基于在犬上的积极结果,NHC-IL12进行人体的I期临床试验。在人体内也引起了外周血IL-10、IFN-γ的升高,病人有较好耐受性。目前NHC-IL12的临床试验仍在进行中。
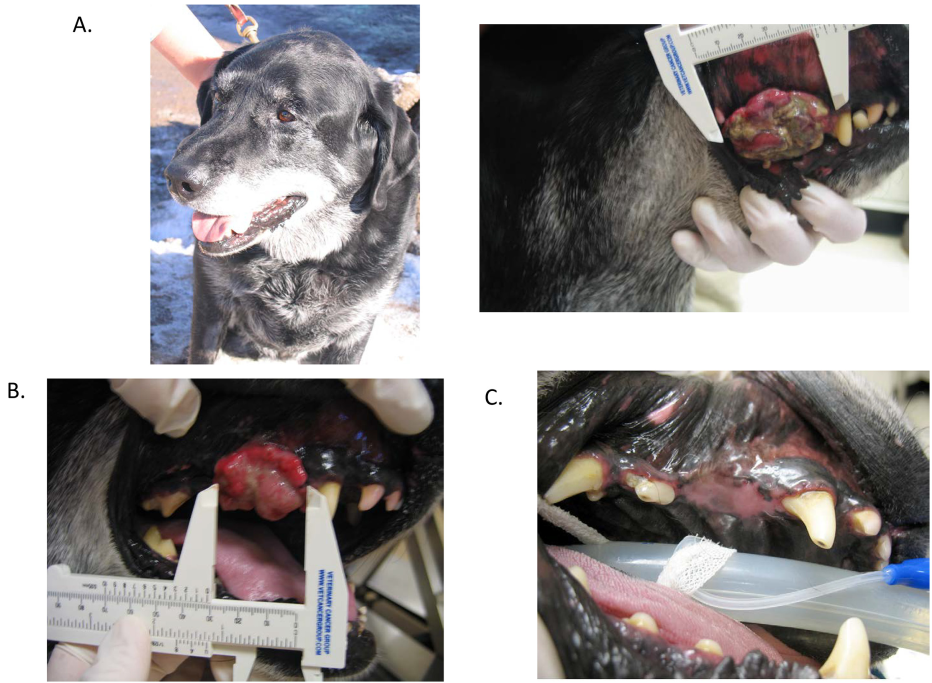
图5. NHS-IL12在患有恶性黑色素瘤的犬中的效应

图6. NHS-IL12治疗后犬血清IL-10, IFN-γ变化
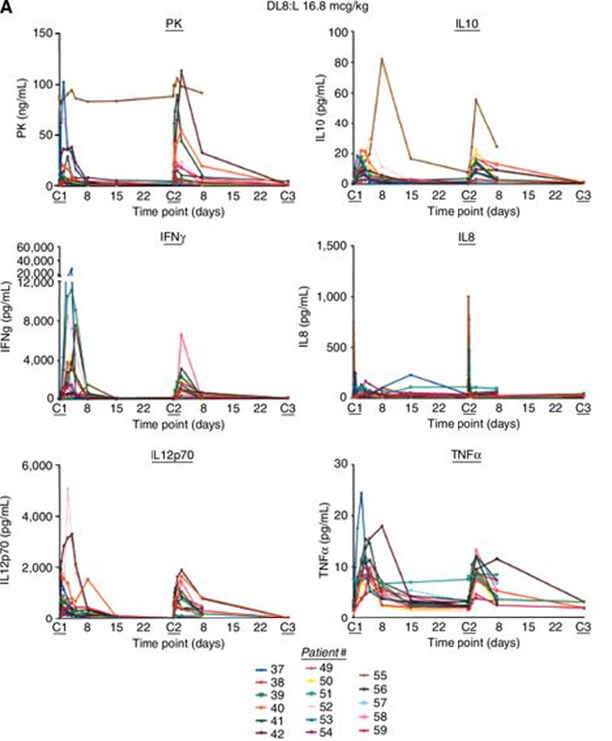
图7. I期临床实验中NHS-IL12治疗后人血清细胞因子变化
犬肿瘤治疗的临床试验是提高药物研发转化效率的重要保障,具有自发性肿瘤的犬作为治疗模型与小鼠相比具有许多优势,包括犬和人类基因组之间的广泛同源性,可比的遗传复杂性和肿瘤异质性,以及TME中类似的宿主-肿瘤相互作用。犬肿瘤治疗的临床试验为生物标记分析提供有价值的免疫监测数据,与人类研究相似,可以分析犬血清,PBMC和肿瘤组织中的免疫标记,鉴定对犬和人类患者均可获益的新型预测性和预后性生物标志物。这些结果将增强犬类免疫疗法试验的价值,加快新型免疫疗法的转化速度。由此,美国国立卫生研究院成立了比较肿瘤试验平台,该研究院会在癌症研究信息平台搜集犬试验信息,研究犬自发肿瘤作为人类癌症的转化模型,以改善对犬类和人类肿瘤的治疗。
随着物种特异性相关科技和技术的发展,犬类临床的研究将迎来进一步的突破,助力新药研发,提高临床试验成功率。
百奥赛图体外检测平台建立了犬血清中抗体药物浓度,抗药抗体ADA的检测方法;犬外周血细胞受体占位,免疫细胞分析,肿瘤TILs免分析及多种细胞因子检测;犬组织病理分析,毒性检测等技术。可提供犬疾病诊断,PK, PD, 毒性,细胞功能测试服务。
参考文献
1. Seyhan, A.A., Lost in translation: the valley of death across preclinical and clinical divide – identification of problems and overcoming obstacles. Translational Medicine Communications, 2019. 4(1).
2. Strauss, J., et al., First-in-Human Phase I Trial of a Tumor-Targeted Cytokine (NHS-IL12) in Subjects with Metastatic Solid Tumors. Clin Cancer Res, 2019. 25(1): p. 99-109.
3. Paoloni, M., et al., Defining the Pharmacodynamic Profile and Therapeutic Index of NHS-IL12 Immunocytokine in Dogs with Malignant Melanoma. PLoS One, 2015. 10(6): p. e0129954.
4. Park, J.S., et al., Canine cancer immunotherapy studies: linking mouse and human. J Immunother Cancer, 2016. 4: p. 97.
5. Momozawa, Y., The potential of translational research in dogs in human medicine. Translational and Regulatory Sciences, 2019. 1(1): p. 31-36.






 010-56967680
010-56967680 info@bbctg.com.cn
info@bbctg.com.cn 苏公网安备:32068402320845号
苏公网安备:32068402320845号