百奥赛图将参加于2023年4月14-19日在美国佛罗里达州奥兰多市举行的2023年美国癌症研究协会(AACR)年会,在现场展示25张海报,并设立展台#723,欢迎大家莅临交流。其中,9张百奥动物临床前研究创新动物模型海报展示安排如下:
靶点人源化小鼠海报
1.A Novel Triple Humanized B-hPD-1/hPD-L1/hCCR8 Mouse Model to Evaluate In vivo Efficacy of Combination Therapies
编号: 3233
场次: Combination Immunotherapies 1
展示时间: April 17, 2023, 1:30 PM – 5:00 PM
简介
调节性T细胞(Tregs)在肿瘤微环境中起抑制作用,因此改变或耗竭Treg功能已经成为抗肿瘤的重要治疗策略。CCR8在肿瘤浸润的Treg中高表达,靶向CCR8药物展示出降低肿瘤负荷和增加肿瘤免疫反应的治疗潜力。百奥动物自主开发的B-hPD-1/hPD-L1/hCCR8小鼠可以用于评估联合疗法的体内药效。
部分研究数据
抗PD-1抗体与抗CCR8抗体联合治疗

抗人PD-1抗体(内部合成)联合抗人CCR8抗体(内部合成)在B-hPD-1/hPD-L1/hCCR8小鼠(雄性,8周,n=6)接种 B-hPD-L1 MC38 plus肿瘤模型中的抗肿瘤活性。(A)肿瘤体积 (B)体重变化
2.B-hCD94/hNKG2A Mice Provide a Preclinical Tool for Evaluating Therapeutic Antibodies Targeting Human NKG2A
编号: 3286
场次: Combination Immunotherapies 2
展示时间: April 17, 2023, 1:30 PM – 5:00 PM
简介
免疫检查点NKG2A及共受体CD94在许多循环性NK细胞及肿瘤的CD8+T细胞亚群中表达。当CD94/NKG2A识别HLA-E-肽复合物时,蛋白酪氨酸磷酸酶SHP-1被募集到信号传导突触中,从而抑制信号传递来抑制其免疫活性。在临床前小鼠模型中,阻断NKG2A的抗体可恢复这些效应细胞的免疫反应,从而更好地抑制肿瘤生长。
部分研究数据
抗人PD-L1抗体与抗人NKG2A抗体联合治疗
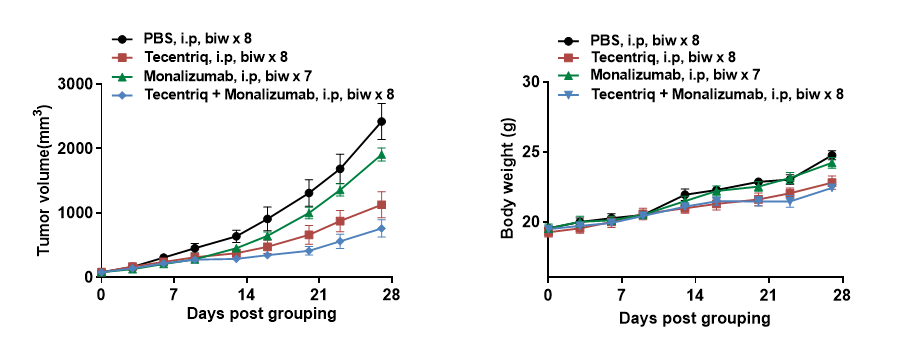
Tecentriq(合作方提供)和monalizumab(合作方提供)联合治疗在 B-hCD94/hNKG2A小鼠(雌性,6-7周,n=6)接种B-hHLA-E MC38肿瘤模型中的抗肿瘤活性。(A)肿瘤体积 (B)体重变化
3. Generation of Humanized TREM2 Mice for Preclinical Evaluation of Therapeutics Targeting Tumor-Associated Macrophages
编号: 5209
场次: Novel Preclinical Models for Cancer Immunotherapy
展示时间: April 18, 2023, 1:30 PM – 5:00 PM
简介
近年来,免疫检查点抑制剂改善了多种癌症的治疗方法,但总体反应率仍然较低,并且可能会发生耐药反应。这种耐药性被认为部分归因于肿瘤相关的巨噬细胞(TAM),TAM可以通过多种机制来抑制抗肿瘤免疫反应,从而导致肿瘤免疫逃逸。髓系细胞触发受体2(TREM2)是一种跨膜受体,免疫球蛋白超家族的一部分,在TAMs表面高度表达,在肿瘤组织中表达上调。缺乏TREM2的小鼠肿瘤进展较慢,并且对PD-1免疫疗法更敏感,表明TREM2是潜在肿瘤治疗靶点。
部分研究数据
抗人TREM2抗体的体内药效
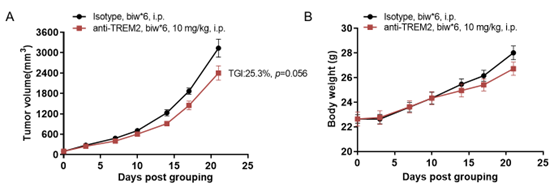
抗人TREM2抗体在B-hTREM2小鼠(C57BL/6)(雄性,6-7周,n=6)接种MC38肿瘤模型中的抗肿瘤活性。(A)肿瘤体积 (B)体重变化

抗人TREM2抗体(内部合成)在B-hTREM2小鼠(Balb/c)(雌性,10周,n=6)接种鼠乳腺癌EMT-6肿瘤模型中的抗肿瘤活性。(A)肿瘤体积 (B)体重变化
4. In vivo Efficacy Evaluation of Anti-Human VEGFR2 Antibodies in Humanized B-hVEGFR2 Mice
编号: 4592
场次: Advances in Angiogenesis
展示时间: April 18, 2023, 1:30 PM – 5:00 PM
简介
VEGF和VEGFR2结合形成二聚体激活下游信号通路,调节血管生成、血管发育、血管通透性和胚胎造血等。除了发育外,VEGFR2也与银屑病、类风湿关节炎、糖尿病性视网膜病及肿瘤生长和耐药性有关。多个VEGFR2抑制剂已进入临床研究阶段,并显示出令人鼓舞的结果。百奥动物构建的B-hVEGFR2小鼠模型能够用于评估VEGFR2靶向免疫疗法。
部分研究数据
抗VEGFR2抗体的体内药效评估
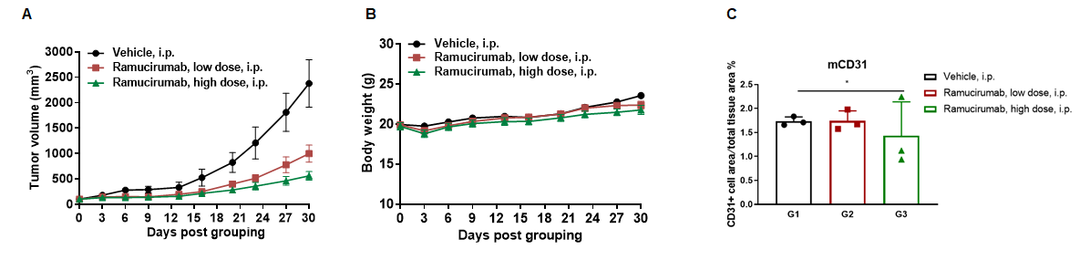
抗人VEGFR2抗体Ramucirumab (内部合成)在B-hVEGFR2小鼠(雌性,8周,n=6)接种MC38肿瘤模型中的抗肿瘤活性。(A)肿瘤体积 (B)体重变化 (C)肿瘤组织中CD31阳性细胞的占比
5. In vivo Efficacy of an Anti-Human IL11RA Antibody in B-hIL11RA Mice With APAP-Induced Liver Damage
编号: 3993
场次: Oncogenes and Tumor Suppressor Genes as Targets for Therapy 3
展示时间: April 18, 2023, 9:00 AM – 12:30 PM
简介
对乙酰氨基酚(APAP)过量是造成药物诱导的急性肝损伤的常见原因,因此APAP给药是常用的实验模型,可以再现剂量依赖的肝毒性。APAP诱导的肝损伤小鼠模型表现出IL11表达上调,表明靶向IL11或其受体IL1RA有潜在的治疗潜力。百奥动物制备的B-hIL11RA小鼠能够评估抗人IL11A抗体对于肝损伤的抑制作用,包括肝细胞死亡、肝小叶中心坏死等。
部分研究数据
抗人IL11RA抗体在APAP诱导的肝损伤B-hIL11RA小鼠模型中的体内药效评估
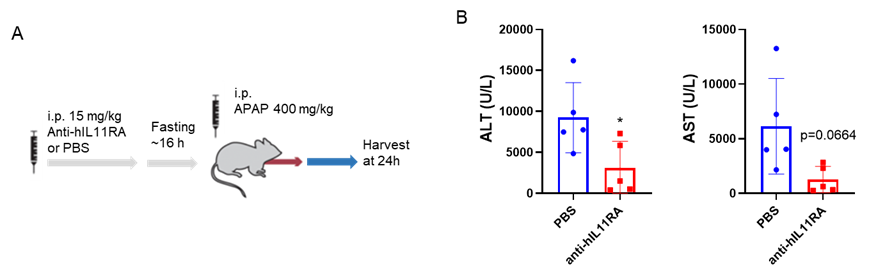
抗IL11RA治疗减少B-hIL11RA雄性小鼠中APAP诱导的肝损伤。(A)显示APAP诱导肝损伤小鼠模型的治疗剂量。用PBS/抗人IL11RA治疗的B-hIL11RA小鼠(雄性,8周,n=5)禁食过夜,并用APAP(400 mg/kg)反应24小时。 收集血液和肝组织进行分析。 (B)与对照相比,在抗人IL11RA抗体处理的雄性小鼠组中, ALT和AST的血清水平降低。 值表示为平均值±SD。 *p <0.05。
6. Novel Humanized CD36 Mouse Model for Therapeutic Studies
编号: 5196
场次: Novel Preclinical Models for Cancer Immunotherapy
展示时间: April 18, 2023, 1:30 PM – 5:00 PM
简介
肿瘤细胞上促进脂质运输的各种转运蛋白能够介导致癌信号通路的激活。CD36被认为是一种脂肪酸转运蛋白,并参与肿瘤生长和耐药。百奥动物构建了B-hCD36小鼠,是评估抗人CD36抗体的有力临床前模型。
部分研究数据
抗CD36抗体体内药效评估
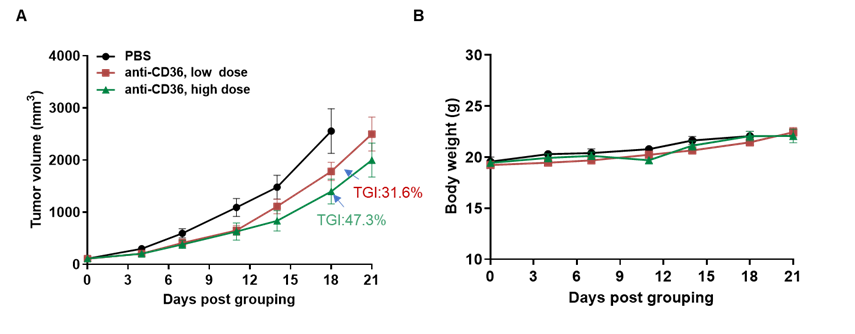
抗CD36抗体(内部合成)在B-hCD36小鼠(雌性,8周,n=6)接种MC38肿瘤模型中的抗肿瘤活性。(A)肿瘤体积 (B)体重变化
7. Humanized OX40/OX40L Mice as a Tool for Evaluating Novel Therapeutics
编号: 5178
场次: Modifiers of the Tumor Microenvironment
展示时间: April 18, 2023, 1:30 PM – 5:00 PM
简介
表达人源免疫基因的小鼠模型为新型免疫疗法开发提供了一个理想的临床前工具。包括OX40和OX40L在内的新兴免疫疗法能够增强T细胞激活、增殖和效应功能。阻断OX40/OX40L途径可以改善自身抗原特异性T细胞反应,并降低自身免疫疾病的免疫活性。百奥动物开发的B-hOX40/OX40L小鼠可以用于抗人OX40及抗人OX40L抗体的体内药效研究。
重度免疫缺陷小鼠海报
1. Development of Immunodeficient Mice Expressing Human IL3, GM-CSF, CSF1 and THPO for Improved Human Myeloid and Lymphoid Cell Reconstitution
编号: 5208
场次: Novel Preclinical Models for Cancer Immunotherapy
展示时间: April 18, 2023, 1:30 PM – 5:00 PM
简介
人免疫系统重建小鼠是研究人免疫反应及肿瘤免疫疗法的重要工具。但是由于人髓系细胞发育不良有一定局限性,这是因为造血细胞的分化、成熟和存活高度依赖几种人细胞因子。THPO(血小板素)可以增强功能性人造血干细胞的维持,并刺激巨核细胞的产生和分化,从而在骨髓中产生大量血小板。 IL3(白介素3)、GM-CSF(粒细胞-巨噬细胞集落刺激因子,CSF2)和CSF1(巨噬细胞刺激因子,M-CSF)可以促进包括髓细细胞的增殖和分化。百奥动物构建了B-NDG MGMT3小鼠,将4种细胞因子进行了人源化改造,是适合人髓系和淋系细胞重建的新型模型。
部分研究数据
人CD34+ HSCs免疫重建
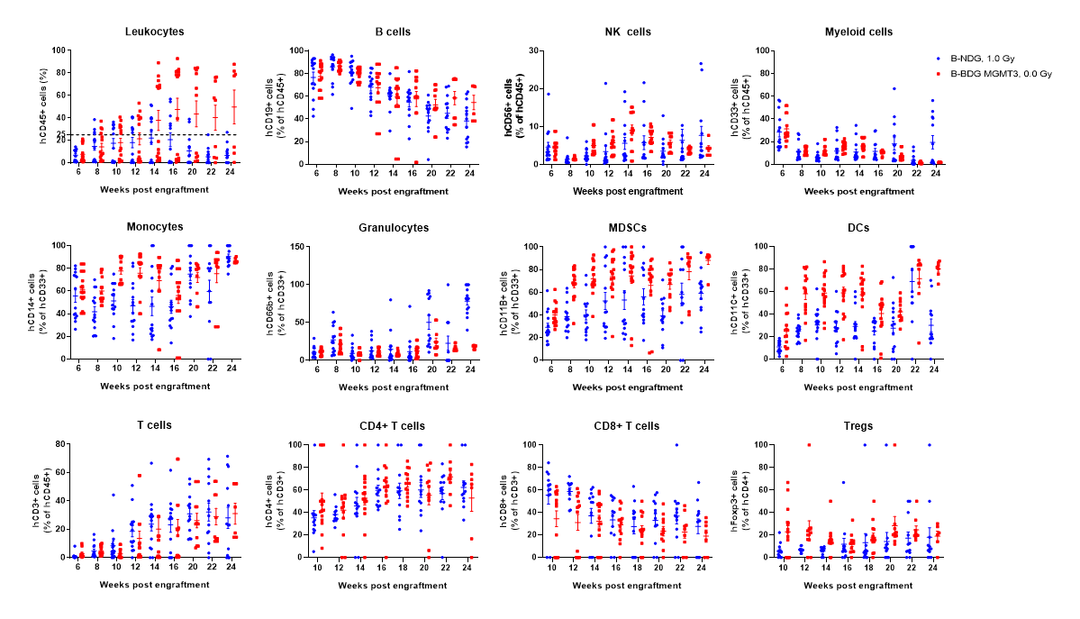
将人CD34+HSC(3E4)分别经面部颞静脉植入出生24-72小时的B-NDG小鼠和B-NDG MGMT3小鼠(双性别,n=15)。B-NDG小鼠提前经1.0 gy辐照预处理;B-NDG MGMT3小鼠不做辐照预处理。结果显示:植入12周后,B-NDG MGMT3小鼠中CD45+比例达25%,且持续升高,显著高于B-NDG小鼠比例。B-NDG MGMT3小鼠中重建的单核细胞、MDSC、DC和Treg细胞的比例高于B-NDG小鼠。
2. Development of MHC I/II Knock-Out Immunodeficient Mouse Strains for Alleviating GvHD Induced by Human PBMC Reconstitution
编号: 5207
场次: Novel Preclinical Models for Cancer Immunotherapy
展示时间: April 18, 2023, 1:30 PM – 5:00 PM
简介
重度免疫缺陷小鼠如B-NDG小鼠,缺乏成熟的T、B、NK细胞,已被广泛用作评估人免疫反应和肿瘤免疫疗法的模型。但当小鼠植入人外周血细胞(PBMC)时,由于人T细胞受体(TCR)与主要组织相容性复合物MHC I 和II的参与,出现了严重的急性移植物抗宿主病(GvHD)反应,缩短了动物的寿命,因此模型的评估窗口期较短。因此,百奥动物开发了B-NDG MHC I/II DKO小鼠,敲除小鼠MHC I 和II类分子,以减少人PBMC诱导的GvHD反应。
部分研究数据
B-NDG MHC I/II DKO plus小鼠显著降低了PBMC移植的GvHD反应的严重程度
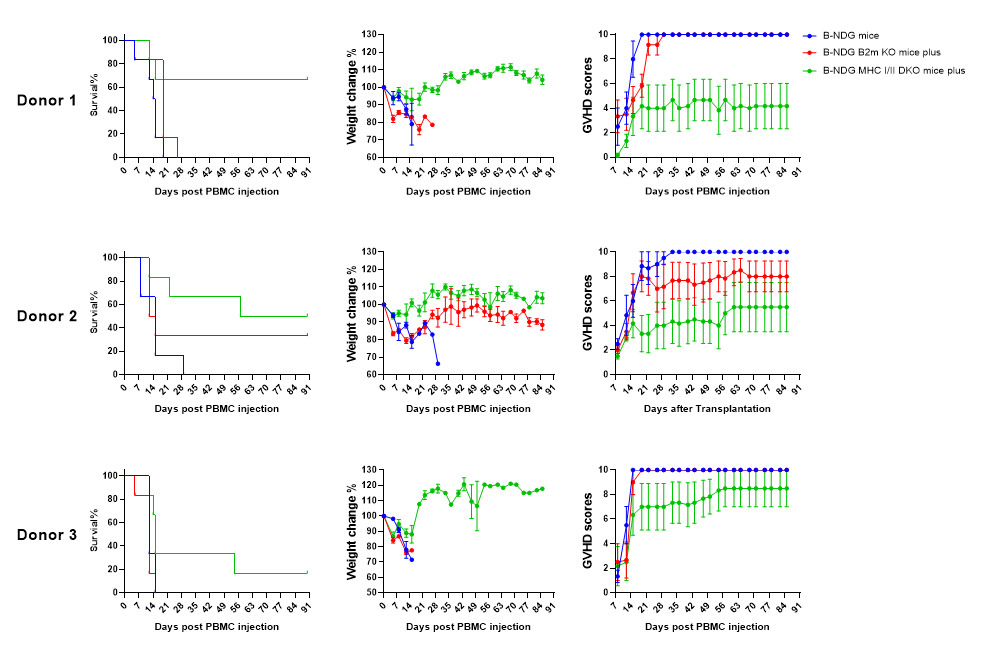
B-NDG小鼠,B-NDG B2M KO plus小鼠和B-NDG MHC I/II DKO plus小鼠诱导的GVHD严重程度的比较。
将三个健康供体的人PBMC(5×106)在第0天分别静脉注射到B-NDG小鼠,B-NDG B2M KO plus小鼠和B-NDG MHC I/II DKO plus小鼠(5周龄,雌性,n=5)。 (A)用Kaplan Meier存活曲线分析小鼠的存活率。 (B)体重变化。 (C)GvHD临床评分(每周两次)






 010-56967680
010-56967680 info@bbctg.com.cn
info@bbctg.com.cn 苏公网安备:32068402320845号
苏公网安备:32068402320845号