乙型(HBV)、丙型(HCV)肝炎病毒和非酒精性脂肪性肝病(non-alcoholic fatty liver disease, NAFLD),是引起肝硬化(cirrhosis)和肝癌(hepatocellular carcinoma, HCC)的主要驱动因素。近些年,广泛的HBV疫苗接种和针对HBC、HCV的高效抗病毒治疗手段的开发使得乙肝和丙肝有所好转。但世界范围内,肥胖症和2型糖尿病越来越流行,使得NAFLD及其进展性疾病非酒精性脂肪性肝炎(non-alcoholic steatohepatitis, NASH)的患病率成比例上升,并逐步取代病毒性肝炎,成为全球肝硬化和肝癌的发病率和死亡率上升的主要驱动因素。
流行病学显示,NAFLD在一般人群中的患病率约为25%,全球NASH患病率则在1.5%-6.5%之间[1]。NASH好发于中年男性,特别是超重肥胖或患有2型糖尿病的个体。同时NASH患者常常并发肥胖、糖尿病和心血管疾病等。因为这种疾病症状雷同于酒精性脂肪肝炎,但患者无酗酒史,故将其命名为非酒精性脂肪性肝炎(NASH)。
从病理角度,NASH最早起源于肝细胞中增加的脂肪合成,机体摄入的葡萄糖和游离脂肪酸是脂肪合成的原料。脂肪过载的肝细胞容易出现应激反应(stress),包括内质网应激、线粒体受损、氧化应激(活性氧ROS的产生)和脂毒性等,出现肝细胞损伤和炎症反应,进一步有可能恶化成肝硬化甚至是肝癌(图1)。

图1. NAFLD演变成NASH的过程以及NASH的病理特征[2]
对应的,治疗NASH的方法主要是抗脂肪化(减脂减重),抗炎和抗纤维化[3]。可以联合应用作用机制不同的药物进行治疗。
目前用于NASH治疗的药物主要包括[4]:
❶ 法尼酯X受体(FXR)激动剂,如奥贝胆酸(Obeticholic acid , OCA)(Intercept公司), Tropifexor和 Cilofexor;
❷ 成纤维细胞生长因子(FGF)变体:Efruxifermin, Aalafermin;
❸过氧化物酶体增殖物激活受体(PPAR)激动剂:Elafibranor, Lanifibranor;成纤维细胞生长因子(FGF)变体:Efruxifermin, Aalafermin;
❹ 胰高血糖素样肽-1(GLP-1)激动剂:Semaglutide;
❺ C-C基序趋化因子受体(CCR2/5)抑制剂:Cenicriviroc(CVC)等。
尽管关于NASH发病机制的研究已取得了大量进展,但在关键3期临床研究中,奥贝胆酸是唯一一种具有显著疗效的药物。至今仍没有欧美药监局获批的NASH治疗药物。通过改变饮食、增强锻炼甚至是手术来减肥仍然是改善NASH的主要方式。未来十年,NAFLD治疗领域仍需深耕。
对疾病机制的深入研究、评估新药药效等都离不开疾病动物模型。目前NASH疾病动物模型主要可以分为3类:饮食诱导、化学诱导和基因编辑动物模型。在这三种方法的基础上,也可以进行组合应用。今天,我们就来着重介绍百奥动物已经建立的3种NASH疾病模型。
NASH小鼠模型
西方饮食(western diet, WD)诱导的NASH小鼠模型
用西方饮食饲料,也就是高糖、高脂,高胆固醇配方的饲料诱导小鼠造模,可以看到明显的体重增加,血糖的升高,糖耐受能力的受损,以及肝脏转氨酶的升高,和血脂的升高。
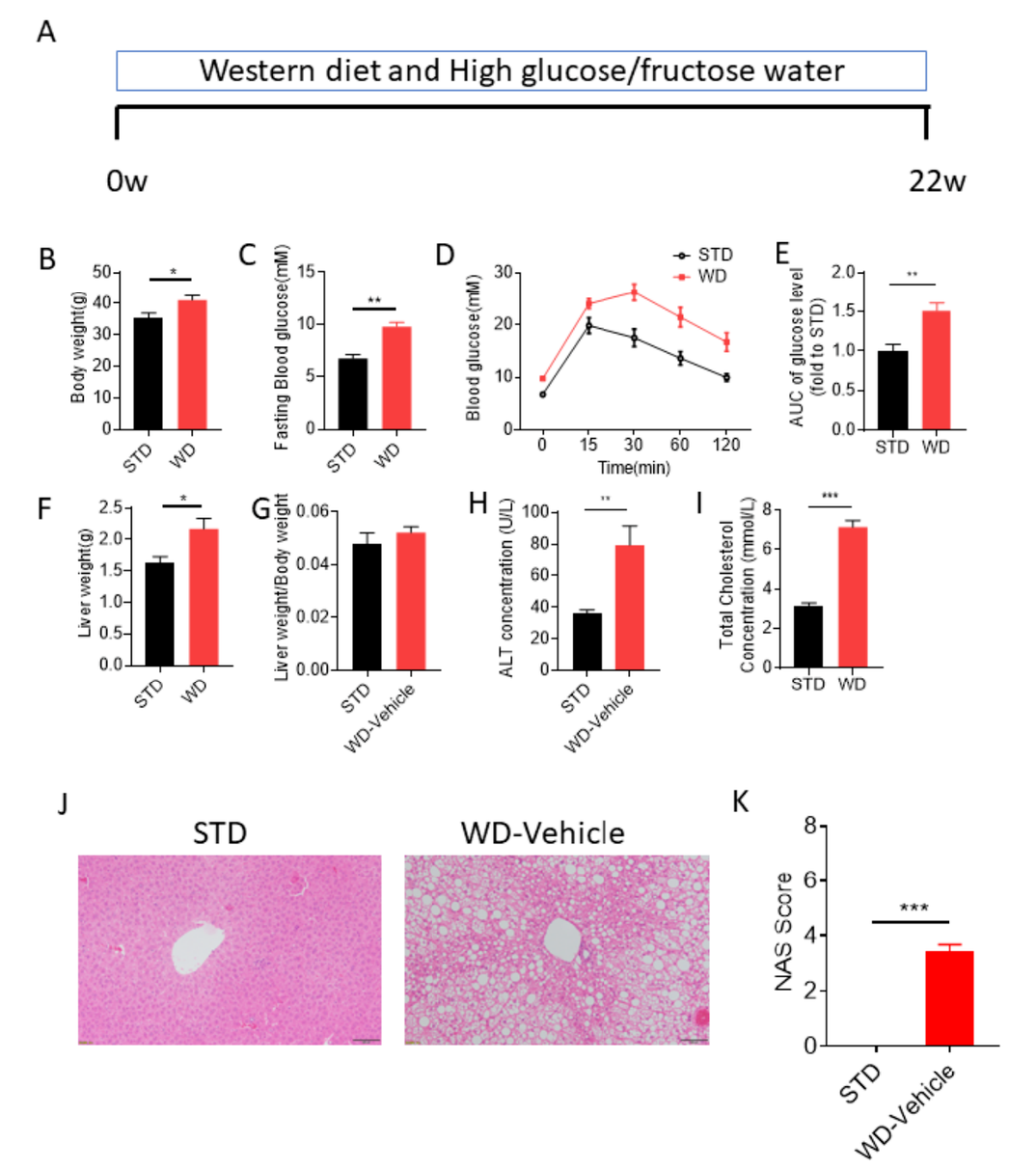
图2. 西方饮食诱导的NASH小鼠模型。(A) NASH模型建立:喂养标准饮食(standard diet, STD)或WD(含有21%的脂肪,50%的碳水化合物和1.5%的胆固醇)给8周龄C57BL/6雄性小鼠共22周;与STD相比,WD组小鼠(B)体重升高;(C)饥饿血糖升高;(D, E)葡萄糖耐受受损;(F)肝重上升;(G)肝重体重比;(H)血清谷丙转氨酶(ALT)水平升高;(I)血胆固醇升高;(J)肝脂肪变H&E染色示例;(K)NAS(NAFLD acticity score)评分升高。Data are means ±SEM; n=8-9 mice/group. *P <0.05, **P <0.01, ***P <0.001.
高脂肪蛋氨酸胆碱缺乏饮食(high fat methionine-choline deficient diet, HFMCD)诱导的NASH小鼠模型
HFMCD成分中含有60 kcal%脂肪,蛋氨酸、胆碱缺乏,该饮食诱导的NASH模型显示出肝损伤、肝脂肪变性和纤维化增加,伴随NAS评分增加。
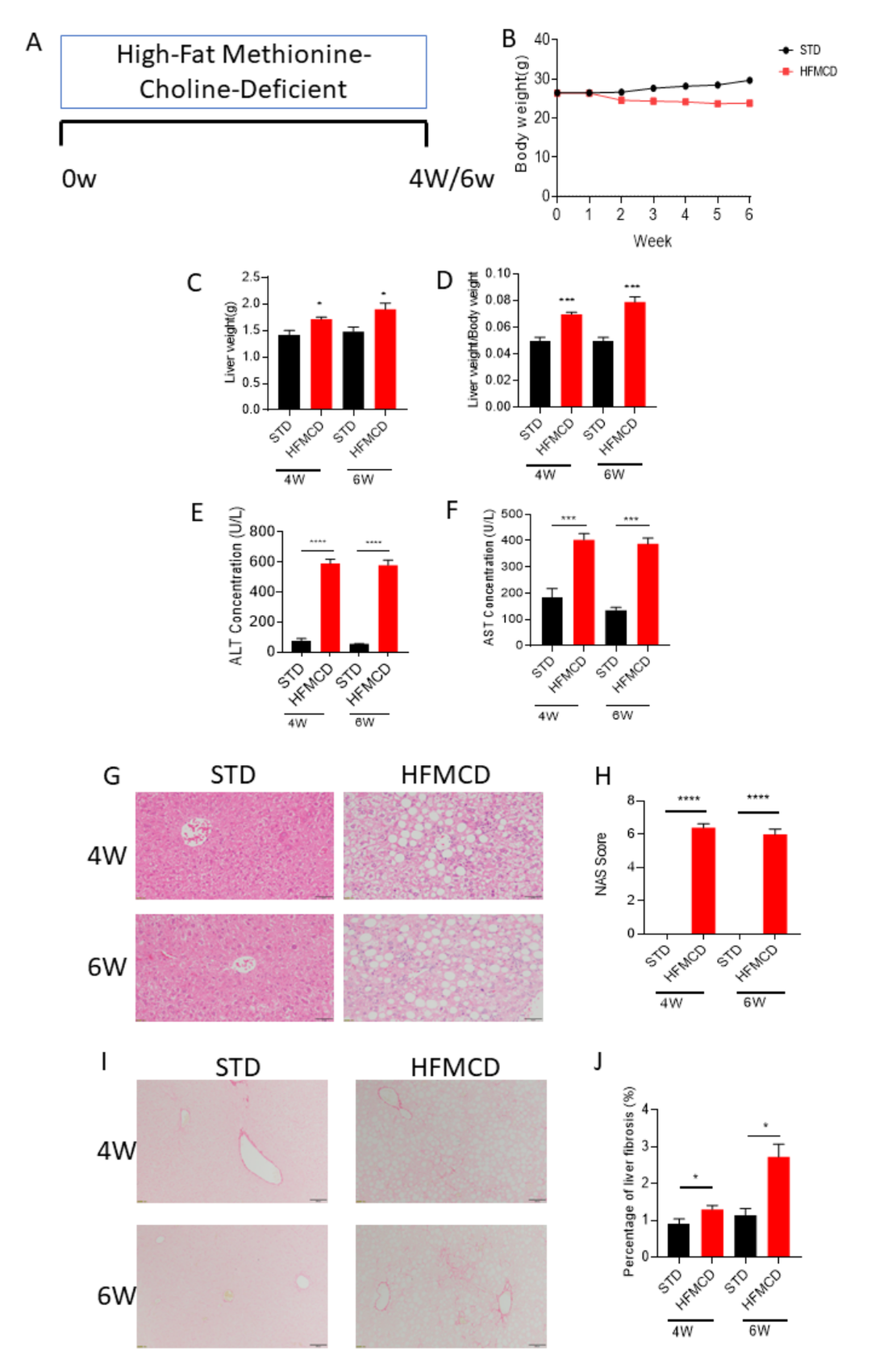
图3. HFMCD诱导的NASH模型。(A) NASH模型建立:喂养标准饮食(standard diet, STD)或HFMCD给8周龄C57BL/6雄性小鼠共4-6周;与STD相比,HFMCD组小鼠(B)体重无显著差异;(C, D)肝重和肝重体重比上升;(E, F)谷丙转氨酶(ALT)和谷草转氨酶(AST)水平升高;(G)肝脂肪变和炎症H&E染色示例及(H)NAS(NAFLD acticity score)评分升高;(I)肝纤维化天狼星红染色示例及(J)统计分析。*P <0.05, ***P <0.001, ****P <0.0001.
药效学研究表明,雷公藤红素(celastrol)可以减轻HFMCD引发的NASH。
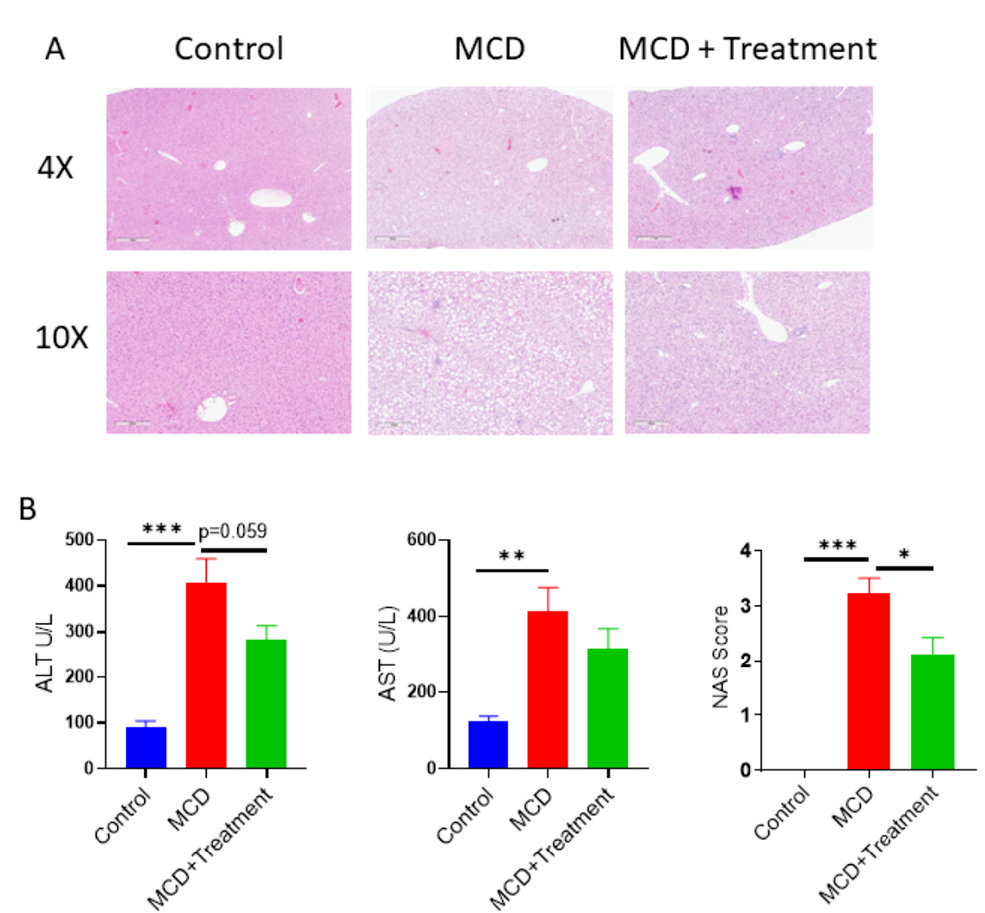
图4. 雷公藤红素(celastrol)可以减轻MCD引发的NASH。(A)H&E染色示例雷公藤红素处理后肝脂肪变和炎症减少;(B)ALT,AST,NAS评分在雷公藤红素治疗后均有好转。
四氯化碳(CCl4)诱导的NASH小鼠模型
四氯化碳(CCl4)注射诱导模型,引起明显的肝脏炎症和纤维化。

图5. CCl4诱导的NASH小鼠模型。(A) NASH模型建立:8周龄的雄性C57BL/6小鼠腹腔注射CCl4,浓度分别为:0.25、0.5和0.75 mL/kg,每周2次。分别诱导4周、6周和8周后进行血生化及组织学染色分析。(B)体重;(C, D)肝重和肝重体重比。
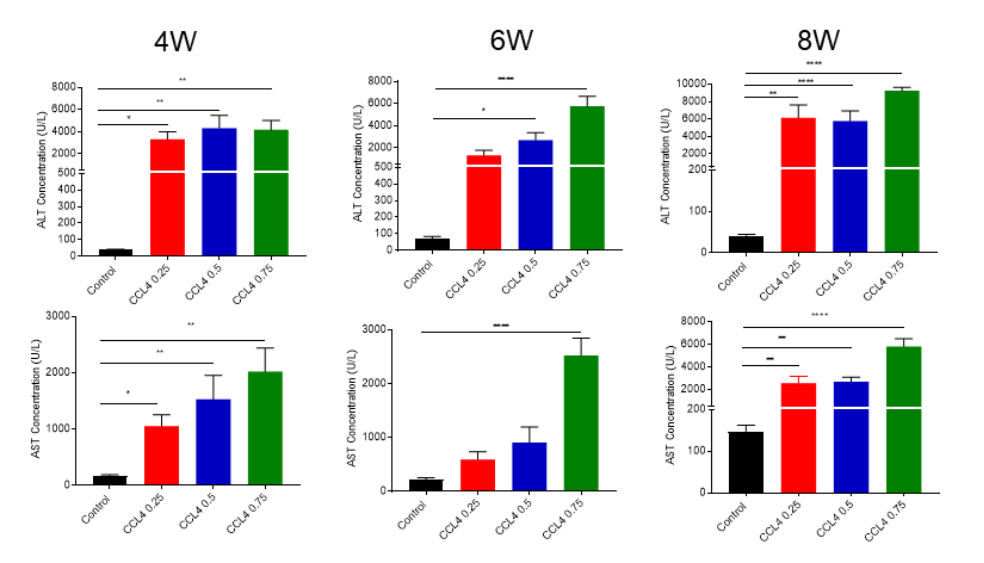
图6. 对CCl4诱导的NASH小鼠模型的肝损伤相关表型分析。

图7. H&E染色示例CCl4诱导后肝炎症增加。Scale bar: 50 um.
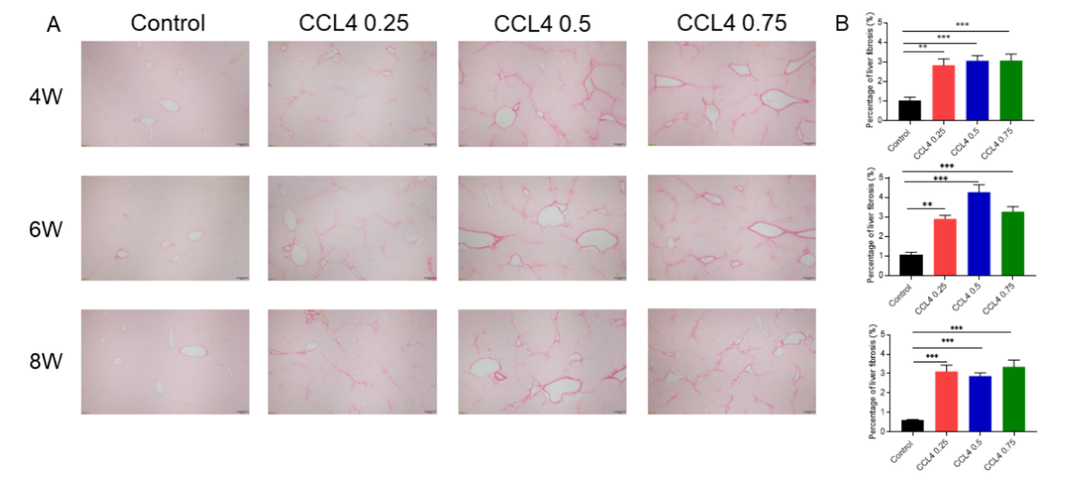
图8. 天狼星红染色及其统计分析表明CCl4诱导后肝纤维化加重。
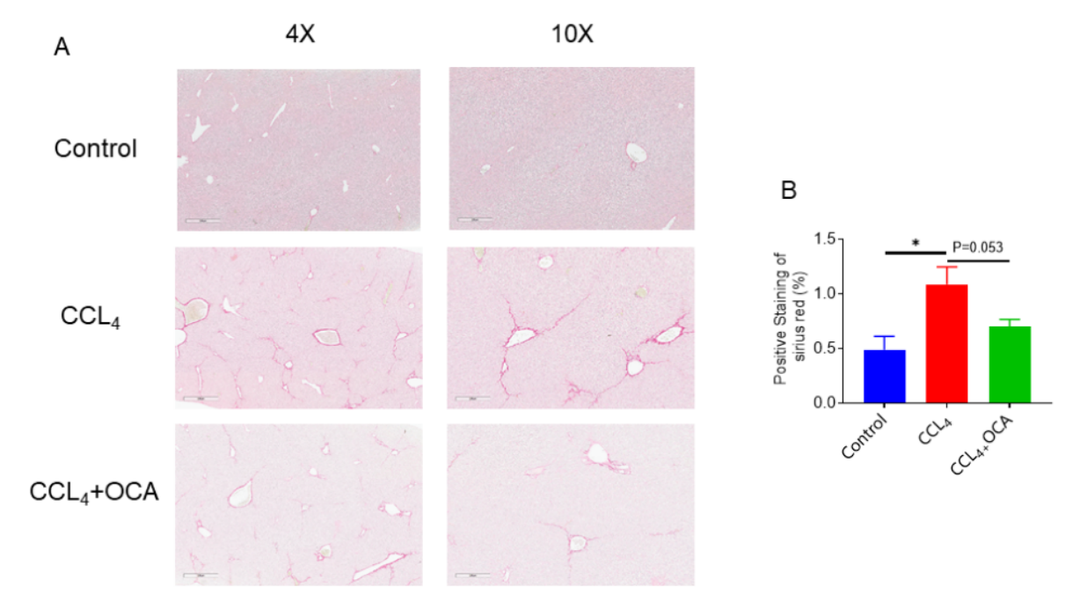
图9. 天狼星红染色及其统计分析表明奥贝胆酸(Obeticholic acid , OCA)治疗后肝纤维化减轻。
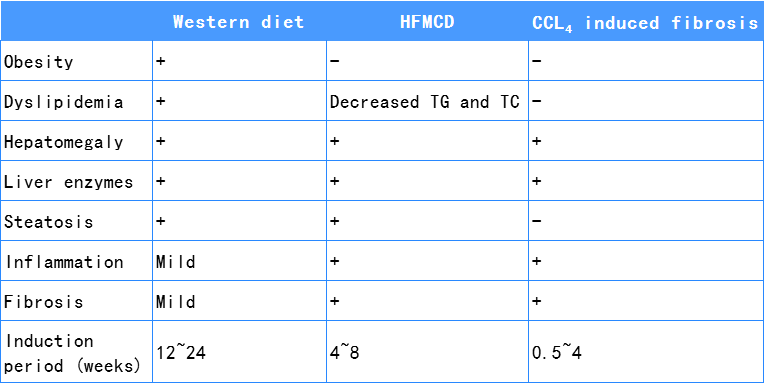
综上所述,三种NASH小鼠模型的特征总结如下
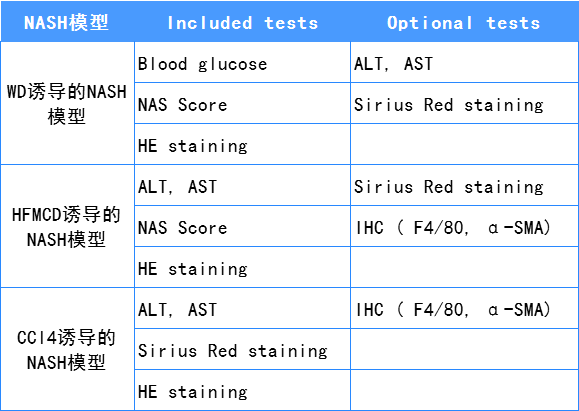
NASH疾病模型的检测指标
百奥动物能够提供的关于NASH疾病模型的检测指标包括
参考资料:
[1] 诺和诺德医学资讯:https://mp.weixin.qq.com/s/bj9u_NSQOUWNgCYEi2qTsg
[2] Huby, T., Gautier, E.L. Immune cell-mediated features of non-alcoholic steatohepatitis. Nat Rev Immunol (2021). https://doi.org/10.1038/s41577-021-00639-3
[3] Dufour J, Caussy C, Loomba R. Combination therapy for non-alcoholic steatohepatitis: rationale, opportunities and challenges. Gut 2020; 69:1877-1884.
[4] 药明康德:首款NASH疗法再度延后,患者何时才能迎来第一缕曙光?http://www.ii77.com/yangsheng/292978.html






 010-56967680
010-56967680 info@bbctg.com.cn
info@bbctg.com.cn 苏公网安备:32068402320845号
苏公网安备:32068402320845号