随着人口老龄化的加深,中枢神经系统退行性疾病已变成现代社会严重的医学问题。目前,大量研究表明多种中枢神经系统(CNS)疾病,例如帕金森病、阿尔兹海默症、脑肿瘤和多发性硬化等疾病的发生、发展与治疗,都与血脑屏障(blood brain barrier, BBB)关系密切。
如今,虽然抗体类药物凭借其靶向的高度特异性已经在多种疾病的治疗中获得成功,但在CNS相关疾病的治疗中却遇到了瓶颈,实现跨血脑屏障进行药物递送成为一重大挑战。如何在维持血脑屏障结构功能完整性的前提下提高药物递送效率,改善相关疾病的治疗,是今后研究CNS相关疾病的重要方向。
血脑屏障的结构与功能
1913年,Goldman 直接将染料注射进了动物的蛛网膜下腔,得到了脑组织着色,其他部分不着色的结果,此结果在1900年 Lewandowsky 正式提出了血脑屏障这一概念的基础上进一步证实了其存在。
血脑屏障(BBB)是一种大脑血管、细胞以及其它组成大脑组织之间的保护性屏障,主要由周细胞、脑毛细管内皮细胞、基膜、星形胶质细胞足突和脑血管内皮细胞间的紧密连接组成,能为大脑提供一种防御机制来抵御血液中的外来病原体和毒素等(图1)。BBB通过严格控制特定营养物质,以及限制有害异生物质分子的通过,来维持CNS 稳态;但另一方面在开发CNS生物药时,由于BBB的存在,导致生物药在大脑中的含量仅相当于血浆的 0.01-0.1%,为实现跨血脑屏障进行药物递送带来了巨大的难度。
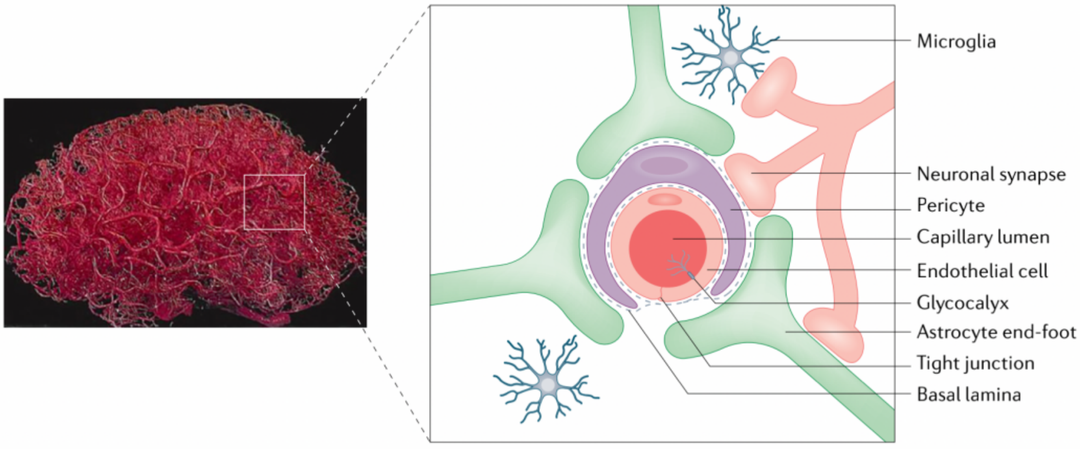
图1. 血脑屏障示意图[1]
脑部药物递送手段--受体介导的胞吞作用(RMT)
大脑中生物药物递送技术包括侵入式和非侵入式技术,利用非侵入式技术跨BBB主要是利用内源性胞吞的过程,例如吸附介导的胞吞作用, 载体介导的胞吞作用(CMT)和受体介导的胞吞作用(RMT)(图2)。在这些过程中,RMT 已成为BBB递送研究最广泛的过程。
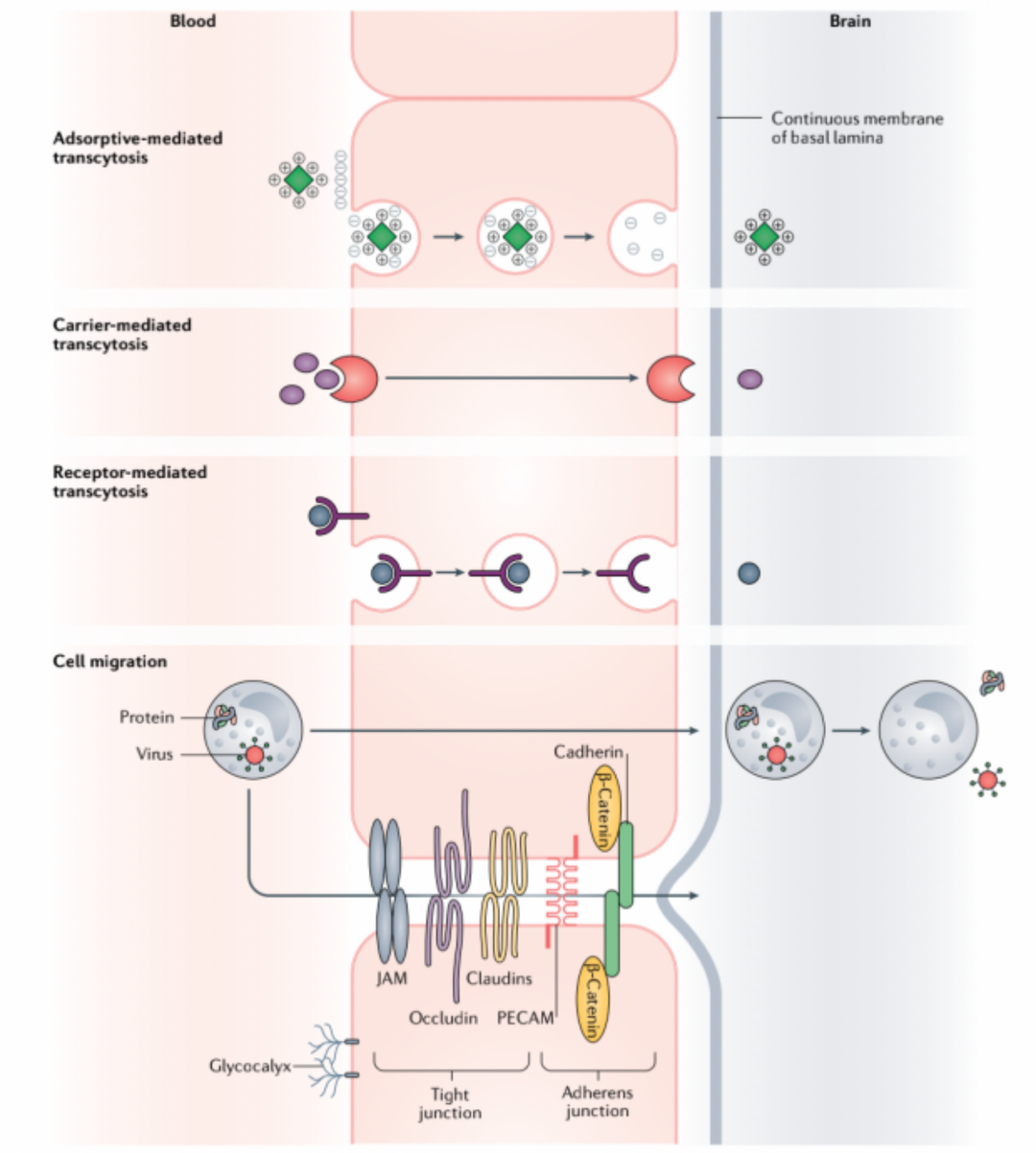
图2. 穿越BBB的生物转运机制[1]
为了通过RMT过程达到最优的治疗药物递送效率,靶受体蛋白应在脑血管的内皮细胞中高表达,同时在外周血管中最低限度表达。遵循这一思路,过去几十年大多数研究都集中于已知在血脑屏障细胞上高表达的靶点,例如转铁蛋白受体(TFR),胰岛素受体(IGF1R),CD98重链(CD98HC)等,针对这些靶点正在进行的药物临床试验(图3)将表明基于RMT的技术是否可安全有效地将治疗相关药物剂量递送至CNS,同时将外周和/或脱靶毒性作用降至最低。
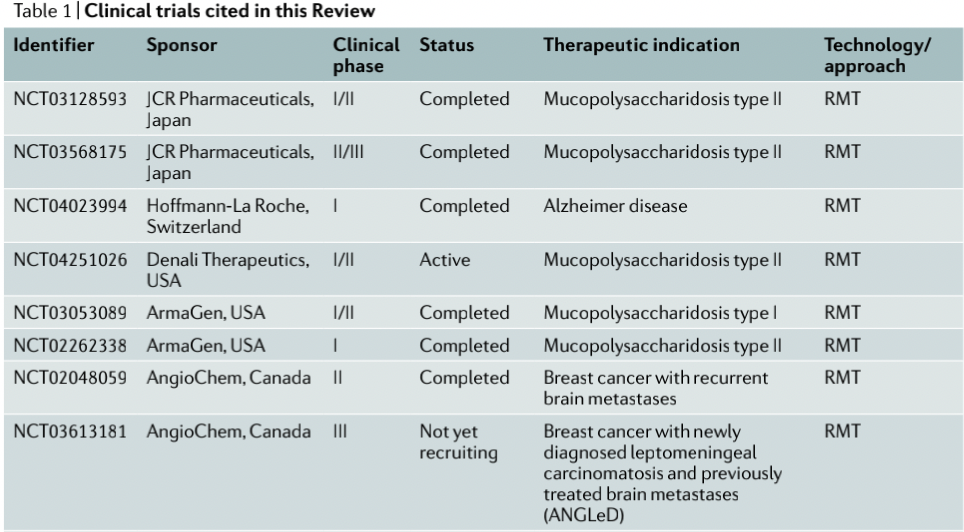
图3. 部分基于RMT进行的临床研究[1]
转铁蛋白受体(TFR1)
转铁蛋白(TF)结合铁是通过与其受体,即 Transferrin Receptor 1(TFR1)相互作用而实现的。TF 与 Fe3+相互作用形成全铁 -TF,并与 TFR1 受体结合,在细胞内吞作用下进入核内体。在偏酸性核内体的环境中,Fe3+ 与Tf分离,同时STEAP3将 Fe3+ 还原为 Fe2+ ,并被二价金属离子转运蛋白1(DMT1)转运到细胞质中,然后释放了Fe3+ 的TF与TFR1组成 TF/TFR1 复合物,通过胞吐作用回游到细胞表面。在细胞表面,转铁蛋白(TF)与受体TFR1分离,成为脱铁 -TF,然后再与Fe3+重新结合参与铁循环。整个过程完成后TF和TFR1被循环利用,进入细胞摄取铁的下一个周期中。
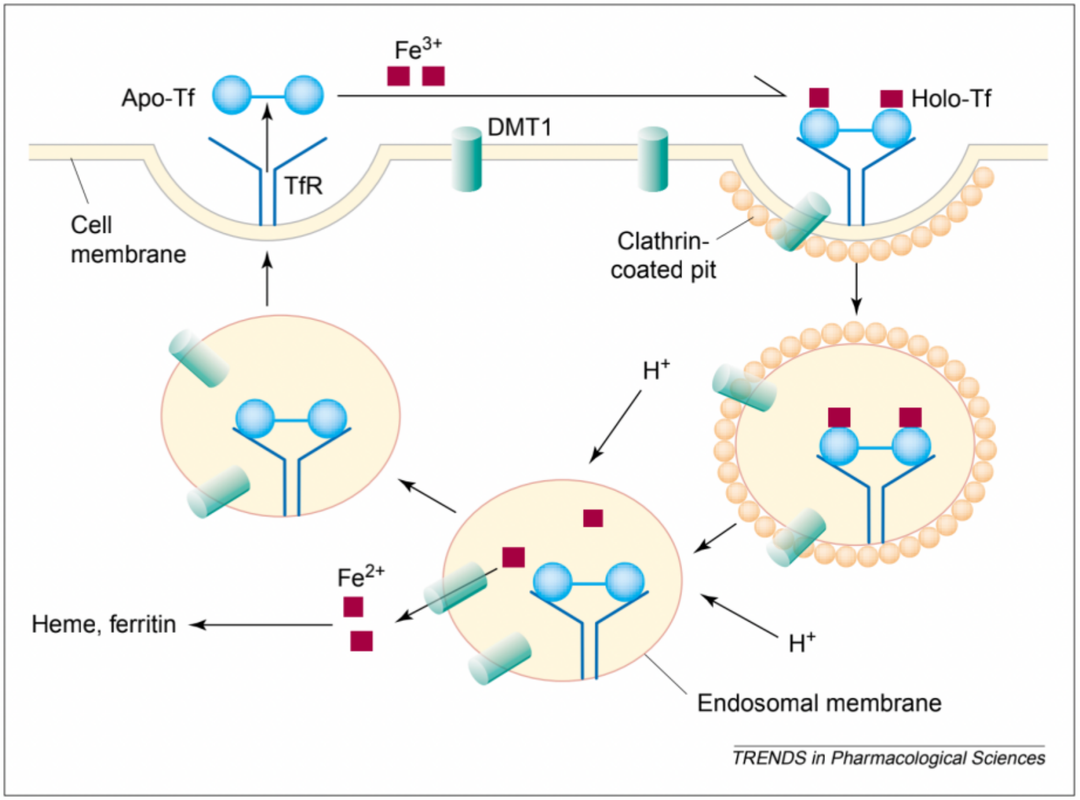
图4. 转铁蛋白循环机制[2]
转铁蛋白受体(TFR1)是用于基于RMT的大脑递送方法中研究最广泛的靶蛋白,TFR1在血脑屏障上高表达,识别携带铁的转铁蛋白将其转运到细胞内,从而介导铁的脑内转运。多项研究证明能够使用转铁蛋白或者 TFR1为靶点来转运药物到脑内,并在动物模型中得到验证。
针对TFR1靶点机制研究和新药开发的需求,BioMice 百奥动物自主研发的 B-hTFR1 mice 是评估蛋白治疗药物对CNS的有效递送的优质临床前实验动物模型。
B-hTFR1 mice 验证数据
红细胞蛋白表达分析
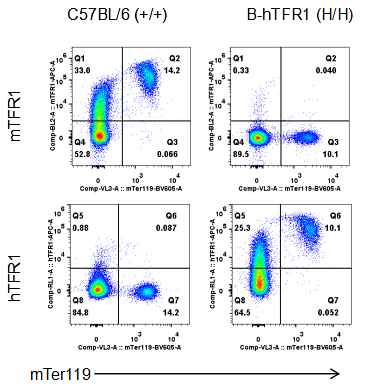
流式细胞术分析纯合B-hTFR1小鼠中TFR1表达
采集野生型小鼠和纯合 B-hTFR1小鼠的骨髓,采用种特异性抗TFR1抗体进行流式分析。小鼠TFR1在野生型小鼠中检测到。人TFR1仅在纯合B-hTFR1小鼠中检测到,而在野生型小鼠中检测不到。
TFR1抗体的体内PK评价
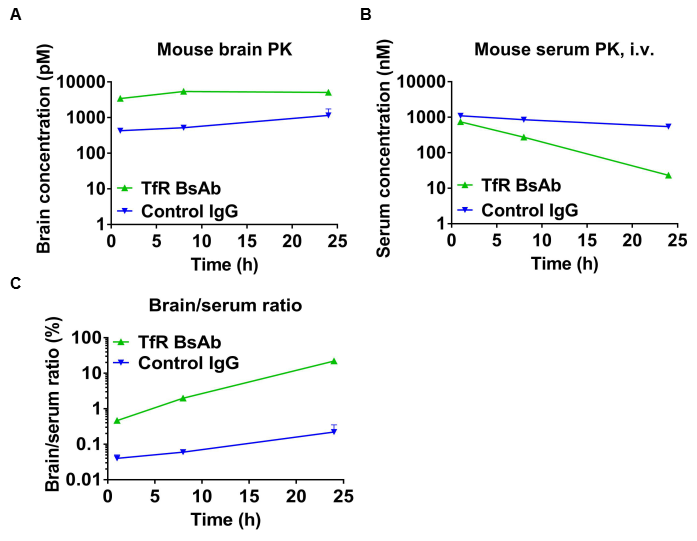
抗人TFR1双特异性抗体(BsAbs)的体内药代动力学(PK)评价
如图所示,抗人TFR1 BsAbs在剂量后表现出更高的血清清除率和增强的脑暴露。研究结果证实,B-hTFR1小鼠的大脑能够摄取静脉注射的抗人TFR1 BsAbs。平均值±SEM。
溶质载体转运蛋白 -CD98 重链(CD98HC)
溶质载体转运蛋白:CD98HC在小鼠大脑毛细血管和微血管中高度富集,并且位于脑内皮细胞的管腔和离腔表面。最近使用能够识别CD98HC和 β‑分泌酶 1(BACE1)的双特异性抗体进行的一项研究表明,将这些抗体静脉注射到小鼠体内可实现药物的大脑递送,并伴随着Aβ产生显着减少。CD98HC/BACE1双特异性抗体在大脑递送中的效率比TfR/BACE1双特异性抗体高 80‑90%,表明靶向CD98HC可能更有效[3]。
针对CD98HC靶点,BioMice 百奥动物自主研发的B-hCD98HC mice助力CNS相关疾病的临床前药物评价。
B-hCD98HC mice 验证数据
蛋白表达分析
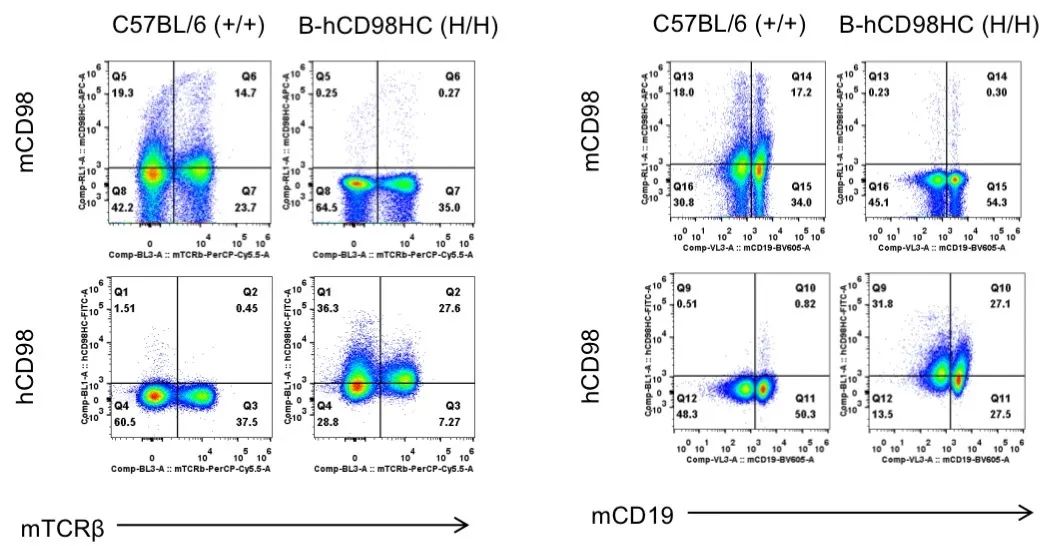
流式细胞术分析 B-hCD98HC 纯合小鼠 CD98 的表达
取野生型小鼠和纯合 B-hCD98HC小鼠脾细胞,用种特异性抗CD98抗体进行流式细胞术分析。野生型小鼠中检测到小鼠CD98。人CD98在 B-hCD98HC纯合小鼠中检测到,而在野生型小鼠中未检出。
胰岛素样生长因子 1 受体(IGF1R)
胰岛素样生长因子 1 受体(IGF1R)在大脑和脑血管中表达。因此,不干扰IGF1结合的抗体与IGF1R的结合可能是在BBB中提供生物治疗剂的一种有前景的策略。在最近的一项研究中,产生了针对IGF1R且远离IGF1结合位点的结构域的新型骆驼单域抗体(VhHs),体外模型中显示与非靶向VhH相比,大鼠的脑和脑脊液暴露量更高。
BioMice 百奥动物针对IGF1R靶点机制研究自主研发的B-hIGF1R mice,是评估蛋白治疗药物对CNS的有效递送的优质临床前实验动物模型。
除以上部分受体介导的胞吞作用外,越来越多的技术已经开始被用于探索增强生物类药物递送到脑部,如外泌体技术,基于腺相关病毒(AAV)的基因递送技术等。随着研究的深入,打破血脑屏障,攻克脑部药物递送的难题指日可待!
参考资料:
[1]Terstappen, G.C., Meyer, A.H., Bell, R.D. et al. Strategies for delivering therapeutics across the blood–brain barrier. Nat Rev Drug Discov 20, 362–383 (2021). https://doi.org/10.1038/s41573-021-00139-y
[2] Li H , Sun H , Qian Z . The role of the transferrin-transferrin-receptor system in drug delivery and targeting.[J]. Trends in Pharmacological ences, 2002, 23(5):206-209.
[3] https://mp.weixin.qq.com/s/5AW3VfVa_xQzHeAVDVPU7A






 010-56967680
010-56967680 info@bbctg.com.cn
info@bbctg.com.cn 苏公网安备:32068402320845号
苏公网安备:32068402320845号