ImmunoGen 与 FRa ADC 药物 Elahere 的最新消息
近日,艾伯维宣布将溢价95%以101亿美元现金收购ImmunoGen,获得全球首款叶酸受体α(FRα)ADC药物Elahere(索米妥昔单抗)。Elahere已于2022年11月获FDA批准用于治疗铂耐药卵巢癌,2023年前三季度销售额达2.12亿美元。
2023年5月3日,ImmunoGen宣布Elahere的Ⅲ期临床研究MIRASOL取得成功,研究纳入453名受试者,与化疗相比,Elahere末线治疗卵巢癌的中位总生存期(OS)为16.46个月vs 12.75个月,中位无进展生存期(PFS)为5.62个月vs 3.98个月,客观缓解率(ORR)为42.3% vs 15.9%。安全性方面,三级及以上TRAE为42% vs 54%,因不良事件导致的停药率为9% vs 16%。总体来看,Elahere无疑是首个延长末线卵巢癌的药物,具有良好的疗效与安全性优势[1]。
FRα简介
叶酸是人体所必需的维生素之一,参与核酸、氨基酸、蛋白质和磷脂代谢,并与细胞分化、倍增及其功能密切相关。叶酸需要从外界摄取,经叶酸受体介导,通过内吞作用将叶酸运送到细胞质中。
人体内转运叶酸的受体有三种,叶酸受体(FR)家族就是其中一种。FR家族是通过糖基磷脂酰肌醇(GPI)锚定于细胞膜的单链糖蛋白,能够结合叶酸并通过内吞作用转运叶酸进入细胞。FR有FRα、FRβ、FRγ和FRδ四种亚型,分别由FOLR1、FOLR2、FOLR3和FOLR4编码,家族同源性约为70%。其中,FRα研究最为广泛,在实体瘤中高度表达,如间皮瘤(72-100%)、三阴性乳腺癌(35-68%)、卵巢癌(76-89%)和非小细胞肺癌(14-74%)等,参与肿瘤浸润、转移和发展。
FRα在肿瘤中的作用机制
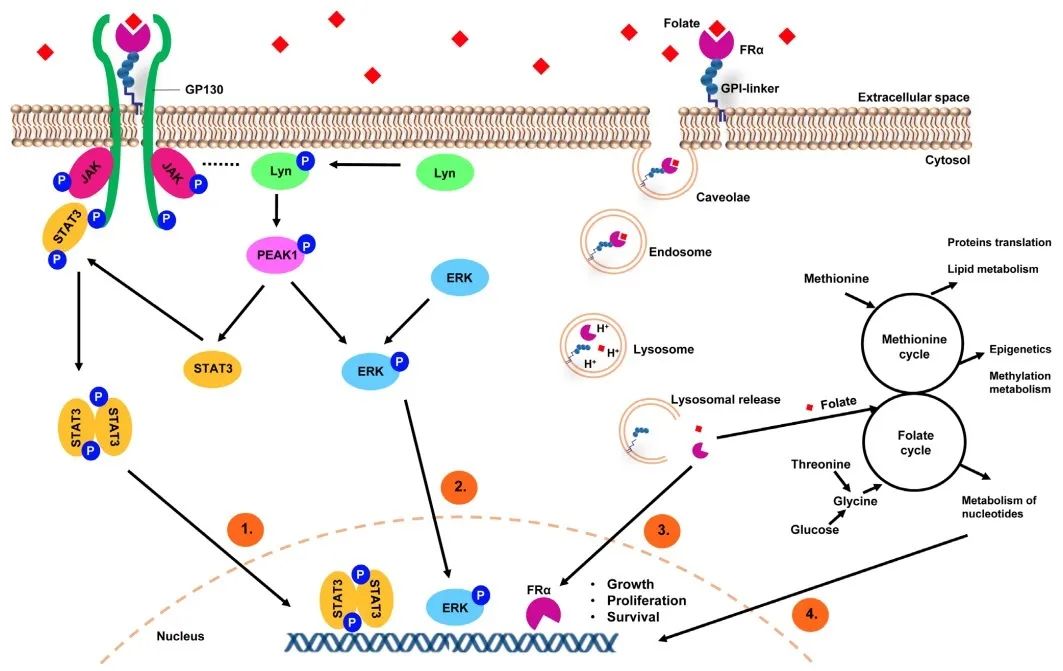
图1 FRα在肿瘤中的作用机制[2]
FRα介导的叶酸内化和癌细胞信号调节机制主要有四种:
1)叶酸与FRα的结合可能通过GP130共受体介导的JAK依赖性过程诱导STAT3的激活;
2)FRα可与LYN酪氨酸激酶形成大分子复合物,调控PEAK1的磷酸化,从而促进ERK和STAT3的激活;
3)GPI锚定的FRα在小窝囊泡中内化,并形成早期内小体,经历酸化并与溶酶体融合,释放FRα和叶酸。FRα随后被转移到细胞核,并直接作为转录因子发挥作用;
4)FRα充当叶酸转运体;在快速增殖的细胞中,需要足够的叶酸摄入以进行一碳代谢反应和DNA合成、修复和甲基化。
靶向FRα的潜在治疗方法
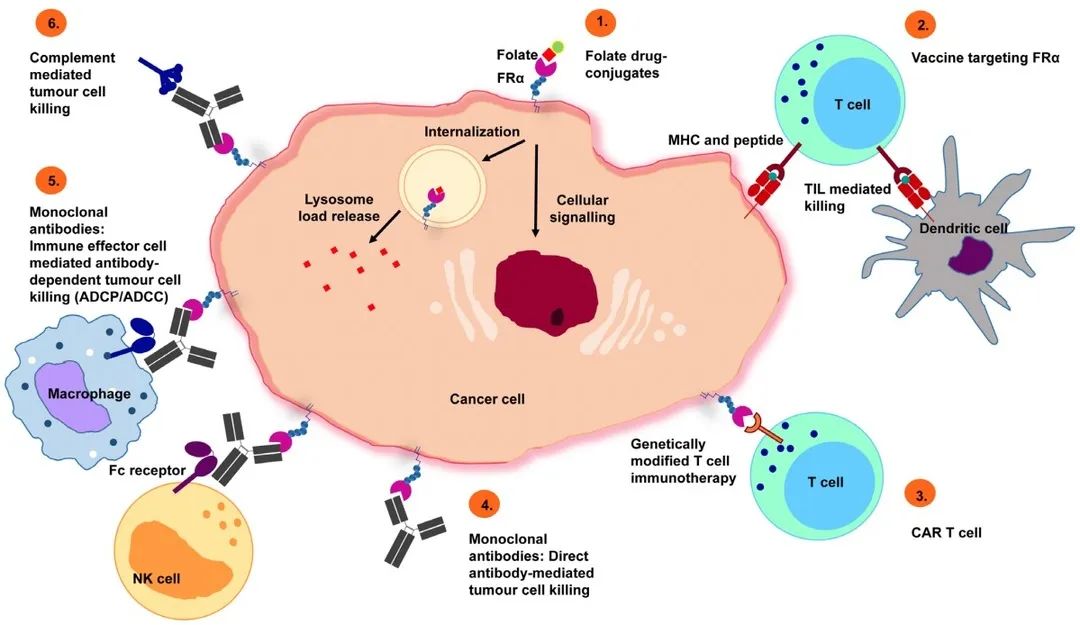
图2 靶向FRα的潜在治疗方法[3]
1) 叶酸偶联药物:小分子,如vintafolide;与叶酸偶联,靶向FRα;
2) 靶向FRα的疫苗:用FRα mRNA工程化的自体树突状细胞通过T细胞介导的抗FRα免疫反应;
3) CAR-T细胞:识别FRα的CAR-T细胞触发肿瘤细胞杀伤;
4) 单克隆抗体(直接作用):特异性识别FRα导致下游信号传导抑制使肿瘤细胞死亡;
5) 单克隆抗体(免疫效应细胞参与):抗体将表达 FRα 的肿瘤细胞与携带 Fc 受体的免疫效应细胞连接起来,通过产生抗体依赖性效应细胞介导的细胞毒性(ADCC)、吞噬作用(ADCP);
6) 补体依赖性细胞毒性(CDC)激活。
FRα药物研究现状
FRα在恶性肿瘤的特异性表达,使之成为一个良好的抗肿瘤药物开发靶点。在研FRα靶向药多为ADC。除此之外,还涉及单抗、小分子、CDC(纳米偶联药物)、PDC(配体偶联药物)、CAR-T、TIL疗法等。适应症主要为卵巢癌,子宫内膜癌,前列腺癌等生殖系统癌症[4]。
表1 靶向FRα的部分在研药物
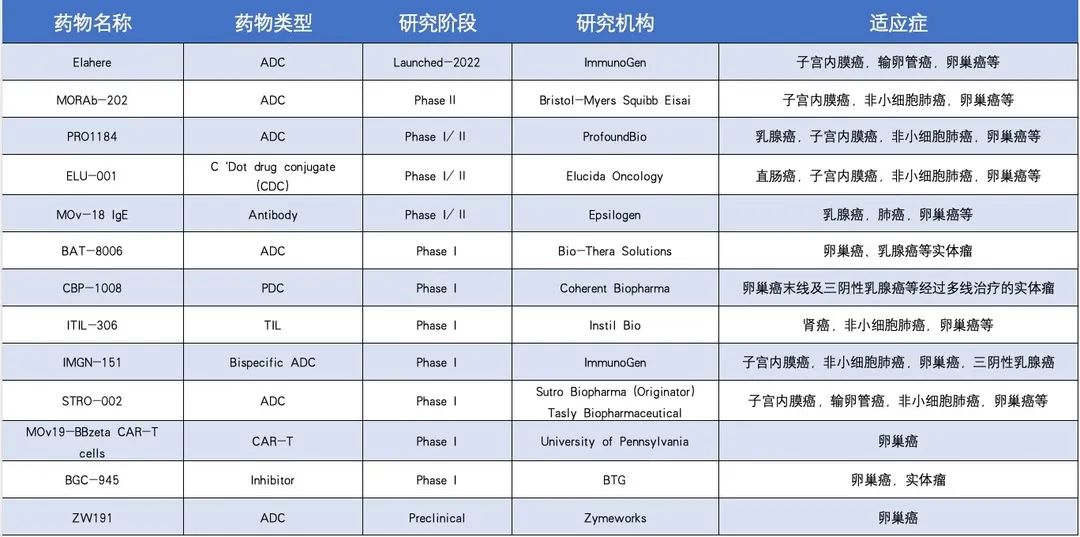
数据参考来源:CDDI数据库
新一代ADC命运的齿轮已经开始加速转动,艾伯维是否能靠FRα ADC成功完成赛道卡位拭目以待。目前全球范围针对FRα研发的企业还相对较少,不过FRα为ADC领域差异化布局提供了新的方向。
百奥动物针对叶酸受体(FR)家族开发了人源化小鼠&细胞模型,以及CDX模型,助力相关药物临床前研究。
针对FR家族的人源化小鼠&细胞模型

用于FOLR1(FRα)相关药物评价的CDX模型
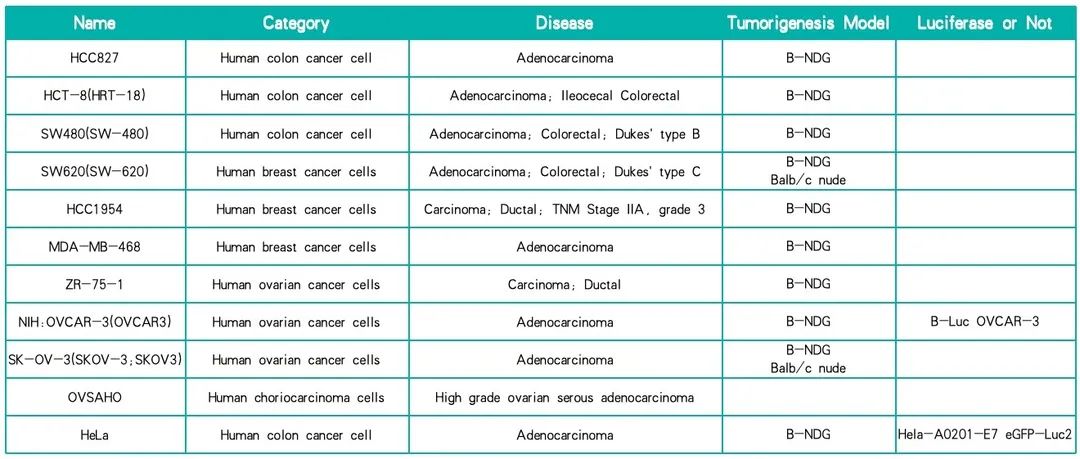
*CDX模型成瘤数据可咨询相关BD
部分数据展示
B-hFOLR1/hFOLR2 小鼠
基本信息

mRNA表达分析
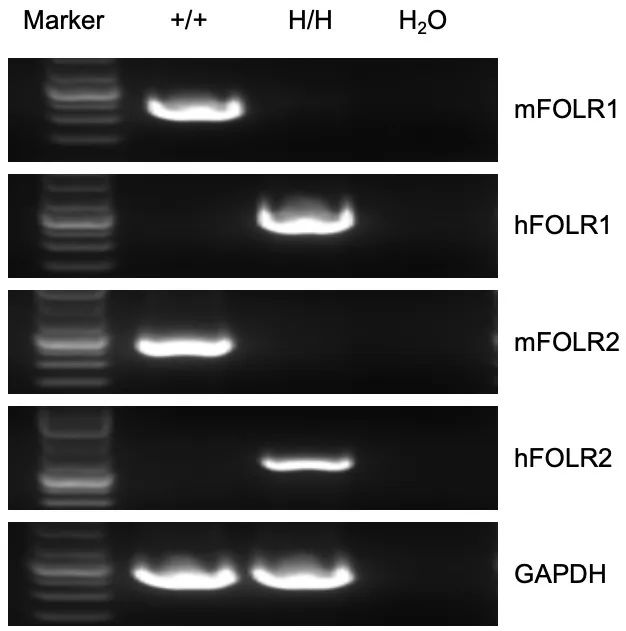
流式细胞术分析野生型小鼠和纯合B-hFOLR1/hFOLR2小鼠中种属特异性FOLR1和FOLR2的表达。野生型(+/+)小鼠脾细胞中检测到鼠Folr1 和Folr2 mRNA。人FOLR1和FOLR2 mRNA仅在纯合B-hFOLR1/hFOLR2小鼠中检测到,而在野生型(+/+)小鼠中检测不到。
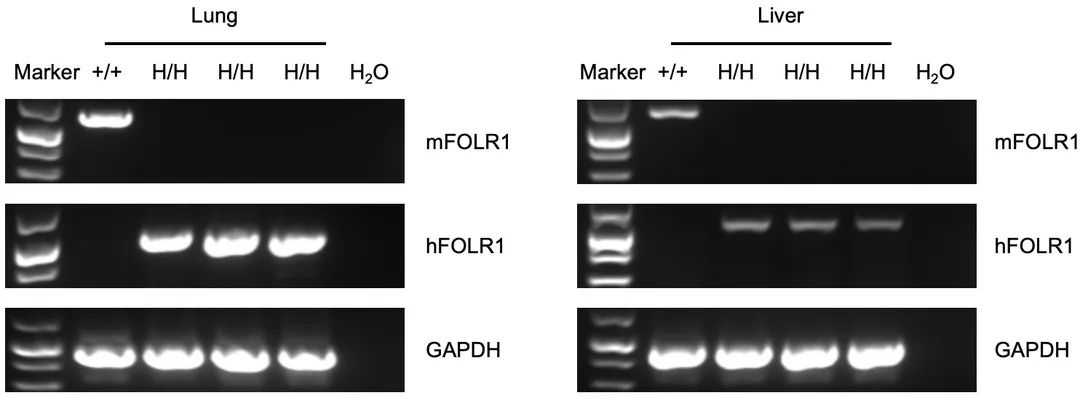
流式细胞术分析野生型小鼠和纯合B-hFOLR1/hFOLR2小鼠中种属特异性FOLR1表达。野生型(+/+)小鼠脾细胞中检测到鼠Folr1 mRNA。人FOLR1 mRNA仅在纯合B-hFOLR1/hFOLR2小鼠的肺和肝脏中检测到,而在野生型(+/+)小鼠中检测不到。
蛋白表达分析
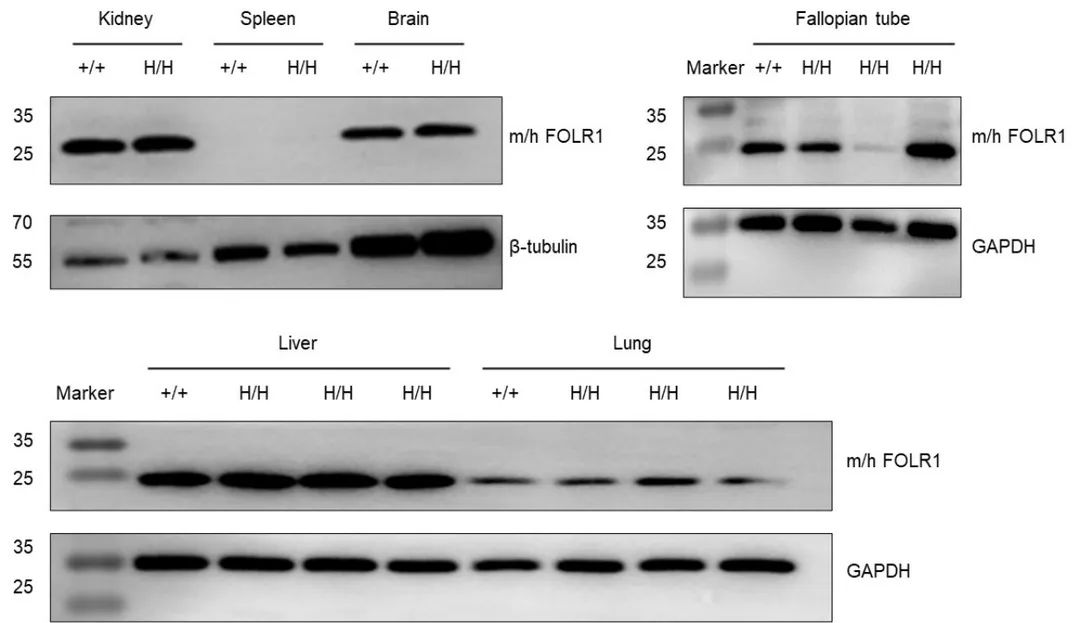
Western blot分析野生型小鼠和纯合B-hFOLR1/hFOLR2小鼠中种属特异性FOLR1的表达。用抗FOLR1抗体检测野生鼠和纯合B-hFOLR1/hFOLR2小鼠的肾脏、脾脏、脑、肝脏、肺脏和输卵管,结果表明,可以在肾脏、脑、肝脏、肺脏和输卵管中检测到表达,但在脾脏中未检测到表达。注:该抗体人鼠交叉识别。
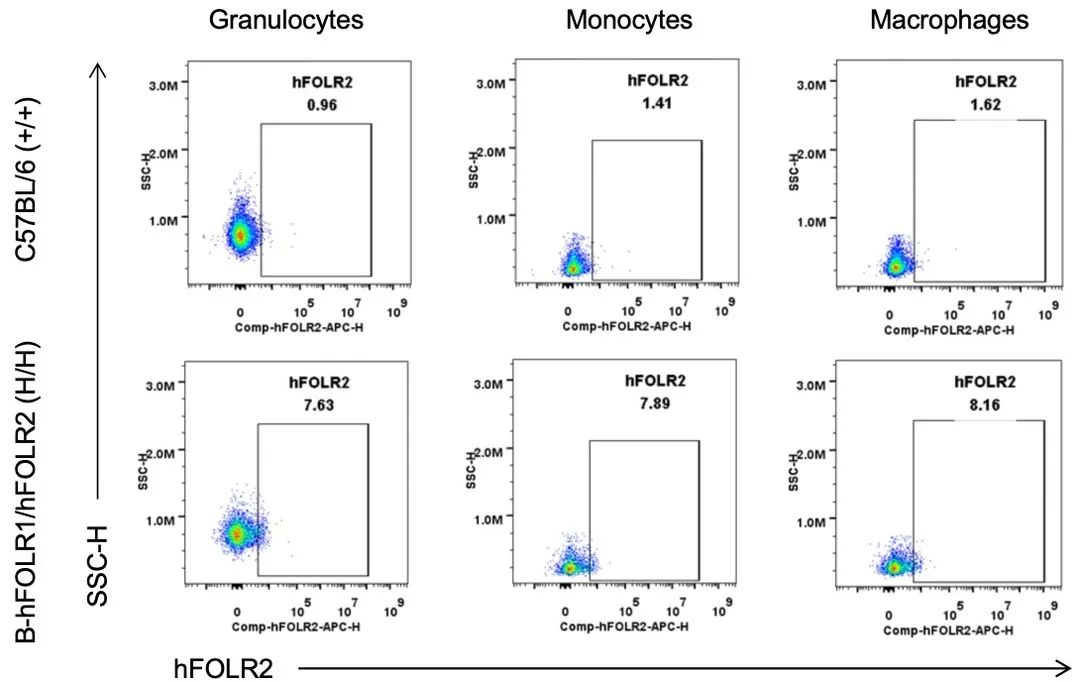
流式细胞术分析野生型小鼠和纯合B-hFOLR1/hFOLR2小鼠中种属特异性FOLR2的表达。采集C57BL/6小鼠(+/+)和纯合B-hFOLR1/hFOLR2小鼠(H/H)的血液,用抗FOLR2抗体进行流式细胞术分析。人FOLR2仅在纯合B-hFOLR1/hFOLR2小鼠的粒细胞、单核细胞和巨噬细胞中检测到,而在野生型小鼠中检测不到。
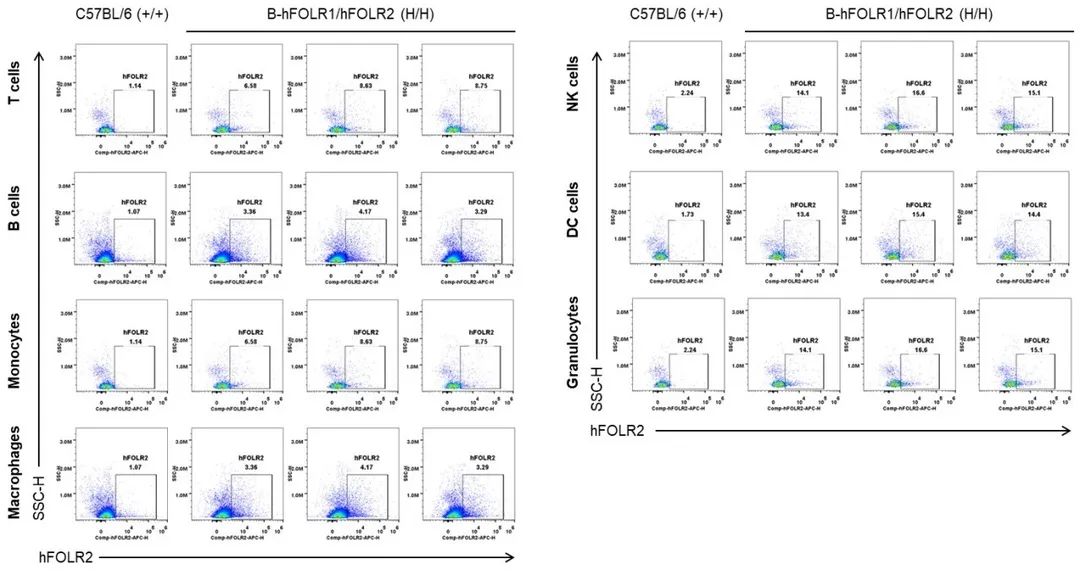
流式细胞术分析野生型小鼠和纯合B-hFOLR1/hFOLR2小鼠中种属特异性FOLR2的表达。取C57BL/6小鼠(+/+)和纯合B-hFOLR1/hFOLR2小鼠(H/H)骨髓,用抗FOLR2抗体进行流式细胞术分析。人FOLR2仅在纯合B-hFOLR1/hFOLR2小鼠的T、B、NK、DC、单核细胞、巨噬细胞和粒细胞中检测到表达,而在野生型小鼠中未检测到。
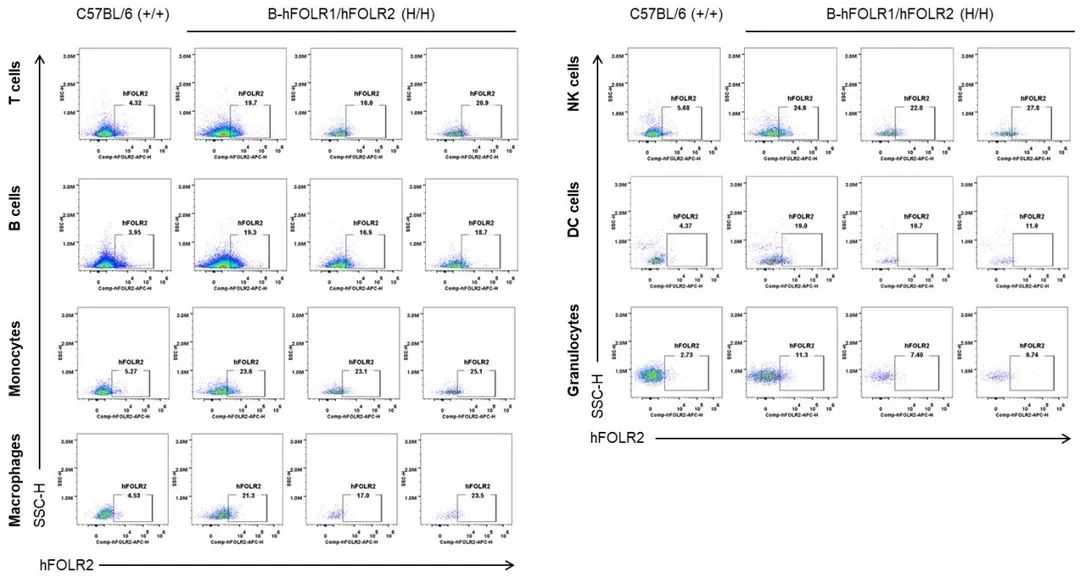
流式细胞术分析野生型小鼠和纯合B-hFOLR1/hFOLR2小鼠中种属特异性FOLR2的表达。采集C57BL/6小鼠(+/+)和纯合B-hFOLR1/hFOLR2小鼠(H/H)的血细胞,用抗FOLR2抗体进行流式细胞术分析。人FOLR2仅在纯合B-hFOLR1/hFOLR2小鼠的T、B、NK、DC、单核细胞、巨噬细胞和粒细胞中检测到表达,而在野生型小鼠中未检测到。
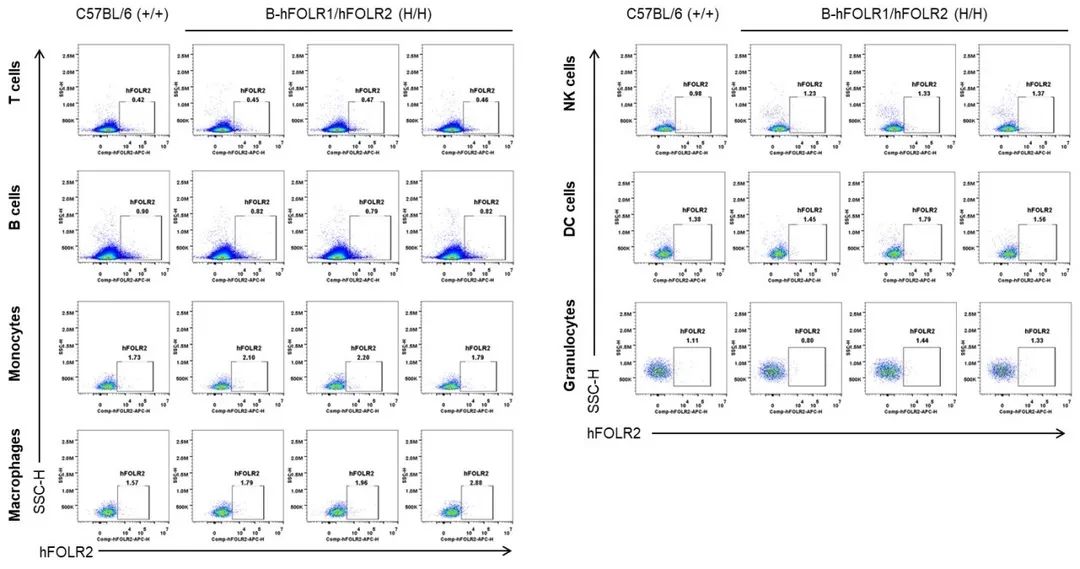
流式细胞术分析野生型小鼠和纯合B-hFOLR1/hFOLR2小鼠中种属特异性FOLR2的表达。取C57BL/6小鼠(+/+)和纯合B-hFOLR1/hFOLR2小鼠(H/H)的脾脏,用抗FOLR2抗体进行流式细胞术分析。人FOLR2仅在纯合B-hFOLR1/hFOLR2小鼠的T、B、NK、DC、单核细胞、巨噬细胞和粒细胞中检测到表达,而在野生型小鼠中未检测到。
免疫分型
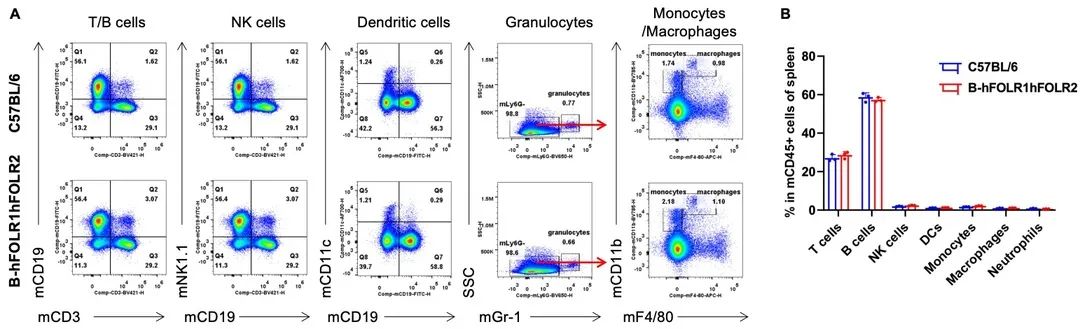
脾脏白细胞亚群的流式细胞术分析。从雌性C57BL/6和纯合B-hFOLR1/hFOLR2小鼠(n= 3,8周龄)中分离脾细胞。用流式细胞术分析脾细胞以评估白细胞亚群。纯合B-hFOLR1/hFOLR2小鼠的T细胞、B细胞、NK细胞、树突状细胞、粒细胞、单核细胞和巨噬细胞的百分比与C57BL/6小鼠相似,表明人源化FOLR1/FOLR2并不会改变脾脏中这些类型细胞的整体发育、分化或分布。
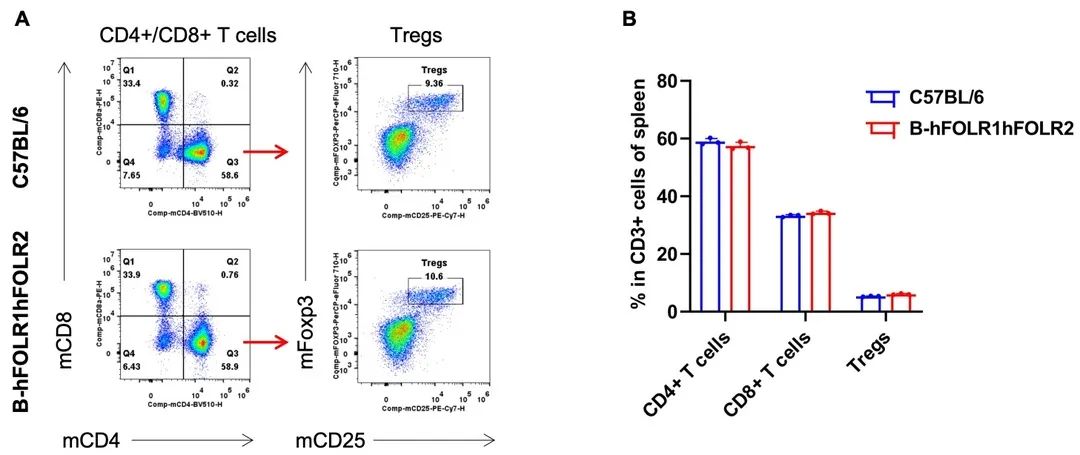
脾脏T细胞亚群的流式细胞术分析。从雌性C57BL/6和纯合B-hFOLR1/hFOLR2小鼠(n= 3,8周龄)中分离脾细胞。用流式细胞术分析脾细胞以评估T细胞亚群。纯合B-hFOLR1/hFOLR2小鼠中CD8+ T细胞、CD4+ T细胞和Treg细胞的百分比与C57BL/6小鼠相似,表明人源化FOLR1/FOLR2并不会改变脾脏中这些T细胞亚群的整体发育、分化或分布。数值以平均值±SEM表示。
实验结果表明人源化FOLR1/FOLR2同样也不影响淋巴结、血液中白细胞亚群和T细胞亚群总体的发育、分化和分布。(数据未展示)
B-hFOLR4 小鼠
基本信息

mRNA和蛋白表达分析
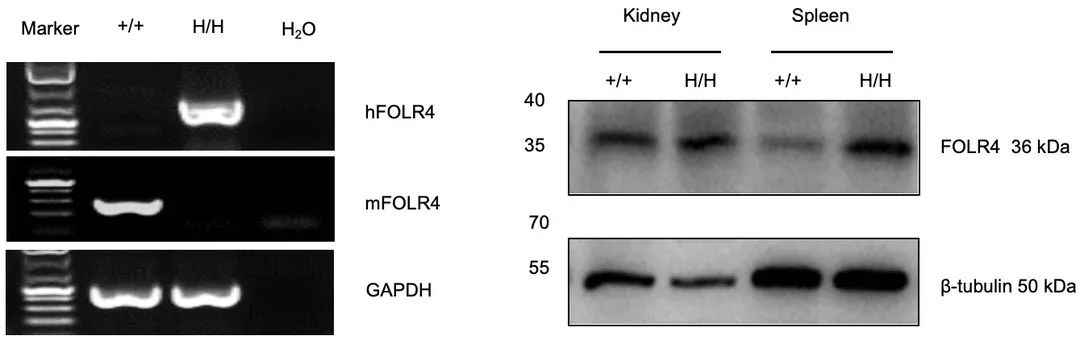
RT-PCR分析野生型小鼠和B-hFOLR4小鼠中FOLR4基因表达的种属特异性。野生型小鼠脾细胞中检测到鼠Folr4 mRNA(+/+)。人FOLR4 mRNA仅在纯合B-hFOLR4小鼠(H/H)中检测到,而在野生型小鼠中检测不到。
Western blot分析纯合B-hFOLR4小鼠种属特异性FOLR4表达。取野生型C57BL/6小鼠(+/+)和纯合B-hFOLR4小鼠(H/H)的脾组织和肾组织,用抗FOLR4抗体进行western blot分析。在野生型小鼠和纯合B-hFOLR4小鼠中检测到人FOLR4。注:该抗体人鼠交叉识别。
B-hFOLR1 MC38 细胞
基本信息
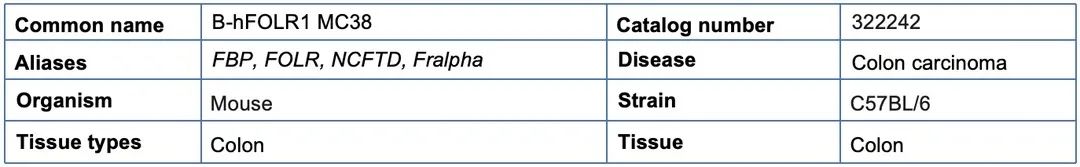
蛋白表达分析
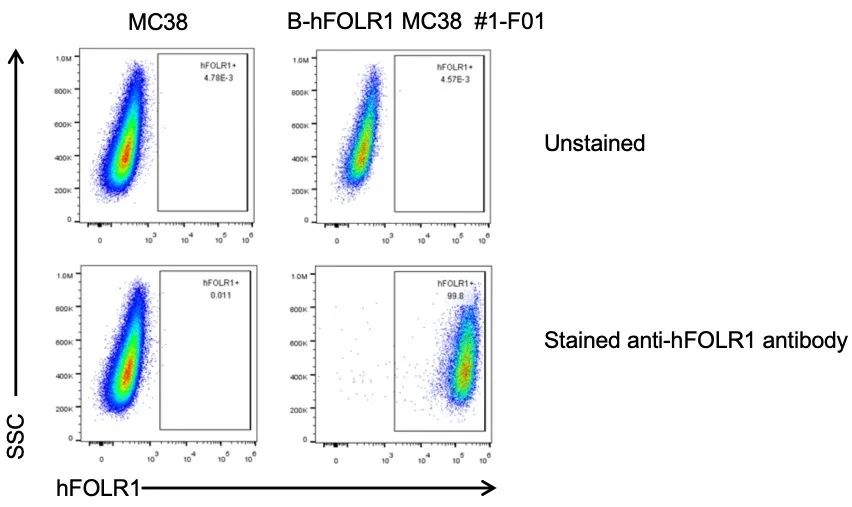
流式细胞术分析B-hFOLR1 MC38细胞中FOLR1的表达。野生型MC38和B-hFOLR1 MC38培养的单细胞悬液用种属特异性抗FOLR1 抗体染色。B-hFOLR1 MC38细胞表面检测到人FOLR1,野生型MC38细胞表面未检测到人FOLR1。采用B-hFOLR1 MC38细胞的1-F01克隆进行体内实验。
肿瘤生长曲线及体重变化
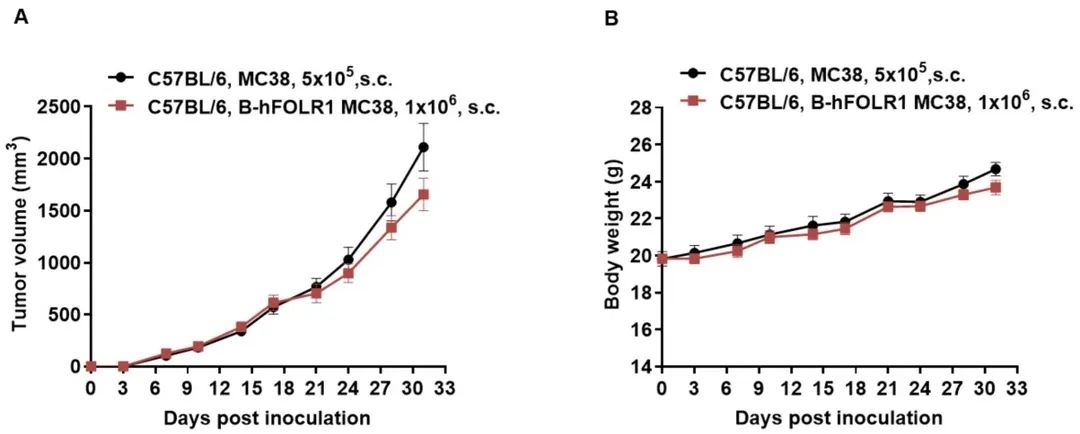
B-hFOLR1 MC38细胞皮下同种移植物肿瘤的生长。将B-hFOLR1 MC38细胞(1x106)和野生型MC38细胞(5x105)皮下植入C57BL/6小鼠(雌性,8周龄,n=6)。每周测量两次肿瘤体积和体重。(A)平均肿瘤体积±SEM。(B)体重(平均值±SEM)。体积以mm3表示,公式为:V=0.5 × 长径 × 短径2。如A图所示,B-hFOLR1 MC38细胞能够在体内形成肿瘤,可以用于药效研究。
单只小鼠肿瘤生长曲线
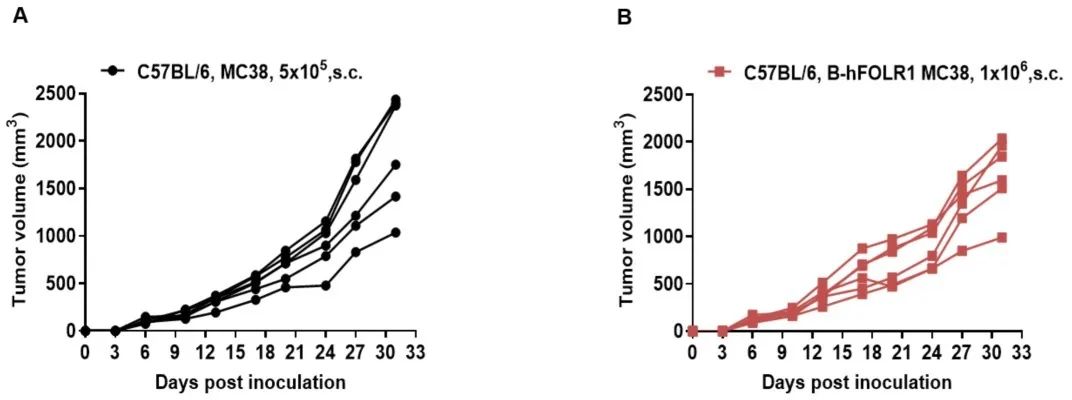
B-hFOLR1 MC38肿瘤细胞的生长。将B-hFOLR1 MC38细胞(1x106)和野生型MC38细胞(5x105)皮下植入C57BL/6小鼠(雌性,8周龄,n=6)。如图所示,B-hFOLR1 MC38细胞能够在体内形成肿瘤,可以用于药效研究。
肿瘤细胞蛋白表达分析
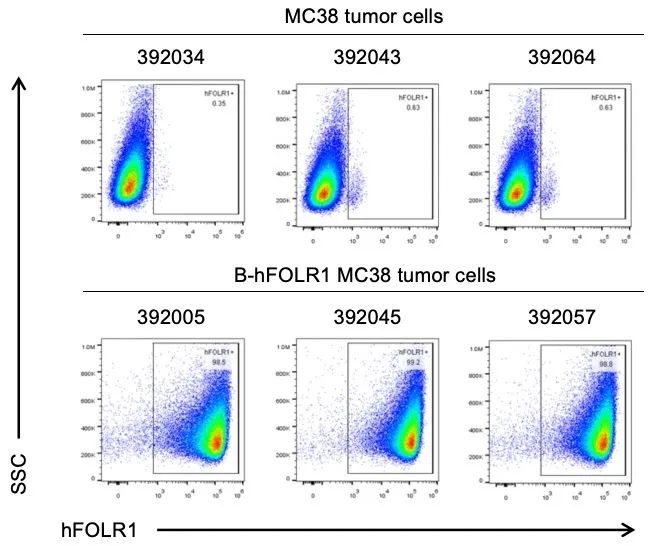
将B-hFOLR1 MC38细胞皮下移植到C57BL/6小鼠(n=6)体内,接种后31天采集肿瘤细胞,流式细胞术检测人FOLR1的表达。如图所示,人FOLR1在肿瘤细胞表面高表达。因此,B-hFOLR1 MC38细胞可用于新型FOLR1疗法的体内药效研究。
参考资料:
[1] https://mp.weixin.qq.com/s/Z_pQKOJJdu6dSff6TckYGg
[2] Cheung Anthony,Bax Heather J,Josephs Debra H et al. Targeting folate receptor alpha for cancer treatment.[J] .Oncotarget, 2016, 7: 52553-52574.
[3] Anthony,Cheung,Heather,et al.Targeting folate receptor alpha for cancer treatment[J].Oncotarget, 2016.DOI:10.18632/oncotarget.9651.
[4] https://mp.weixin.qq.com/s/vqIOi6dVcL9D10k3UJI48g






 010-56967680
010-56967680 info@bbctg.com.cn
info@bbctg.com.cn 苏公网安备:32068402320845号
苏公网安备:32068402320845号