靶点介绍
“尿激酶型纤溶酶原激活剂”或简称“尿激酶”(uPA) 是一种关键的丝氨酸蛋白酶,在人体中发挥多种作用,主要涉及细胞增殖、迁移和侵袭,以及纤溶酶原激活的调节。1947 年,MacFarlane 和 Pilling 首次在尿液中发现了它,他们报告了一种新型“未命名”蛋白质的纤溶活性[1]。五年后,索贝尔和同事将这种“未命名”的蛋白质命名为“尿激酶”[2]。进一步的研究报道了血浆、精液和许多组织的 ECM 中存在尿激酶。
uPA(尿激酶型纤溶酶原激活物)是一种蛋白水解酶,能够促进纤溶过程。它的主要功能是促进纤溶酶原(plasminogen)的转化成纤溶酶(plasmin),纤溶酶负责降解纤维蛋白,溶解血栓和组织纤维。除了在纤溶系统中的作用外,uPA也与细胞迁移、侵袭和肿瘤的生长扩散相关。
uPAR是uPA的受体,在细胞膜表面上存在。它与uPA结合,形成复合物,促进了uPA在细胞表面的活性,从而调节细胞迁移、侵袭和融合。uPAR也与细胞黏附、信号转导以及炎症等生物学过程相关。
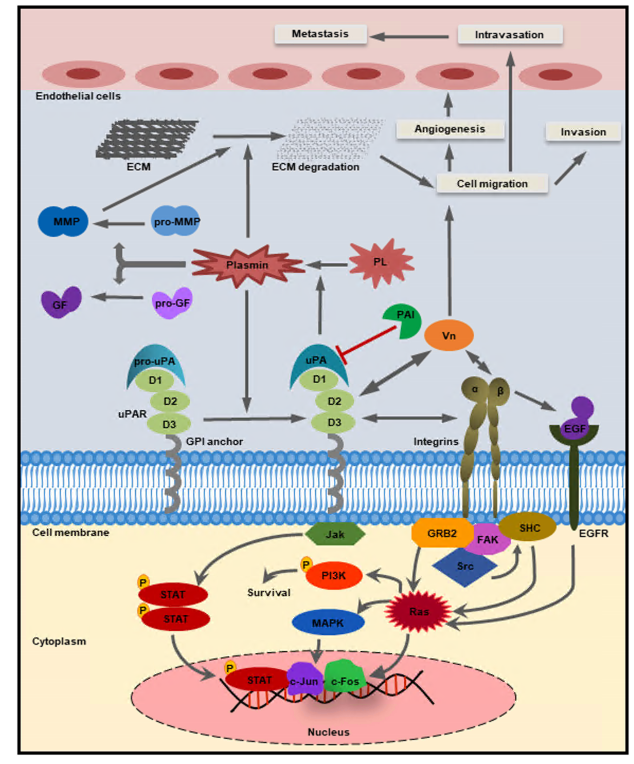
uPA-尿激酶型纤溶酶原激活物受体(uPAR)介导途径示意图[3]
uPAR 在肿瘤组织中的表达升高,而在周围正常组织中却没有升高,这使其成为一个有吸引力的治疗靶点[4]。最近的证据表明,uPAR 激活的信号通路有助于癌细胞逃避和降低抗癌药物的细胞毒性作用[5]。编码 uPAR(PLAUR)的基因在癌症中的表达升高可能受到不同机制的调控。转录因子,如 Sp1、NF-κB、TCF 和缺氧诱导因子 1α,经常被不同类型的癌症相关信号通路激活,它们与 PLAUR 基因上游的顺式作用元件结合,触发其在癌症中的高表达。
研究进展
针对uPA和uPAR的研究和药物开发正在进行,试图利用对这些靶点的干预来调节细胞行为,尤其是在癌症治疗方面有潜在的重要性。目前针对该靶点进行开发的药物有344个,其中处于临床Ⅱ/Ⅲ期的1项,临床Ⅱ期的4项,临床前90项。
uPA抑制剂目前有领晟医疗引进的德国Wilex公司开发的WX-671,目前处于临床Ⅱ/Ⅲ期,已联合盐酸吉西他滨用于局部晚期/转移性胰腺癌患者。目前进行的临床试验证明WX-671可以明显提高吉西他滨单药治疗胰腺癌的有效率,显著延长患者的无进展生存期,且具有非常好的耐受性和安全性。有望成为全球首款以uPA为靶点的抗胰腺癌药物。
2022年由兰州大学第二医院焦作义、杨靖及兰州华帜天成公司王琦共同在SCIENCE ADVANCES期刊发表重要研究成果,确定了靶向尿激酶型纤溶酶原激活物受体(uPAR)在弥漫型胃癌中特异性过表达,并开发了新的免疫联合治疗策略。该研究利用细胞系衍生异种移植和DGC患者衍生异种移植小鼠模型表明,抗uPAR和抗程序性细胞死亡蛋白1(PD-1)联合使用可通过多种机制显著抑制肿瘤生长并延长存活时间。此外,基于新型抗uPAR的表达uPAR嵌合抗原受体的T细胞能有效杀死DGC患者衍生的器官组织,与PD-1阻断疗法相结合时,在已建立的小鼠模型中表现出生存优势。[6]

数据来源于科睿唯安
百奥动物利用基因编辑技术自主开发了uPA/uPAR相关产品鼠,助力临床前药物/该基因功能研究。

模型示例
B-hUPA/hUPAR mice
蛋白表达分析
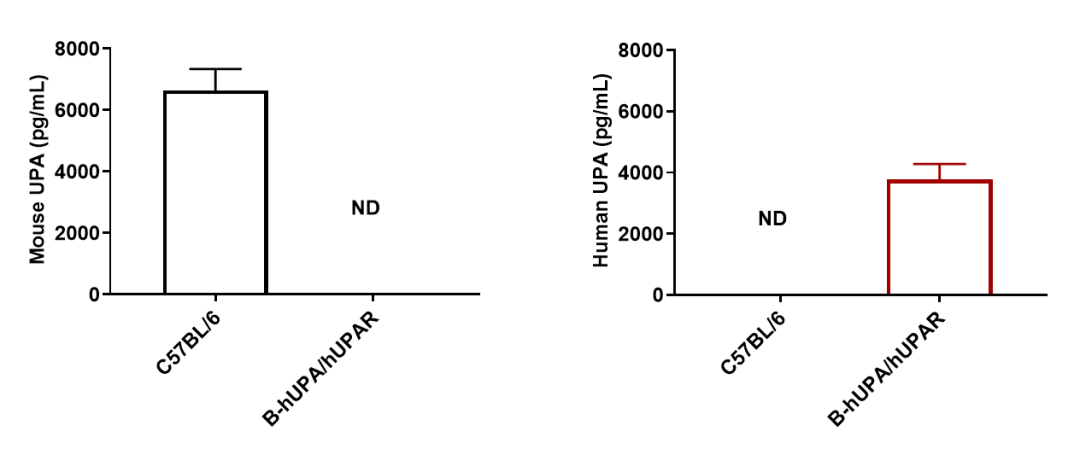
通过ELISA分析纯合子B-hUPA/hUPAR小鼠的种属特异性UPA表达。收集野生型C57BL/6小鼠和纯合B-hUPA/hUPAR小鼠(雄性,9周龄,n=3)血清,采用种属特异性UPA ELISA试剂盒进行酶联免疫吸附试验(ELISA)分析。野生型C57BL/6小鼠体内可检测到小鼠UPA。人UPA只在纯合B-hUPA/hUPAR小鼠中检出,而在野生型小鼠中未检出。
蛋白表达分析

通过流式细胞术分析种属特异性uPAR(也称为PLAUR)在纯合B-hUPA/hUPAR小鼠中的表达。收集野生型C57BL/6小鼠和纯合B-hUPA/hUPAR小鼠骨髓,用种属特异性抗uPAR抗体进行流式细胞术分析。小鼠uPAR仅在野生型小鼠树突状细胞中检测到。人uPAR仅在纯合B-hUPA/hUPAR小鼠的单核/巨噬细胞、粒细胞和树突状细胞中检测到,在野生型小鼠中检测不到。
参考文献
1. MacFarlane R, Pilling J. Fibrinolytic activity of normal urine. Nature (1947) 159(4049):779. 10.1038/159779a0
2. Sobel G, Mohler S, Jones N, Dowdy A, Guest M, editors. Urokinase-an activator of plasma profibrinolysin extracted from urine. Am J Physiol (1952) 171(3):768–9.
3. Mahmood N, et al. Front Oncol. 2018 Feb 12;8:24.
4. Mazar AP. Urokinase plasminogen activator receptor choreographs multiple ligand interactions: implications for tumor progression and therapy. Clin Cancer Res (2008) 14(18):5649–55. 10.1158/1078-0432.CCR-07-4863
5. Gonias SL, Hu J. Urokinase receptor and resistance to targeted anticancer agents. Front Pharmacol (2015) 6:1–6. 10.3389/fphar.2015.00154
6. Long Qin, Long Wang, et al. Therapeutic strategies targeting uPAR potentiate anti–PD-1 efficacy in diffuse-type gastric cancer.Sci. Adv. 8, eabn3774 (2022).






 010-56967680
010-56967680 info@bbctg.com.cn
info@bbctg.com.cn 苏公网安备:32068402320845号
苏公网安备:32068402320845号