肿瘤治疗药物是全球最大和增长最快的药物细分市场,近年来,疫苗开发也已经成为癌症这一重大疾病新治疗选择的一个热门研究方向。相比全球疫苗市场,全球肿瘤疫苗市场规模增长更快,2019年为46亿美元,预计到2024年将达到101亿美元,复合年增长率为17.28%。
01、肿瘤疫苗简介
疫苗是指含有抗原、能够诱导人体产生特异性主动免疫的制剂,它可以保护机体免受感染源、毒素,以及感染源引起的抗原性物质的损伤。肿瘤疫苗作为肿瘤治疗的新方向,已成为当今肿瘤研究的热点话题。
肿瘤疫苗(又称癌症疫苗)通常是含有肿瘤特异性抗原(TSA)或肿瘤相关抗原(TAA)的肿瘤细胞或碎片或片段,可分为肿瘤预防性疫苗(如HPV疫苗)和肿瘤治疗性疫苗(如新抗原mRNA疫苗),主要由肿瘤抗原、制剂、免疫佐剂和递送载体4个关键成分组成。进入人体后,癌症疫苗可激活患者自身免疫系统,诱发特异性免疫反应,克服免疫抑制状态,提高对特定肿瘤的抵抗,是一种主动免疫治疗方法。对于已经发生癌症的患者来说,治疗性疫苗或可延长他们的生存期,成为救命稻草。肿瘤疫苗作为一种新兴的治疗手段,究竟“优秀”在何处呢?
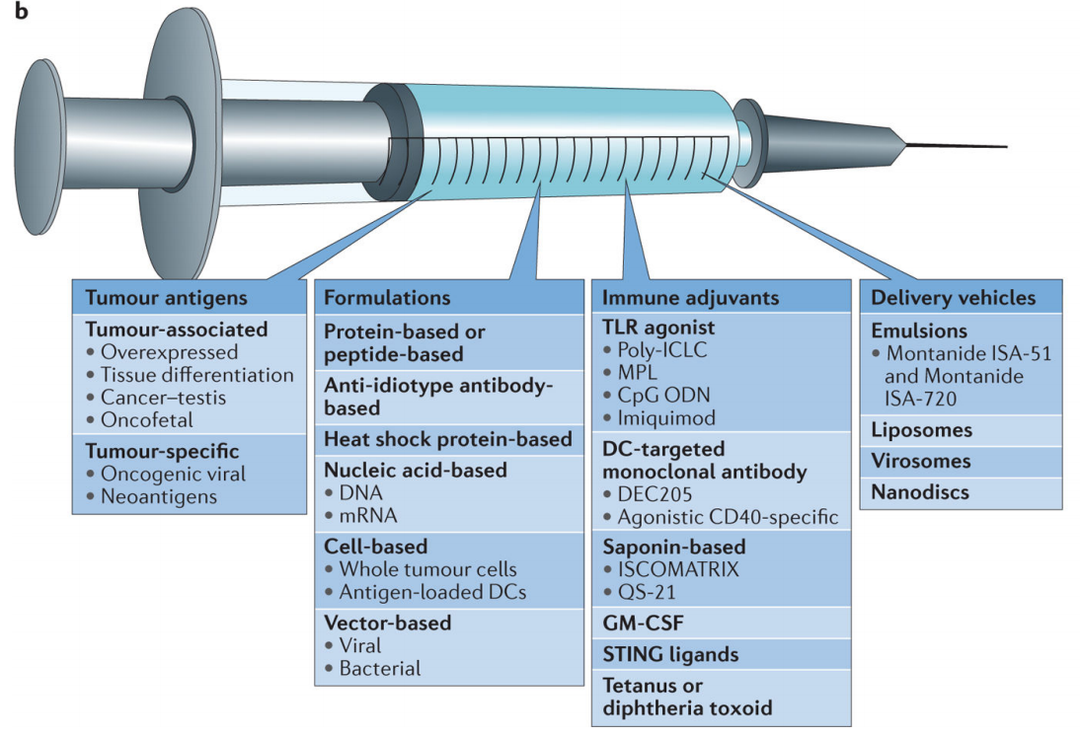
肿瘤疫苗组成因素[1]
首先,治疗性肿瘤疫苗可通过主动免疫方式诱导全身性的特异性抗瘤效应,与手术治疗、放射治疗相比,作用范围更广泛,特别适用于多发病灶性肿瘤、广泛转移性瘤或非实体性肿瘤(如白血病);其次,肿瘤疫苗可调动机体自身的力量达到抗肿瘤作用,与放射治疗、化学药物治疗相比不良反应小、特异性高。尽管各种治疗性肿瘤疫苗的设计思想各不相同,诱导免疫应答的方式不同,抗瘤效应各有特点,但不论采用何种方法制备,都是围绕如何提高肿瘤抗原的免疫原性以及如何打破肿瘤免疫耐受这一最关键的核心问题展开的。一种理想的肿瘤疫苗不但能够诱导主动性免疫,刺激荷瘤宿主产生有效的免疫应答,同时还应当是安全的和无不良反应的;不仅能特异性地消除扩散的肿瘤细胞,而且更为重要的是,还能提供保护性的预防肿瘤复发的长期免疫记忆功能。
02、肿瘤疫苗是如何发挥作用的?
肿瘤疫苗通过利用肿瘤细胞相关抗原,来唤醒人体针对癌症的免疫系统功能。目标是预防和治疗癌症,或防止癌症的复发。而肿瘤疫苗想在人体中发挥作用,离不开人类MHC(即HLA复合体)的抗原呈递过程。肿瘤疫苗的作用过程为:通过皮下/肌肉注射使抗原进入机体内,被DC细胞摄取。DC细胞通过淋巴管的归巢进入淋巴结,在淋巴结中存在有大量初始T细胞。通过与APC细胞表面的MHC I/II 类分子结合,初始T细胞被激活为CD8或CD4阳性T细胞。激活的T细胞通过血液循环进入肿瘤部位,从而实现对肿瘤细胞的杀伤。
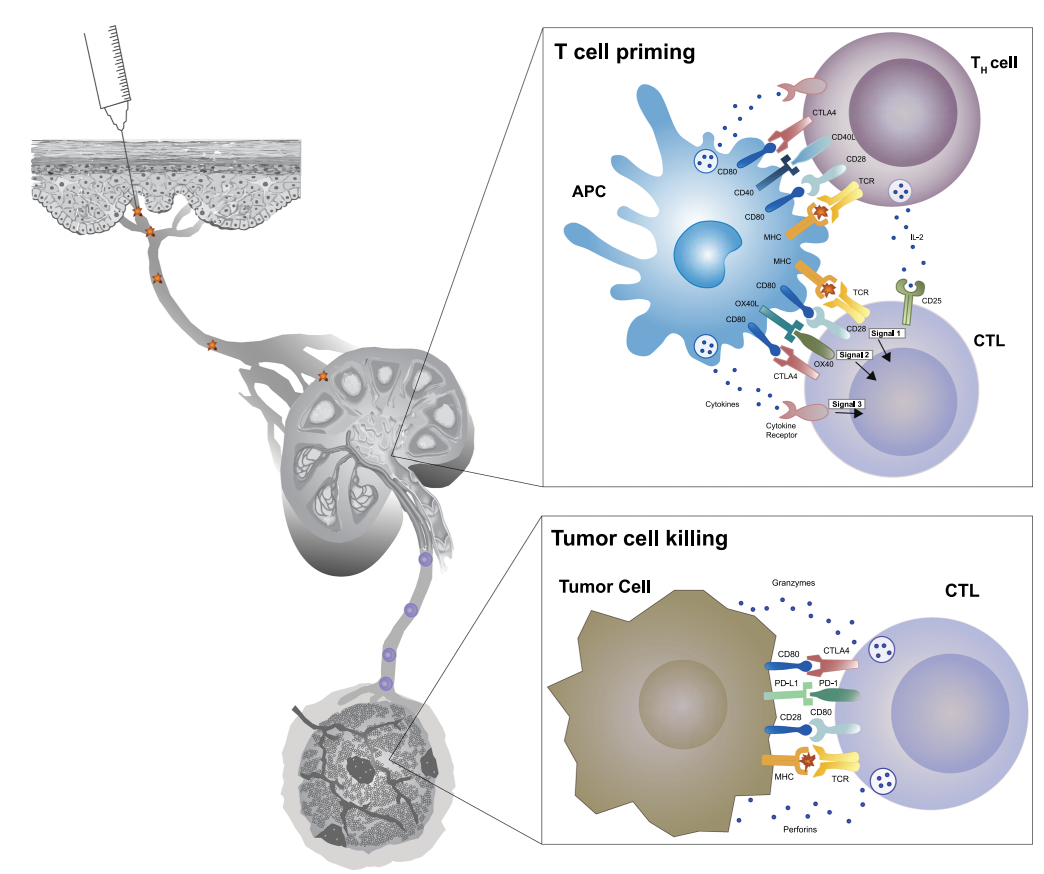
T细胞激活与肿瘤细胞杀伤机制[2]
03、百奥赛图可提供肿瘤疫苗相关临床前安全性及药效评价
在进行临床试验之前,疫苗与治疗性药物一样,也需要进行临床前动物安全性评价。
临床前动物安全性评价的主要目的是通过相关动物来考察疫苗的安全性,包括对免疫器官和其他毒性靶器官的影响、毒性的可逆性,以及与临床相关的参数,预测其在大规模人群中使用时可能出现的不良反应,降低临床试验受试者和临床使用者承担的风险,并为临床试验方案的制定提供依据。
百奥赛图具有完善的临床前药效评价平台,能够从小鼠免疫,肿瘤药效,免疫原性评估提供肿瘤疫苗临床前评价一站式服务,评估抗肿瘤免疫反应。
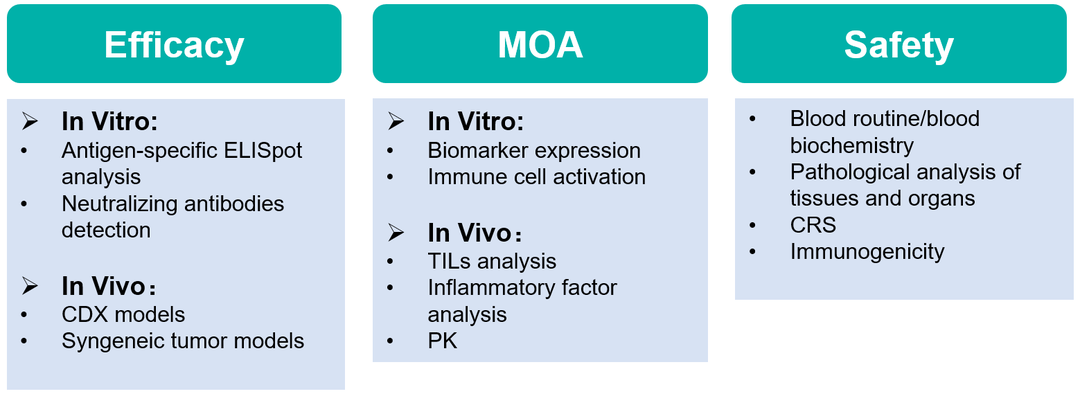
百奥赛图服务能力概览
肿瘤药效
稳定的肿瘤模型减小对试验设计和疫苗评价的影响,治疗给药与rechallenge实验检测疫苗有效性。
细胞免疫
1. 可采用ICS、ELISA、Luminex、MSD等方法检测细胞因子。

2. ELISPOT检测T细胞免疫反应
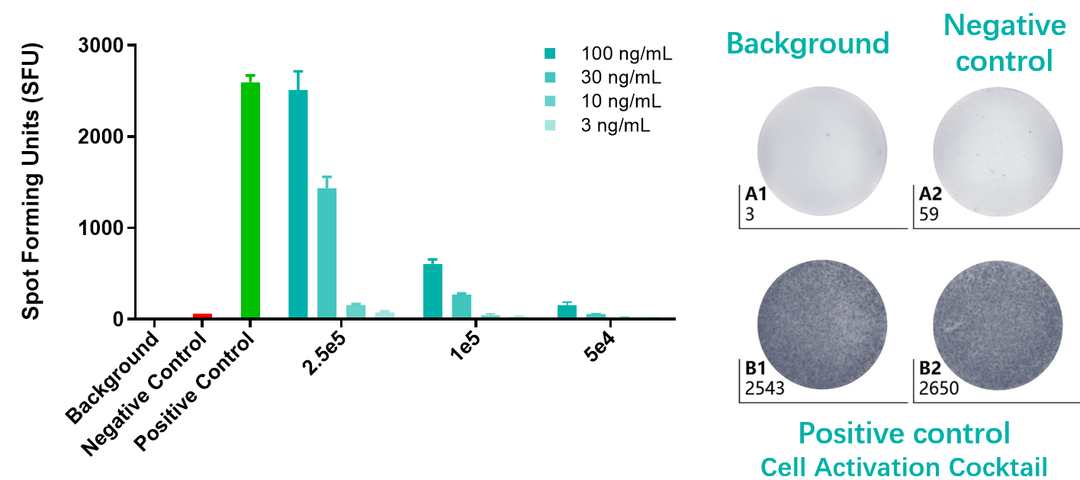
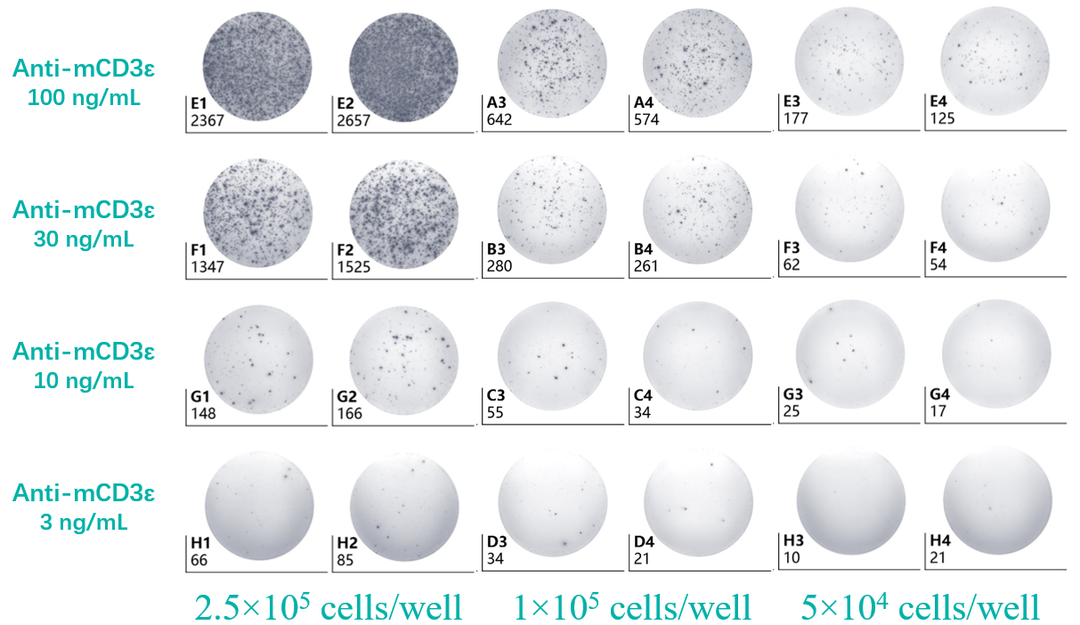
Positive Control:加入工作浓度的阳性刺激物;
Negative Control:细胞浓度跟实验孔保持一致,不加阳性刺激物;
Background:加入不含细胞的培养基,不加阳性刺激物。
3. 可用FACS方法检测T/B/NK细胞以及各T细胞亚群比例
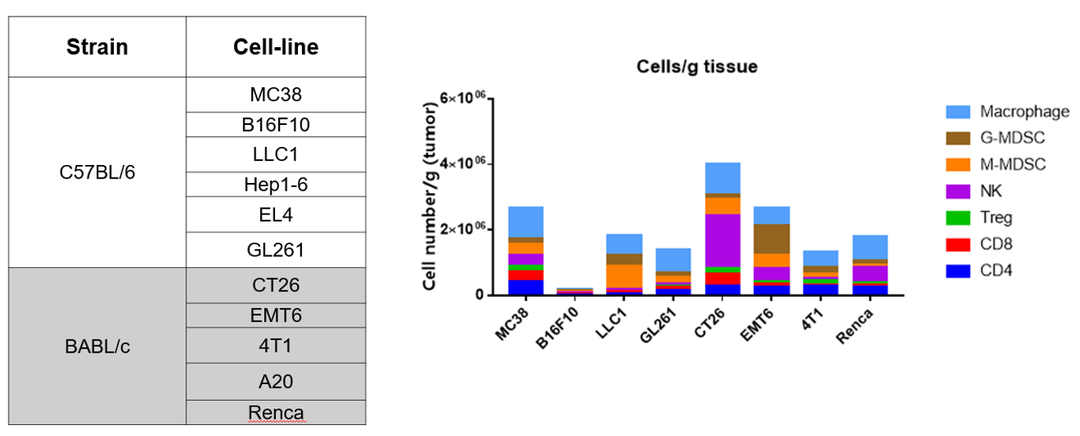
小鼠肿瘤模型TILS检测与细胞分型生物标记物
免疫细胞及小鼠体内标记物

4. 此外,我们还能提供体外T细胞杀伤、四聚体检测等服务。
体液免疫
百奥赛图能够定制化进行肿瘤特异性抗体检测的ELISA方法开发和方法学验证。
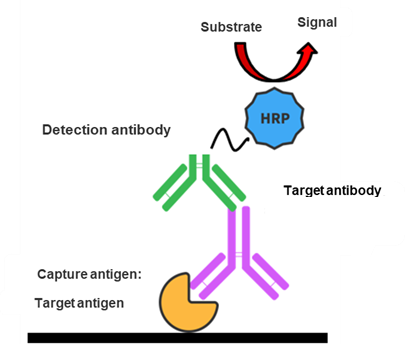
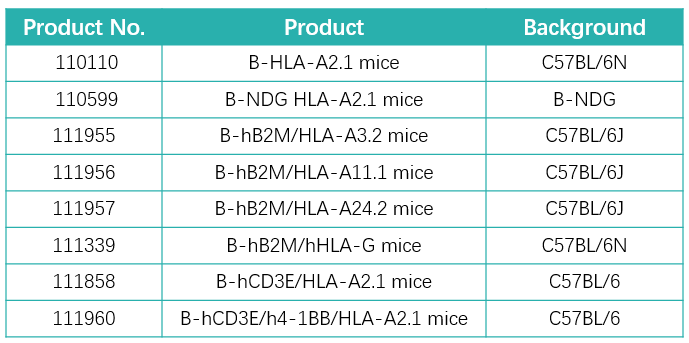
04、百奥赛图上市多款HLA人源化小鼠
我们使用HLA人源化小鼠细胞能呈递和识别与人类呈递的表位相似或相同的肽表位。
百奥赛图已上市多款HLA人源化小鼠,可助力疫苗领域的研发。下面以B-HLA-A2.1 mice的数据为例:
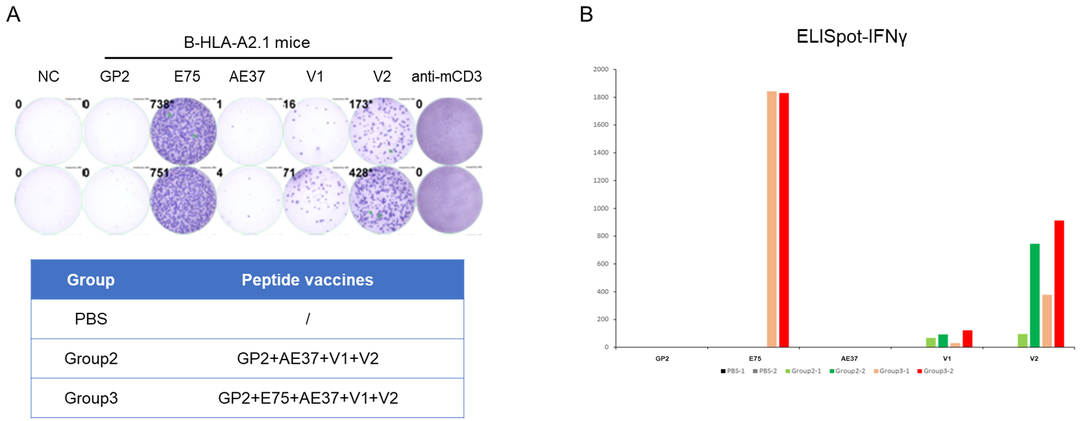
IFN-γ ELISA实验检测B-HLA-A2.1小鼠疫苗诱导的免疫应答。
将9-10周龄雌性 B-HLA-A2.1小鼠分为 PBS 组,Group2和Group 3 (n=2)共三组 ,在小鼠双腿内侧肌肉接种 PBS 或疫苗。最后一次免疫三周后处死小鼠。取小鼠脾细胞,用单肽或与靶标无关的多肽作为阴性对照(NC)或anti-mCD3作为阳性对照刺激,然后测定 IFN-γ 的分泌量。各组间体重无显著差异(数据未显示)。(A) 显示用阴性对照、肽疫苗或阳性对照刺激后的免疫小鼠脾细胞。(B) IFN-γ分泌量。结果表明,B-HLA-2.1小鼠为疫苗的体内评价提供了一个强有力的临床前模型。
其他相关品系详细信息,可访问百奥动物官网查询或咨询BD。
参考资料:
[1] Hu Z, Ott PA, Wu CJ. Towards personalized, tumour-specific, therapeutic vaccines for cancer. Nat Rev Immunol. 2018 Mar;18(3):168-182.
[2] Hollingsworth RE, Jansen K. Turning the corner on therapeutic cancer vaccines. NPJ Vaccines. 2019 Feb 8;4:7.






 010-56967680
010-56967680 info@bbctg.com.cn
info@bbctg.com.cn 苏公网安备:32068402320845号
苏公网安备:32068402320845号