异基因造血干细胞移植(allogeneic hematopoietic stem cell transplantation,allo-HSCT)是治疗白血病、淋巴瘤以及其他恶性血液病和免疫学疾病的有效措施,然而移植物抗宿主病(graft-versus-host disease,GvHD)的发生显著降低了移植后患者的生存率和生活质量,成为移植的最大障碍。GvHD可分为急性移植物抗宿主病(acute graft versus host disease,aGvHD)和慢性移植物抗宿主病(chronic graft versus host disease,cGvHD)。急性和慢性GvHD最初是根据其发生的时间来定义的,分别是在移植后100天之前或之后,但现在是根据病理学的差异来定义的,并被认为是在原来的时间范围之外发生的,在一些患者中是重叠的。目前,100天之前和之后发生的急性GvHD分别被定义为典型和晚期急性GvHD,而没有或存在急性GvHD的慢性GvHD分别被定义为典型和重叠的慢性GvHD,不考虑任何时间限制。皮肤病变是GvHD 最常见也是最早期的表现,其次是胃肠道和肝脏,并逐渐累及多个器官及组织。在接受allo-HSCT的患者中GvHD的发生率可达30%~70%,高达30%的病例中是致命的,因此GvHD 的预防成为移植后需要解决的首要问题[1]。
GvHD最初由Barnes、Loutit和Micklem报道,Billingham将其经典定义为供体免疫功能良好的细胞识别并攻击免疫功能低下的异体受体的宿主组织的综合症[2,3]。许多研究报道显示供者T细胞的激活、增殖、分化在GvHD的发生、发展中起着重要作用。供者的T细胞识别受者相异的抗原引起对靶器官的损伤,从而导致GvHD的发生。
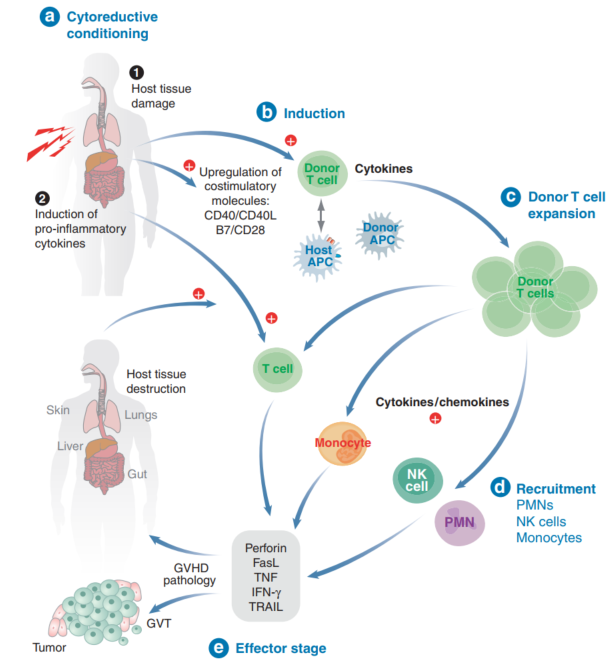
图1 GvHD的病理生理学[4]
GvHD的发生发展可分为多个阶段,如图1所示:
1. 第一阶段的特点是启动免疫反应。预处理(如辐照)诱导组织损伤和促炎细胞因子风暴的释放;
2. 第二阶段,诱导T细胞激活。开始于T细胞表面分子(TCR和共刺激分子)与二级淋巴组织中APC表面同源配体的识别和相互作用,在小鼠模型中,尽管供体和宿主APCs都可以在GvHD期间驱动进一步的T细胞激活,但宿主APCs是诱导GvHD的关键组成部分;
3. 在第三阶段,异体反应性T细胞经历扩增和分化为Th1/Tc1或Th2/Tc2细胞,这些细胞与GvHD的表现差异有关;
4. 第四阶段的特点是激活的细胞迁移到GvHD靶组织(肠道、肝脏、皮肤和肺),随后招募其他效应白细胞,导致随后的组织损伤。T细胞和其他类型的细胞对目标组织的归宿是由粘附性、趋化因子受体分子等调节,并由受伤组织中的趋化因子的产生来加强。趋化因子的产生最初是由于预处理导致,然后被疾病过程所放大;
5. 疾病过程的效应阶段是由这些细胞通过细胞表面和可溶性免疫效应分子,即FasL、肿瘤坏死因子(TNF-α)、TNF相关凋亡诱导配体(TRAIL)、穿孔蛋白、颗粒酶、干扰素(IFN-γ)对目标组织的破坏所决定的。组织损伤导致炎症信号增加,通过促进细胞因子风暴来延续和加强疾病过程,增强GvHD。
在小鼠的临床前研究中,GvHD的发生率和严重程度可以通过总生存率、体重减轻的测量、临床症状的评分和/或受影响组织的组织病理学评价来评估。
尽管已有60多年的研究,但广泛的免疫抑制仍被用于预防或治疗GvHD,导致癌症复发和感染的风险增加。因此,进一步深入了解疾病机制以及预测和预后生物标志物的开发是改善同种异体HSCT后GvHD发生、发展的关键。小鼠模型是研究GvHD的病理生理学和了解导致GvHD发展关键机制的一个重要临床前工具,GvHD进展机制和治疗方法的发展主要来自同种异体小鼠模型,然而并不能很好的转化到临床中;GvHD的人源化小鼠模型,将人类外周血单个核细胞(hPBMCs)注射到免疫缺陷小鼠中,可能在研究人类免疫反应时提供优势,这可能更容易转化为临床[5]。然而,GvHD人源化小鼠模型同样存在一些缺点,如人源化小鼠模型是异质性的,并非所有组织都会受到影响,这可能取决于预处理方法或人类细胞的来源。尽管如此,GvHD人源化小鼠模型仍然是一个有价值的工具,可以深入了解疾病机制以及异体HSCT后在GvHD发展中重要的关键分子和细胞靶点。
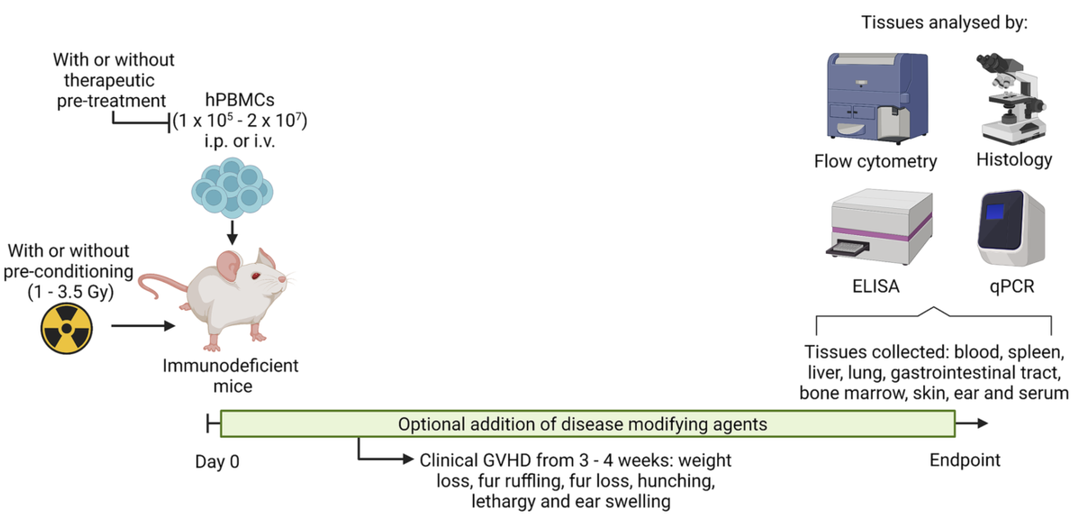
图2. GvHD人源化小鼠模型[6]
人源化小鼠模型大致可分为靶点人源化模型(用人类同源基因替换特定小鼠基因)和免疫重建人源化模型(将人类细胞注射到免疫缺陷小鼠体内)。后者已被广泛用于构建GvHD的人源化小鼠模型,以更好地了解该疾病的机制和测试治疗方法。当前,最常见的是通过将hPBMCs移植到免疫缺陷的小鼠体内来研究GvHD,如图2所示,在辐照或者未辐照条件下移植hPBMCs至免疫缺陷小鼠体内。
百奥赛图同样构建了GvHD人源化小鼠模型,使用B-NDG小鼠经辐照预处理后移植hPBMCs。B-NDG小鼠与NSG、NOG等小鼠具有相同的免疫缺陷程度,都是缺失T、B、NK细胞,是目前公认的免疫缺陷程度最高的小鼠之一。在构建PBMC重建小鼠模型时(通常不需要进行辐照预处理),需要对Donor进行筛选,选择合适的Donor进行PBMC重建;在此过程中,实验结果显示不同的Donor引起的GvHD会不同,不同的Donor注射到小鼠体内后,小鼠的生存、体重变化、姿势状态、小鼠活力、小鼠皮毛状态、小鼠皮肤状态会有不同的临床表现,如图3所示。在5×106 hPBMCs注射量下,GvHD强的Donor通常会在注射2周后先表现出小鼠体重下降、小鼠弓背的现象,严重时小鼠死亡。在GvHD研究中,小鼠死亡、体重下降是非常关键的2个指标,根据筛选时积累的数据,可以将hPBMCs Donor分为GvHD表现强的Donor和表现弱一些的Donor。
GvHD人源化小鼠模型造模时,选用的hPBMC Donor不同,最终构建的模型会有不同的临床表现,如图4。
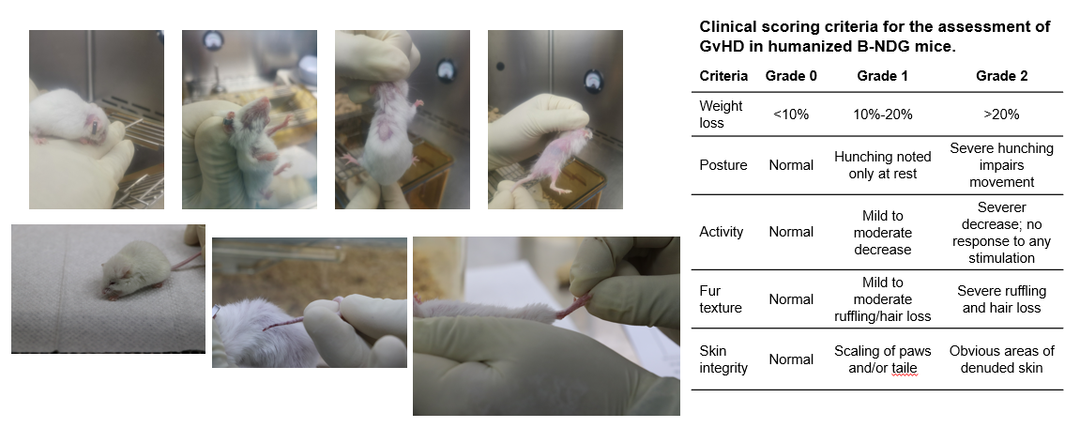
图3.小鼠模型GvHD的临床表现和评分标准
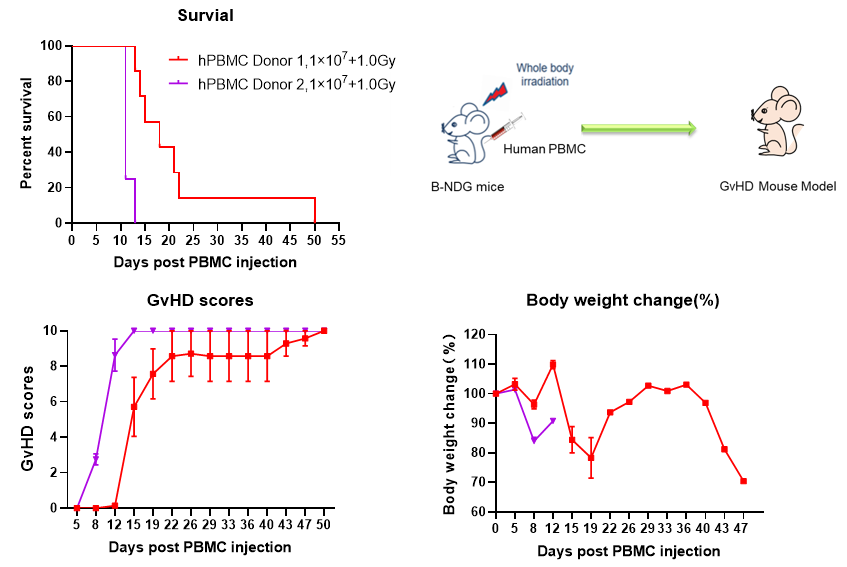
图4. 不同hPBMC Donor构建GvHD人源化小鼠模型的生存曲线、临床评分、体重变化
构建GvHD模型时,辐照预处理、hPBMCs注射量这两个变量的改变,是会对构建的小鼠模型产生的GvHD有影响;通常,辐照剂量的增加或者hPBMCs接种量的增加都可以增强GvHD。辐照后的小鼠注射hPBMCs细胞后,通常能够增强T细胞的重建,从而因T细胞重建水平更高导致GvHD增强,使小鼠更早的死亡,如图5所示。此外,在不进行辐照预处理,增加hPBMCs注射量也能构建GvHD模型,相比于进行辐照预处理的方法,前者需使用的hPBMCs细胞量更多。
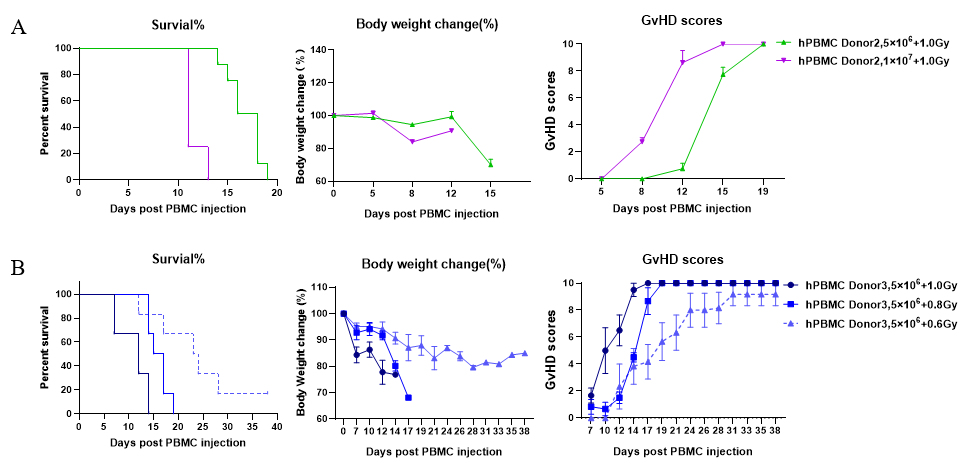
图5. (A) 不同hPBMC细胞注射量GvHD小鼠生存曲线、体重变化及GvHD评分; (B)不同辐照剂量GvHD小鼠生存曲线、体重变化与GvHD评分
在进行GvHD模型药效实验时,初次实验在不确定药物的药效情况下,建议先在GvHD弱一些的造模条件制备的模型小鼠上进行尝试;如有阳性药效,可增强GvHD造模条件,进一步探究受试品的药效。目前,我们已经完成了构建的GvHD模型药效应用的验证,使用T细胞上OX40靶点抑制剂在以B-NDG小鼠构建的GvHD模型上验证该抗体的药效,结果显示抗体给药组可以延长小鼠的生存周期和生存状态,分析原因可能是OX40抑制剂可以抑制T细胞的增殖,如图6。
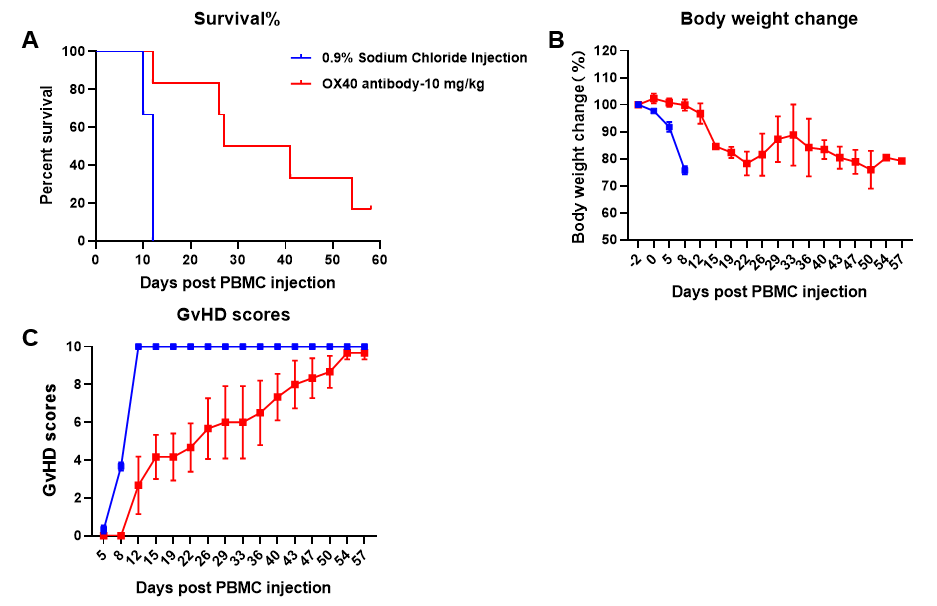
图6. B-NDG mice GvHD人源化小鼠模型药效验证: (A)生存曲线;(B)体重变化;(C)临床评分。
综上,基于B-NDG小鼠可成功构建GvHD人源化小鼠模型并用于相关受试品药效验证。目前,GvHD人源化小鼠模型主要应用在研究GvHD的发病机制及开发临床新型治疗药物,如人源抗体、MSC等;某些FDA批准的同种异体人源细胞治疗产品同样需要进行GvHD研究,如CAR-T治疗等。不仅仅是GvHD的研究,该模型还可用于评估药效学终点,根据作用机制不同,可分为两类:1.测试药物是免疫抑制型,如Treg、T细胞信号拮抗剂;2.测试药物是免疫激活型,如检查点抑制剂、T细胞激动剂。
在临床前肿瘤免疫治疗研究中,GvHD的发生、发展同样给肿瘤治疗研究带来了阻碍。特别是在PBMC重建人源化小鼠模型中,因GvHD发生导致的小鼠体重下降、严重时动物死亡,对药物药效实验的影响很大,使给药窗口缩短。针对这一问题,百奥赛图开发了B-NDG二代产品鼠,包括B-NDG B2m KO mice plus(敲除了小鼠MHC I)与B-NDG MHC I/II DKO mice plus(敲除了小鼠MHC I和MHC II),相比于B-NDG小鼠均能够改善小鼠PBMC重建后的GvHD,其中以B-NDG MHC I/II DKO mice plus效果最优。如图7,分别使用3个健康人来源的PBMC,经1.0Gy辐照后,注射PBMC 5×106。结果如预期一样,B-NDG B2m KO mice plus与B-NDG MHC I/II DKO mice plus均能改善GvHD,又以后者效果最佳;因为对体重变化、生存期的明显改善,能够延长给药窗口适合用于肿瘤免疫治疗药效研究。
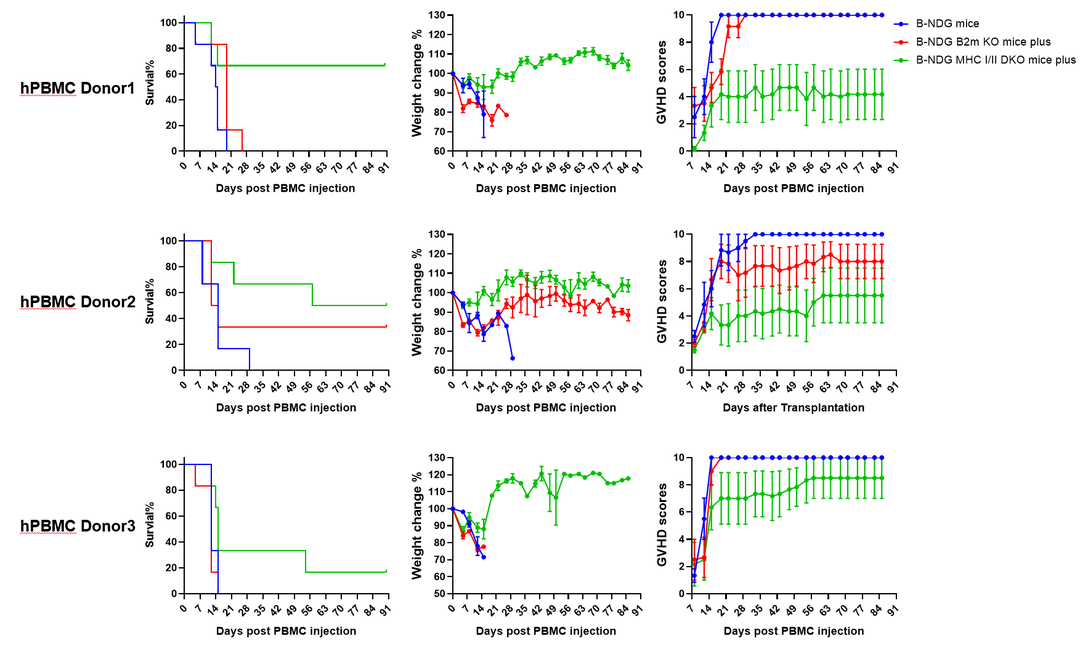
图7.不同品系小鼠GvHD模型构建后生存期、体重变化、临床评分的差异。
百奥赛图相关产品:
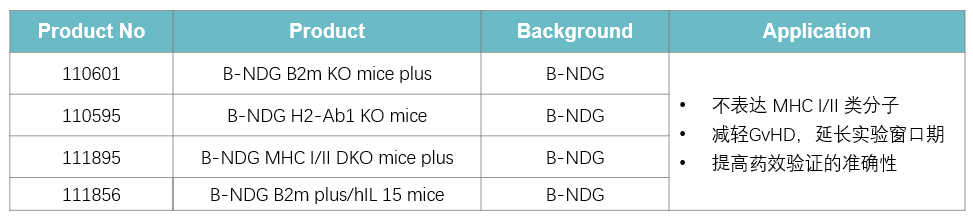
参考文献:
[1] Shouval, R., Fein, J.A., Labopin, M., et al. Outcomes of allogeneic haematopoietic stem cell transplantation from HLA-matched and alternative donors: a European Society for Blood and Marrow Transplantation registry retrospective analysis. Lancet Haematol. 2019, 6, e573–e584,
[2] Barnes D.W., Loutit J.F., Micklem H.S. “Secondary disease” of radiation chimeras: a syndrome due to lymphoid aplasia. Ann. NY Acad. Sci. 1962, 99:374–385.
[3] Billingham R.E. The biology of graft-versus-host reactions. Harvey Lect. 1966, 62:21–78.
[4] Welniak L. A., Blazar B.R., Murphy W.J. Immunobiology of Allogeneic Hematopoietic Stem Cell Transplantation. Annu. Rev. Immunol. 2007. 25:139–170.
[5] Sluyter R. and Watson D. Use of humanized mouse models to investigate the roles of purinergic signaling in inflammation and immunity. Front. Pharmacol. 2020, 11:596357.
[6] Elhage A., Sligar C., Cuthbertson P., et al. Insights into mechanisms of graft-versus-host disease through humanised mouse models. Bioscience Reports. 2022, 42:BSR20211986.






 010-56967680
010-56967680 info@bbctg.com.cn
info@bbctg.com.cn 苏公网安备:32068402320845号
苏公网安备:32068402320845号