药物靶点,即药物与人体生物大分子的结合部位,是新药发现的源头。目前全世界在研的抗体类药物靶点有一千多个,如何在其中找到好的药物靶点,开发出一类新药是所有创新药企面临的共同问题。
靶点基因的鉴定和验证在药物发现、开发过程中是必不可少且至关重要的一步。在哺乳动物生理学的背景下,基因敲除动物的表型研究已经成为破译基因功能及靶点验证的有力手段。与其他技术相比,基因敲除模型在药物靶点发现方面有自身独特的优势,敲除动物模拟了该靶点被完全抑制时的表型,因而能帮助我们了解该靶点在疾病中的作用,增加我们对人类正常生理过程及疾病发生机制的理解。

图片来源 [1]
小鼠作为在临床前生物医学研究中常用的模式动物之一,具有诸多方面的优势[2]:
小鼠和人类有着绝大部分同源序列,尽管二者在生理和免疫学存在一些差异,但基因组测序发现,小鼠和人类的~30,000个基因中,只有300个(即1%)是两个物种特有的;
在一项研究中所有小鼠通常具有相同的遗传背景(即单一近交系或回交到同一个遗传背景)。因此,所有研究对象的基因是相同的,消除了如遗传变异和基因多态性等潜在的复杂因素影响;
小鼠繁殖周期短,代际间隔小于3个月,且每窝产仔数量多,可以快速扩繁获得具有统计学意义数量的实验用鼠;
在特定的研究中小鼠具有明确的病史,且所有动物可在相同的环境下饲养,排除了其对实验结果可重复性的影响;
在一项特定的研究中,所有小鼠采用相同的实验方案,并可进行终点病理学的完整评估,包括检测生理参数和组织病理学分析;
小鼠基因组计划已经完成且小鼠基因改造技术成熟,可以构建模拟人类疾病的转基因小鼠模型以了解发病机制及对药物的反应等研究。

转基因小鼠模型在生物医学研究中的应用[2]
基因敲除小鼠模型除了可以提供表型分析信息外,其在抗体产生和鉴定方面具有两个优势。(1)与野生型小鼠相比,理论上特定基因敲除小鼠产生抗体的效率应该更高,因为敲除小鼠的免疫系统从未接触过免疫蛋白。(2)用于验证抗体特异性,“……严格控制抗体特异性,要求将野生型组织或细胞中的抗体反应性与敲除动物中的抗体反应性进行比较”。[3]
因此,基因敲除小鼠是开发新型药物或新治疗策略非常有用的实验工具。百奥动物开发了一系列靶点基因敲除(KO)小鼠,可以满足新药开发中“靶点发现”过程的动物模型需求,助力新药研发。
扫描下方二维码查看700+基因敲除小鼠资源库,下面以B-IL4ra KO mice(C)为例进行部分数据介绍。

B-IL4ra KO mice(C)
哮喘小鼠模型构建

实验动物:BALB/c,B-IL4ra KO mice(C),4-5周龄,雌性;
致敏阶段:第0,7,14天腹腔注射OVA+AI(OH)3;
激发阶段:小鼠在第21-25天每天接受2%的OVA雾化30分钟。
检测分析
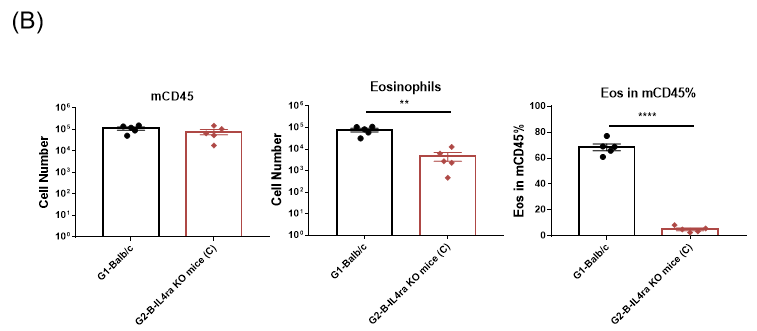
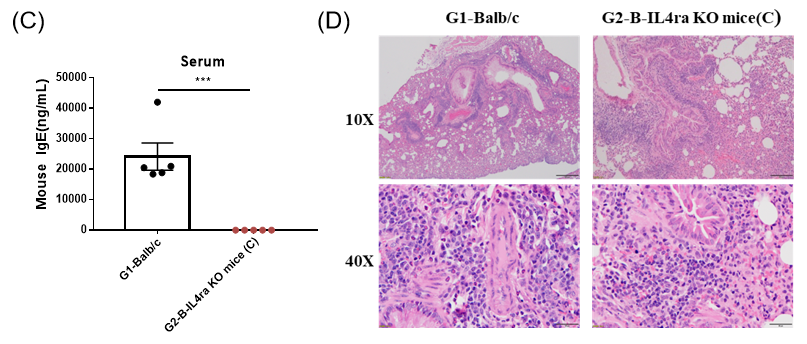
(B)哮喘小鼠的支气管肺泡灌洗液(BALF)中免疫细胞浸润分析;(C)血清中IgE的检测;(D)肺组织的HE染色。
通过对IL4RA靶点敲除小鼠的哮喘模型数据分析发现:Il4ra基因敲除后,与对照组相比,BALF中浸润的嗜酸性粒细胞数量和比例有显著性下降;血清中检测不到IgE;肺组织中浸润的炎性细胞和粘液分泌减少。这些结果证明IL4RA可以作为哮喘治疗的潜在靶点进行开发。
更多小鼠数据信息,欢迎联系我们。
参考资料
[1] Disease Models & Mechanisms (2016) 9, 101-103. doi:10.1242/dmm.024547
[2] Transgenic Res (2012) 21:327–349. doi:10.1007/s11248-011-9537-3
[3] Disease Models & Mechanisms (2019) 12, dmm038224.
[4] Drug Discovery Today, Volume 17, Supplement, February 2012, Pages S24-S30. https://doi.org/10.1016/j.drudis.2011.09.007






 010-56967680
010-56967680 info@bbctg.com.cn
info@bbctg.com.cn 苏公网安备:32068402320845号
苏公网安备:32068402320845号