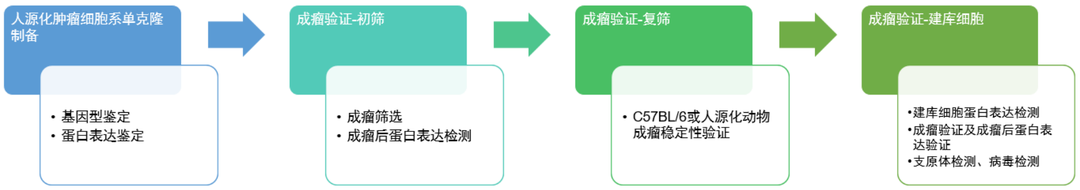
百奥动物自主研发了100余种人源化肿瘤细胞系,为临床前肿瘤免疫相关药物筛选提供了更多的选择,而如何筛选到稳定用于药效评价的人源化肿瘤细胞系,百奥动物有自己特有的研发流程,在产品研发过程中每个阶段都有严格的质量控制,且经过多次数据验证,最终获得稳定的肿瘤模型。
举个例子。
B-hTF MC38
01、基本信息

02、背景信息
组织因子TF(Tissue Factor),又名CD142、TFA、F3,属于组织因子家族,是单次跨膜蛋白,是凝血因子VII/VIla的细胞受体,表达于动脉外膜的成纤维细胞,并存在于中膜平滑肌细胞的外层中[1, 2]。在正常情况下,血液中的单核细胞与接触血浆的血管内皮细胞并不表达TF,故正常人血浆中TF含量极低(<100ng/L)。
在癌症生物学中,TF是一种参与肿瘤信号传导和血管生成的蛋白质,在绝大多数宫颈癌患者和许多其他实体瘤(包括卵巢、肺、胰腺、结直肠和头颈部癌症)中过度表达。基于TF因子在许多实体瘤中的高表达和快速内化及在血管系统中不表达,TF成为了开发ADC药物的理想靶标。目前有两种策略:
(1)靶向TF,诱导肿瘤梗死;
(2)靶向TF,向肿瘤内输送细胞毒性药物。
目前针对TF靶点开发的抗体类药物有45个,大部分集中在单克隆抗体研究和ADC药物研究,治疗领域包括呼吸障碍性疾病和多种实体瘤,且大部分处于位于临床前研究和生物测试阶段,新药开发前景辽阔,百奥动物自主研发的B-hTF MC38细胞系在C57BL/6小鼠、B-hCD3E 小鼠和B-h4-1BB 小鼠体内成功建立肿瘤模型,助力于靶向TF靶点的单克隆抗体药物及双特异性抗体药物的临床前评价。(数据来源:CDDI)
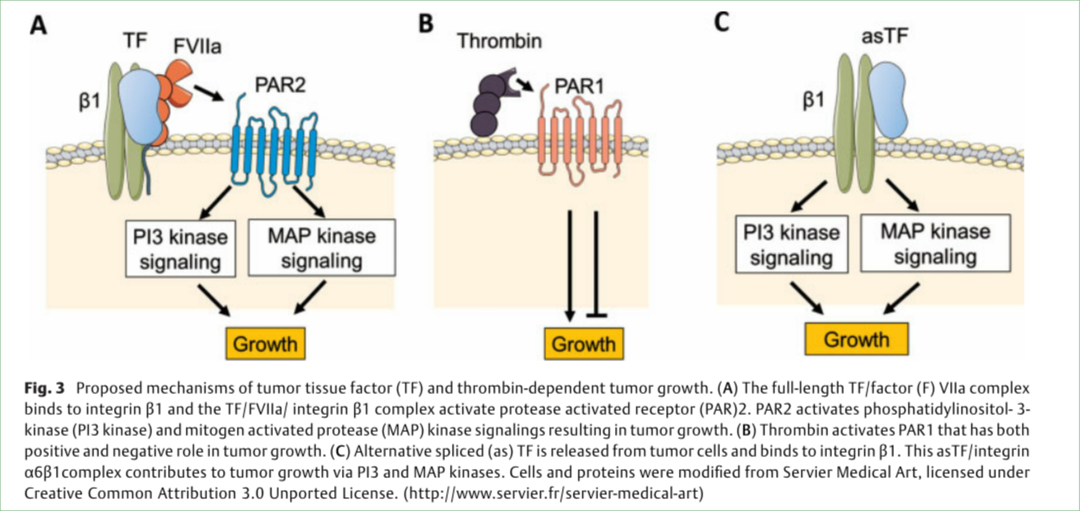
图1. TF对肿瘤生长机制
03、人源化肿瘤细胞系单克隆制备
制备策略
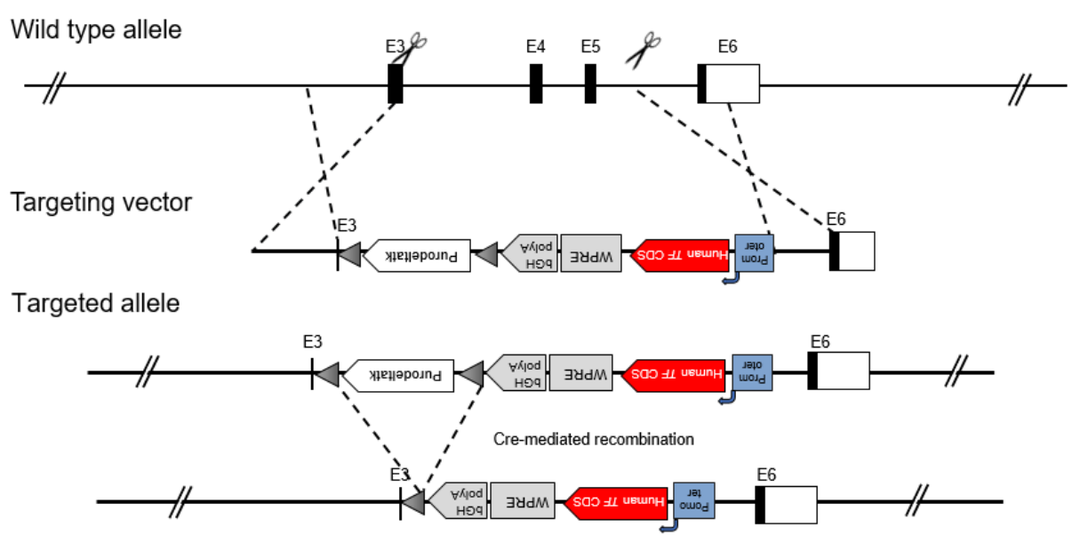
图2. B-hTF MC38细胞系人源化策略
利用基因编辑技术,将鼠源TF基因的3-5号外显子替换为人源TF编码序列,由外源启动子启动人源TF蛋白的表达,同时外源基因的插入导致内源小鼠TF基因的部分缺失,达到鼠源TF蛋白表达缺失的目的,从而构建稳定表达人源TF蛋白的MC38细胞系。
B-hTF MC38基因型鉴定
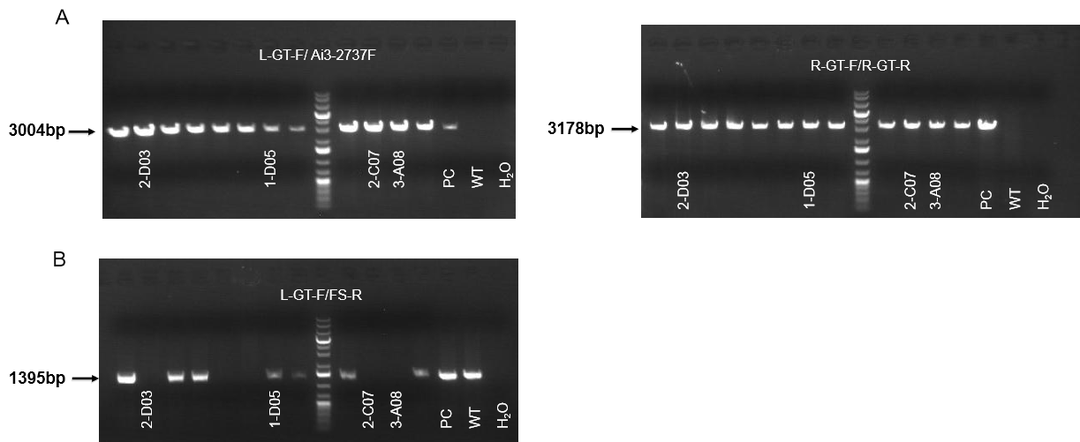
图3. B-hTF MC38细胞系基因型鉴定
利用L-GT-F/Ai3-2737F、R-GT-F/R-GT-R引物进行PCR扩增外源引入的基因序列并通过测序鉴定引入序列的准确性(A),利用L-GT-F/FS-R引物进行PCR扩增并通过测序鉴定鼠源基因是否敲除(或移码突变)(B),每个克隆经过至少两次的基因型鉴定判定最终结果,结果显示B-hTF MC38细胞系成功敲除鼠源基因,敲进人源目标序列。
B-hTF MC38蛋白表达鉴定
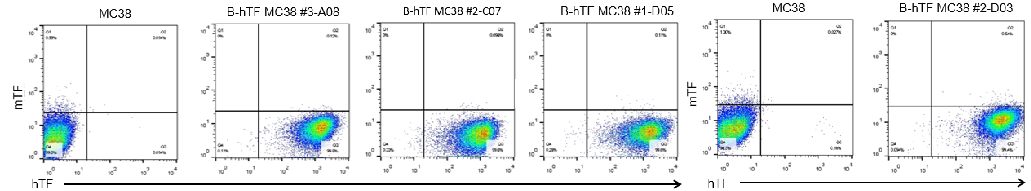
图4. 流式细胞术检测B-hTF MC38及MC38细胞系hTF蛋白表达情况
B-hTF MC38细胞系高表达人源TF蛋白,MC38野生细胞系不表达鼠源及人源TF蛋白。
通过基因型鉴定及蛋白水平鉴定,验证B-hTF MC38人源化细胞系改造成功,可进入成瘤筛选阶段。
04、成瘤验证-初筛
B-hTF MC38阳性单克隆成瘤筛选及成瘤后人源蛋白表达情况
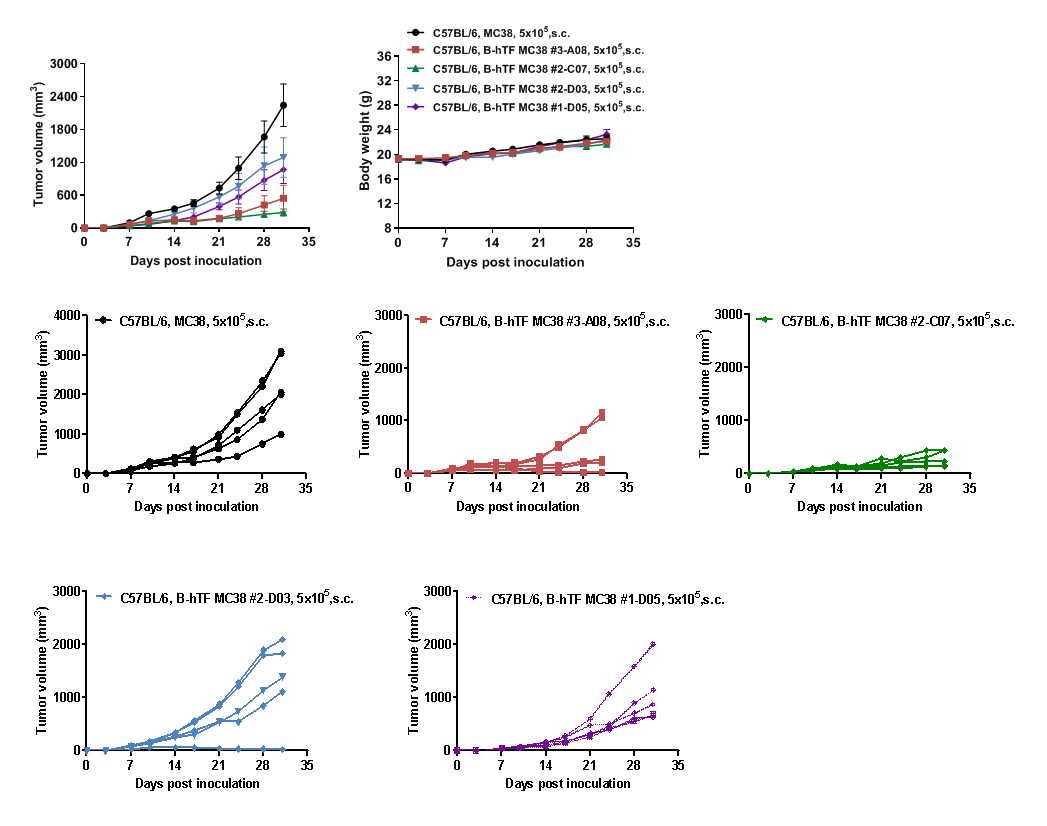
图5. C57BL/6小鼠皮下接种B-hTF MC38单克隆和MC38细胞后的生长动力学及体重变化
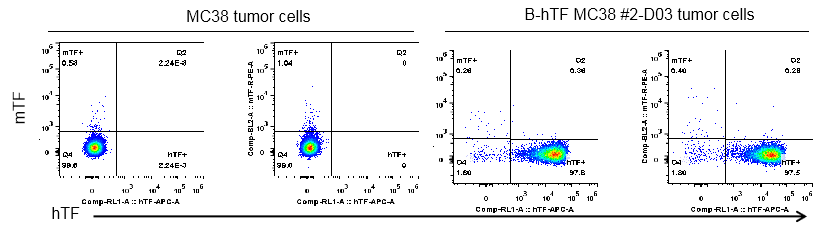
图6. B-hTF MC38 #2-D03和MC38细胞系成瘤后的人源TF蛋白表达情况
结果表明:B-hTF MC38 #2-D03在C57BL/6小鼠体内成瘤成功,成瘤后肿瘤细胞高表达人源TF蛋白,B-hTF MC38细胞系在C57BL/6小鼠体内成功建立肿瘤模型。
05、成瘤验证-复筛
B-hTF MC38 #2-D03在C57BL/6小鼠体内成瘤成功,为验证其稳定性,同时为验证靶向TF双抗药物的评价提供更多人源化动物肿瘤模型,我们将该克隆在B-hCD3E 小鼠和B-h4-1BB 小鼠体内进行成瘤验证。
人源化肿瘤细胞系体内成瘤稳定性验证阶段,我们会根据其应用选择不同的小鼠品系进行验证。
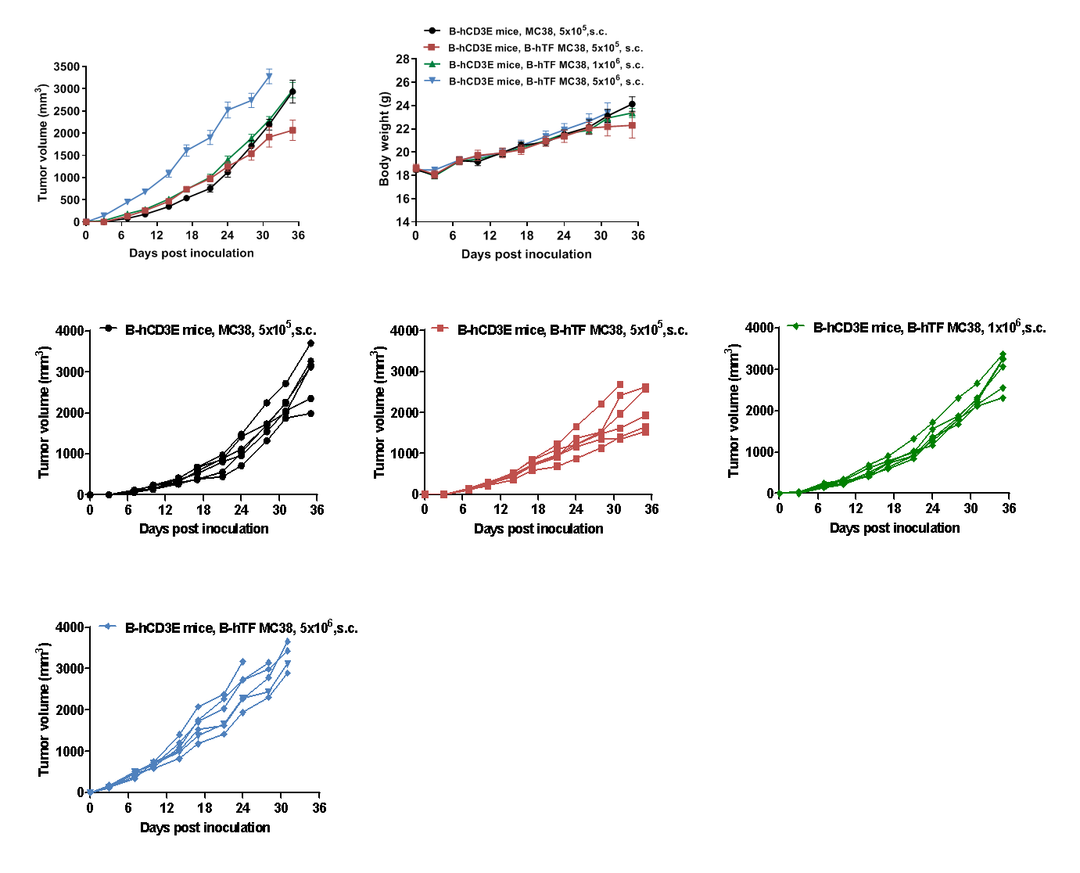
图7. B-hCD3E 小鼠皮下接种B-hTF MC38和MC38细胞后的生长动力学及体重变化
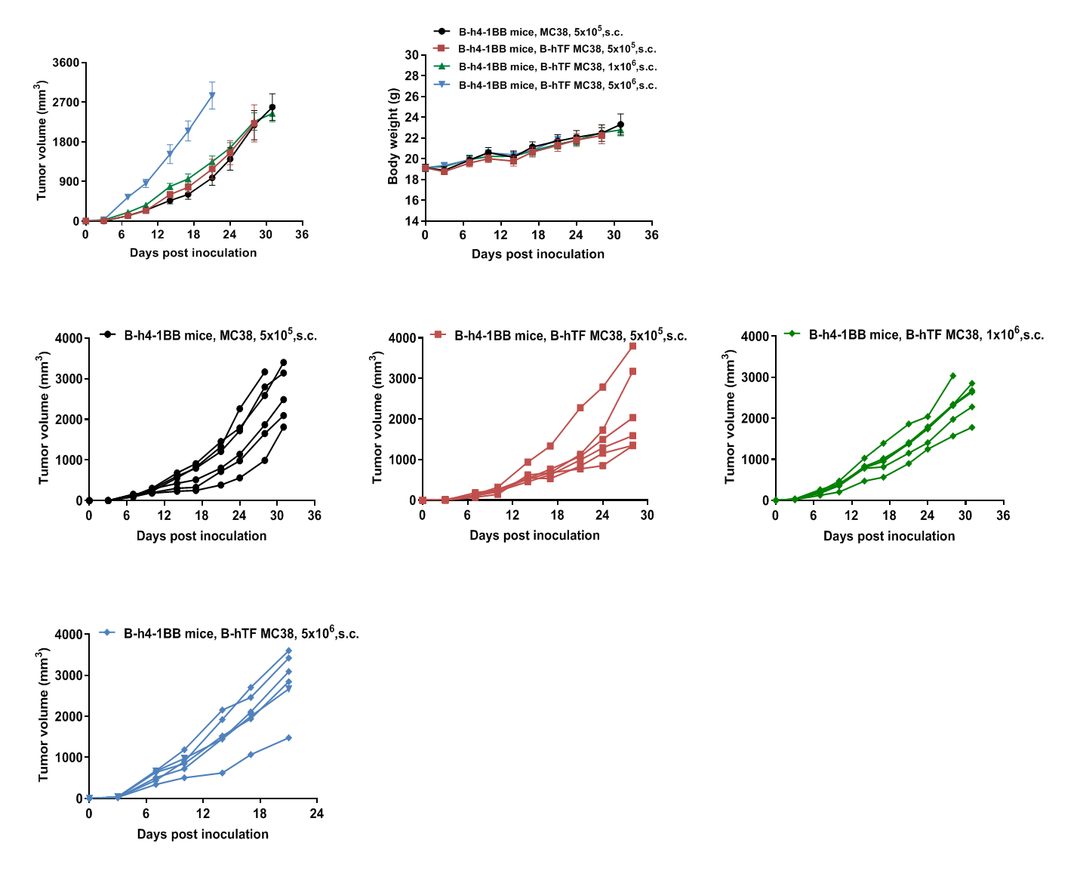
图8. B-h4-1BB 小鼠皮下接种B-hTF MC38和MC38细胞后的生长动力学及体重变化
结果表明:B-hTF MC38 #2-D03在B-hCD3E 小鼠和B-h4-1BB 小鼠体内成功建立肿瘤模型。
06、成瘤验证-建库细胞
B-hTF MC38 #2-D03细胞建库后成瘤筛选及成瘤后人源蛋白表达情况
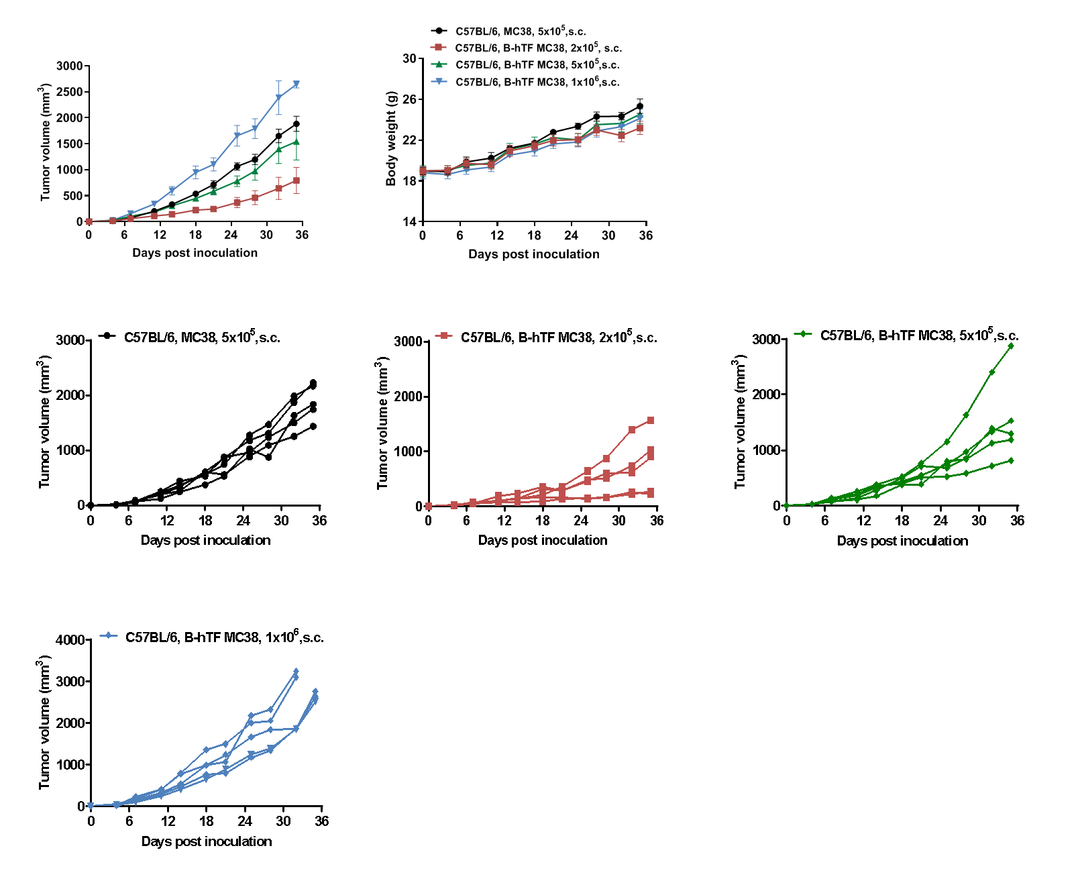
图9. C57BL/6小鼠皮下接种B-hTF MC38 #2-D03和MC38细胞后的生长动力学及体重变化
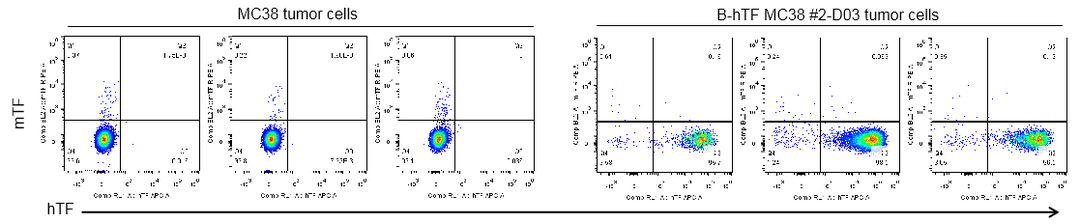
图10. B-hTF MC38 #2-D03和MC38细胞系成瘤后的人源TF蛋白表达情况
结果表明:B-hTF MC38 #2-D03建库细胞在C57BL/6小鼠体内成瘤成功,成瘤后肿瘤细胞高表达人源TF蛋白,建库细胞在C57BL/6小鼠体内成功建立肿瘤模型,可用于靶向TF药物的临床前药效评价。
B-hTF MC38人源化细胞系经过基因型鉴定、蛋白水平表达鉴定证明该细胞成功敲除鼠源TF基因,敲进人源TF目标基因,鉴定后的单克隆经过成瘤初筛筛选合适克隆进入复筛以及细胞建库后成瘤验证,证明B-hTF MC38人源化细胞系在C57BL/6小鼠、B-hCD3E 小鼠和B-h4-1BB 小鼠体内成功建立肿瘤模型,综合多次成瘤数据,该细胞系体内接种剂量建议1E6,该模型可用于靶向TF单抗及多抗药物的临床前药效评价。
应用于双特异性抗体临床前评价的人源化肿瘤细胞系

(部分产品开发中)
更多人源化肿瘤细胞系在开发中,敬请期待~
参考文献
1. Monroe, D.M. and N.S. Key, The tissue factor-factor VIIa complex: procoagulant activity, regulation, and multitasking. J Thromb Haemost, 2007. 5(6): p. 1097-105.
2. Hisada, Y. and N. Mackman, Tissue Factor and Cancer: Regulation, Tumor Growth, and Metastasis. Semin Thromb Hemost, 2019. 45(4): p. 385-395.






 010-56967680
010-56967680 info@bbctg.com.cn
info@bbctg.com.cn 苏公网安备:32068402320845号
苏公网安备:32068402320845号