TSLP(Thymic Stromal Lymphopoietin, 胸腺基质淋巴细胞生成素)编码造血细胞因子,通过结合TSLP受体和IL-7Rα链的异二聚体受体复合物传递信号。主要影响髓系细胞,诱导单核细胞释放T细胞吸引趋化因子,促进CD11c(+)树突状细胞的成熟。该蛋白促进2型辅助性T细胞(TH2)反应,参与各种炎症性疾病中的免疫反应,包括哮喘、过敏性炎症和慢性阻塞性肺疾病。因此TSLP被认为是治疗这类疾病的潜在治疗靶点。
过敏原、细胞因子、病毒、细菌等多种触发因素可以激活肺和肠上皮细胞及角质形成细胞释放TSLP,并携带正电荷,TSLP与携带负电荷的TSLPR快速结合,然后与IL17Rα形成三元复合物,激活STAT3、STAT5和JAK2通路,启动促炎信号。
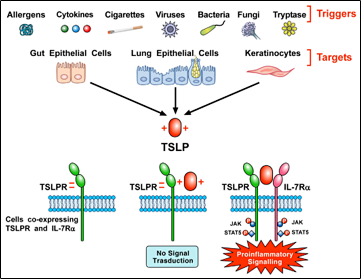
图1 TSLP的产生及信号转导[1]
TSLP在气道上皮接触过敏原或其他激发剂后产生并协调哮喘反应中的核心作用。通过细胞因子在不同细胞类型之间进行细胞间通讯可引起免疫系统天然以及适应性的免疫活性。TSLP能够诱导DC细胞表达OX40L,与初始T细胞的OX40相互作用,促进2型免疫反应发生,导致大量的促炎性细胞因子产生(IL4、IL5和IL13等),从而增强IgE、肥大细胞和黏液产生,增加气道高反应。TSLP在哮喘中的关键介质,靶向TSLP及其信号转导的抗体药物被认为是治疗哮喘的有效策略[2]。
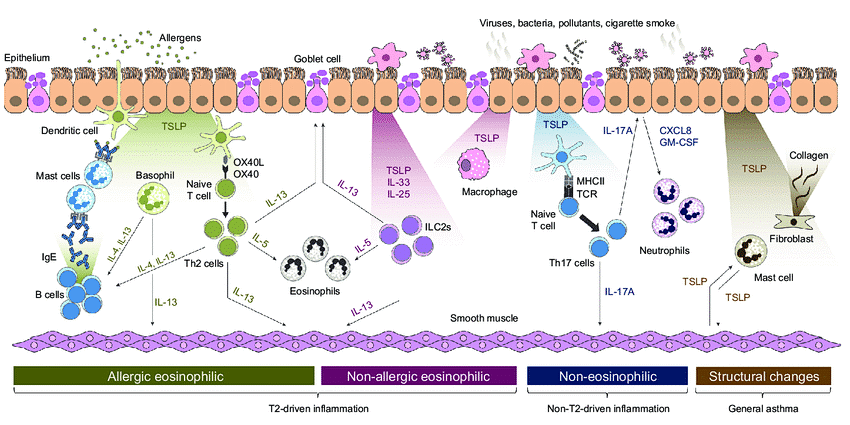
图2 TSLP在不同哮喘内型驱动疾病机制中的作用[2]
国内外TSLP抗体药物开发进展
目前已有针对哮喘疾病的多个靶点抗体药物开发,包括IL4、IL13、IL5、IL6、GM-CSF等。TSLP抗体药物在经历多个临床试验停止后,近期迎来曙光,由阿斯利康与安进合作开发的Tezepelumab(抗TSLP全人源单抗)获FDA受理BLA并授予优先审查,如果成功上市,将使严重哮喘患者广泛受益。
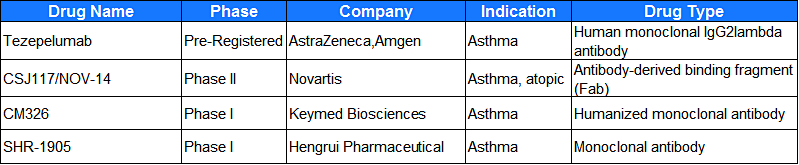
信息来源于公开信息;项目进展仅展示最快阶段
“百奥动物”上新B-hTSLP/hTSLPR小鼠,为TSLP抗体药物的药效评估提供有力的模型。
B-hTSLP小鼠蛋白表达分析
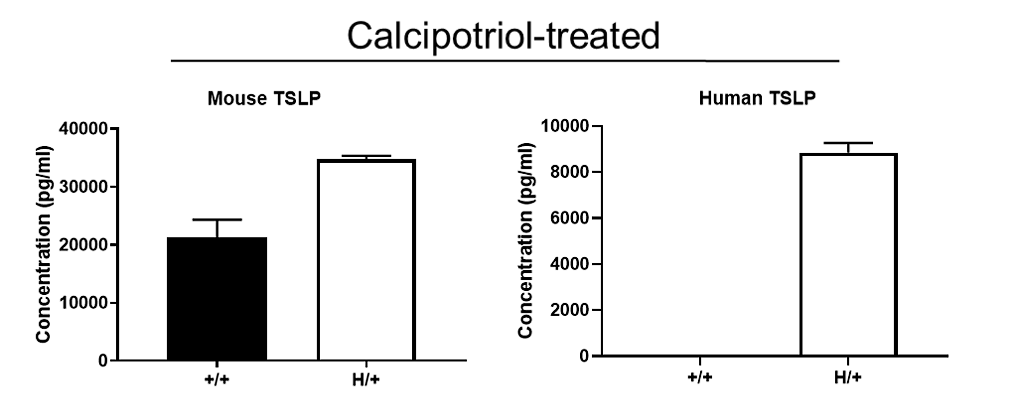
ELISA法检测分析杂合B-hTSLP小鼠种属特异性TSLP表达
将卡泊三醇(MC903)溶于乙醇中,局部应用于野生型C57BL/6小鼠(+/+)或杂合子B-hTSLP小鼠(H/+)的耳部,持续3天。ELISA法分析2只小鼠耳磨上清液。在野生型C57BL/6小鼠和杂合B-hTSLP小鼠中可检测到小鼠TSLP。人TSLP仅在杂合B-hTSLP小鼠中可检测到,在WT小鼠中未检测到。
B-hTSLP/hTSLPR小鼠蛋白表达分析
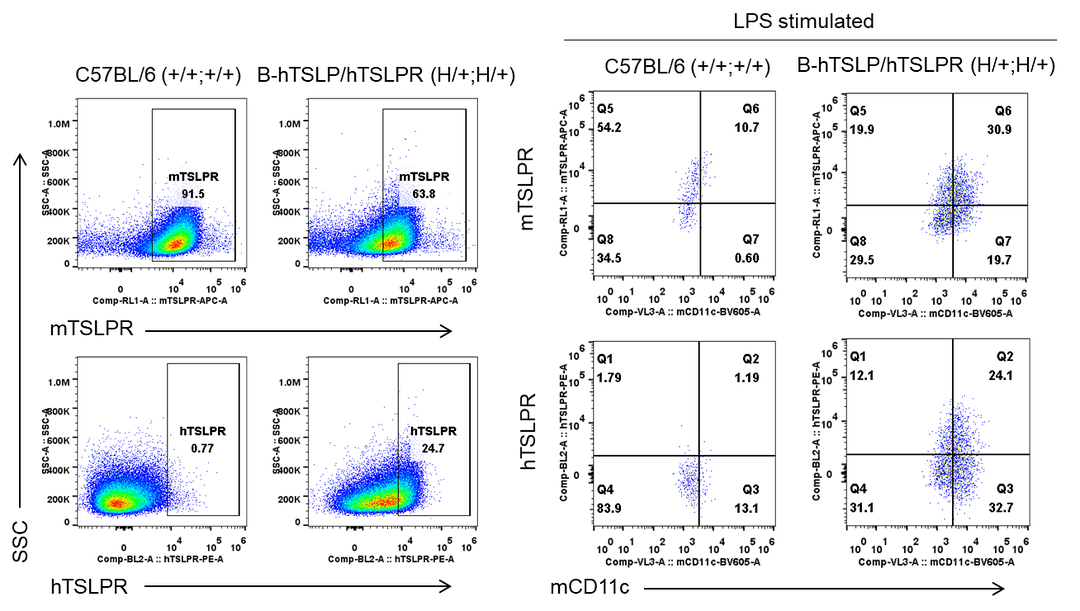
通过流式细胞术对杂合B-hTSLP/hTSLPR小鼠进行种属特异性TSLPR表达分析
(左图)收集野生型C57BL/6小鼠和杂合B-hTSLP/hTSLPR小鼠的巨噬细胞;(右图)从野生型C57BL/6小鼠和杂合B-hTSLP/hTSLPR小鼠的骨髓中诱导树突状细胞,并用LPS刺激。用种属特异性抗TSLPR抗体进行流式细胞仪分析。
在野生型C57BL/6小鼠和杂合B-hTSLP/hTSLPR小鼠中可检测到小鼠TSLPR。在杂合B-hTSLP/hTSLPR小鼠中可检测到人TSLPR,但在野生型小鼠中未检测到。
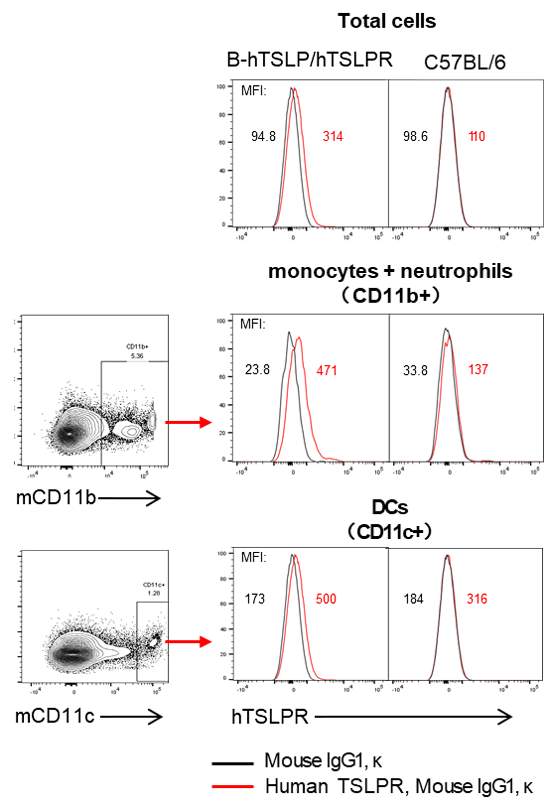
通过流式细胞术在纯合B-hTSLP/hTSLPR小鼠中进行人TSLPR表达分析
收集野生型C57BL/6小鼠和纯合B-hTSLP/hTSLPR小鼠的脾细胞,用种属特异性抗TSLPR抗体进行流式细胞仪分析。在纯合b-hTSLP/hTSLPR小鼠的总脾细胞、CD11b + 细胞(单核细胞和中性粒细胞)和CD11c + 细胞(DC)中可检测到人TSLPR,但在野生型C57BL/6小鼠的这些细胞中未检测到。
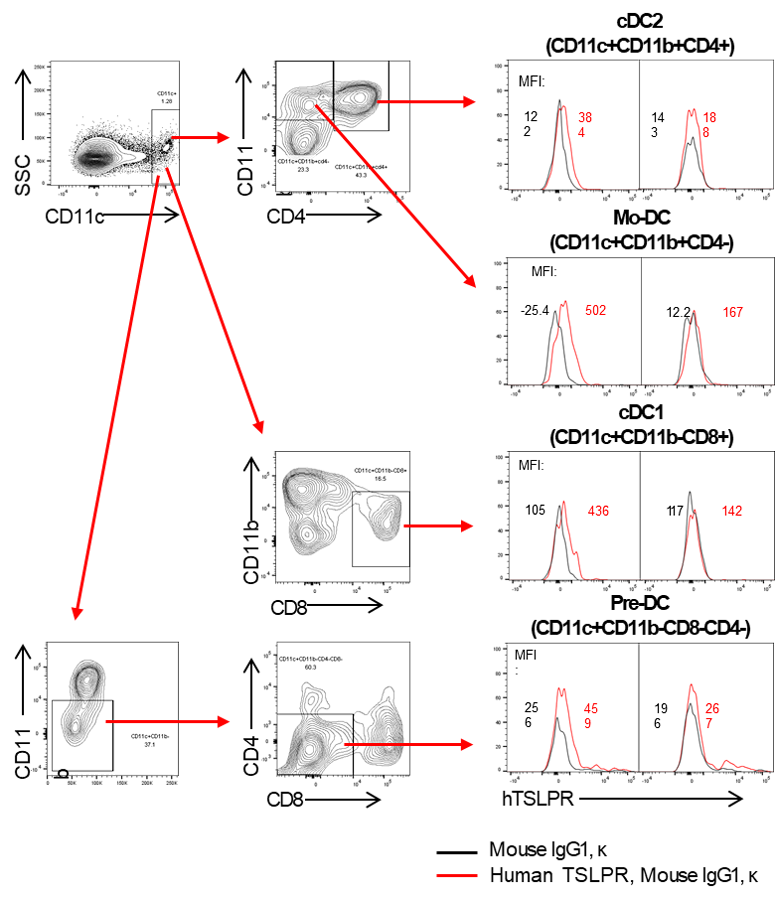
通过流式细胞术在纯合B-hTSLP/hTSLPR小鼠中进行人TSLPR表达分析
收集野生型C57BL/6小鼠和纯合B-hTSLP/hTSLPR小鼠的脾细胞,用种属特异性抗TSLPR抗体进行流式细胞仪分析。在纯合B-hTSLP/hTSLPR小鼠的cDC2、mo-DC、cDC1和pre-DC上可检测到人TSLPR,但在野生型C57BL/6小鼠的这些细胞上未检测到。
哮喘疾病相关动物模型
参考资料
[1]Varricchi, G., et al., Thymic Stromal Lymphopoietin Isoforms, Inflammatory Disorders, and Cancer. Front Immunol, 2018. 9: p. 1595.
[2] Gauvreau, Gail & Sehmi, Roma & Ambrose, Christopher & Griffiths, Janet. Thymic stromal lymphopoietin: its role and potential as a therapeutic target in asthma. Expert Opinion on Therapeutic Targets, 2020.






 010-56967680
010-56967680 info@bbctg.com.cn
info@bbctg.com.cn 苏公网安备:32068402320845号
苏公网安备:32068402320845号