哮喘是一种异质的、高度复杂的呼吸道慢性炎症性疾病,可引起患者咳嗽、喘息、呼吸急促和胸闷等症状,严重时可危及生命。哮喘通常是由各种上皮损伤,如病毒、过敏原、细菌、空气污染物和其他环境刺激物引起的。
不同国家哮喘患病率差异较大,有的国家低至1%,有的则高达18%,全世界的哮喘患者约有3.39亿人。哮喘有明显的性别差异,不同年龄男女性的患病率和严重程度不同,据调查,13岁以下的男孩哮喘发病率较高,但成年后,女性的发病率增加,高于男性(图1)。性激素、遗传和表观遗传变异、社会和环境因素以及对哮喘治疗的反应是影响哮喘发病率、流行率和严重程度的重要因素。

图1. 发达国家哮喘终生患病率百分比。[1]
哮喘的症状主要是由于气道炎症导致的,炎症引起的过程包括粘液产生、气道壁重塑和支气管高反应性。气道壁重塑和气道粘液堵塞导致的持续性气道阻塞是目前临床治疗哮喘未满足的迫切医疗需求之一。哮喘通常在幼年发病(早发型哮喘),但也有些在成年发病(晚发型哮喘)。晚发型哮喘比早发型哮喘更严重,但与过敏的关系更小。过敏性哮喘往往始于幼年时期,与辅助T细胞2 (Th2)反应有关。当接触过敏原后,过敏原特异性Th2细胞产生2型细胞因子(如IL-4、IL-5、IL-9、IL-13),导致气道壁上大量嗜酸性粒细胞积累,粘液分泌增多,过敏原特异性B细胞合成免疫球蛋白E (IgE)增加。而晚发型哮喘分Th2型和非Th2型,非Th2型通常与肥胖、衰老和吸烟有关,Th2型常伴有复发性和慢性鼻-鼻窦炎伴鼻息肉(CRSwNP),并对阿司匹林敏感,可能与气道嗜酸性粒细胞数量增多有关。

图2. 哮喘发病中驱动气道炎症的机制。与哮喘发病相关的2型(绿色)和非2型(黄色)适应性免疫反应。图中显示了2型反应的激活和分化导致IL-4、IL-5、IL-9和IL-13产生增加,以及嗜酸性粒细胞浸润增加,B细胞产生IgE、AHR、FENO和粘液产生增加。非2型炎症在成人比哮喘儿童更常见。非2型炎症导致T细胞产生的IL-17A或IFN-γ增加,或IL-6、TNF和IL-1增加导致中性粒细胞浸润、AHR、FENO和粘液产生增加。[1]
随着研究的深入,哮喘表型的分类已发展成哮喘内型,主要是基于哮喘患者痰液中的炎性细胞类型,分为2-高型或-超高型(嗜酸性粒细胞)和2-低型(非嗜酸性粒细胞,中性粒细胞)。2-高内型是由Th2相关的细胞因子如IL-4、IL-5和IL-13调控的,超2型高哮喘则反映了更严重的疾病形式。2-低内型更加复杂,目前尚未发现生物标志物。2-低型哮喘一般包括所有没有2-高型炎症的哮喘患者。[2, 3]
靶点药物进展
哮喘发病机制复杂,众多细胞因子(TSLP, IL4, IL5, IL13, IL-33等)参与其中,阻断某一个细胞因子治疗哮喘只能达到部分效果,药物联合使用将是治疗该病的发展趋势。根据科睿唯安数据库检索哮喘有3万+的药物发现数据结果,范围缩小到抗体类药物,也有73个上市/处在临床阶段的药物,其中上市药物15个,III期9个,II期29个,部分数据展示如下。阿斯利康已有多个药物上市,覆盖靶点广,占据明显的主导地位。今年2月,Tezspire (tezepelumab)还在美国获批用于12岁及以上严重哮喘患者的一次性预充型自我给药。Tezspire 是第一个也是唯一一个被批准用于治疗严重哮喘患者的生物制剂,在其批准的标签内没有表型或生物标志物的限制。面对如此多哮喘相关靶点药物研究现状,谁会是下一个闪光者,值得期待!
表1. 部分研究进展

数据整理自科睿唯安数据库
BioMice百奥动物利用基因编辑技术自主开发了一系列哮喘相关靶点人源化小鼠,同时基于靶点人源化小鼠和野生型小鼠构建了哮喘模型可用于药效评估,助力该疾病药物的临床前研究。
表2. 哮喘相关靶点人源化小鼠

表3. 药理药效服务内容

模型示例:B-hTSLP/hTSLPR mice plus
胸腺基质淋巴细胞生成素(Thymic stromal lymphopoietin, TSLP)是一种上皮细胞来源的I型细胞因子,属于IL-27细胞因子家族。主要在活化的肺和肠上皮细胞、角质形成细胞和成纤维细胞中表达。TSLPR又称为细胞因子受体样因子2(CRLF2),是TSLP的受体,属于血细胞生成素家族。TSLPR主要在树突细胞和单核细胞中表达。
当过敏原、烟雾、病毒、细菌和真菌等诱因刺激肺和肠道上皮细胞和角质形成细胞释放TSLP(正电荷),结合TSLPR(负电荷)形成TSLPR:TSLP二元复合物,与IL-7Rα结合形成三元复合物TSLPR-TSLP-IL-7Rα,磷酸化JAK和STAT5启动促炎信号(图3)。

图3. TSLP及其信号复合体信号启动示意图。[4]
有证据表明,TSLP是哮喘病理生理学的关键因子,其对各种适应性和先天性免疫细胞和结构细胞的作用,可驱动嗜酸性炎症(过敏性和非过敏性)、非嗜酸性炎症和气道的结构变化。阻断TSLP的临床试验对哮喘患者产生了积极的治疗结果,减少了急性发作和炎症,同时改善了肺功能。[5]
利用B-hTSLP/hTSLPR mice plus 构建哮喘小鼠模型

抗人TSLP抗体在哮喘小鼠模型中的体内药效


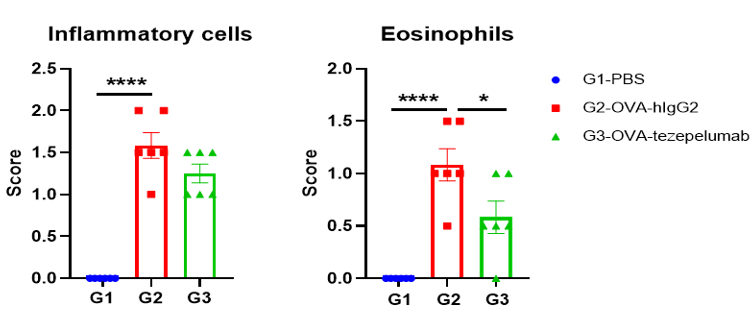
流式细胞术分析BALF中的免疫细胞。雄性B-hTSLP/hTSLPR plus小鼠用OVA免疫诱导建立小鼠哮喘模型(n=6)。在致敏阶段给予抗人TSLP抗体(Tezepelumab,内部合成)。实验结束后收集BALF,检测肺组织浸润炎性细胞。结果显示,嗜酸性粒细胞在OVA诱导但未处理组(G2)的比例显著高于非诱导组(G1),而处理组(G3)与G2组相比,嗜酸性粒细胞比例显著降低。G3组CD45+细胞和嗜酸性粒细胞数量也有下降趋势。结果表明,抗人TSLP抗体能有效降低经OVA诱导的B-hTSLP/hTSLPR plus小鼠嗜酸性粒细胞的数量和比例。

哮喘小鼠模型血清中OVA特异性IgE的产生水平。在实验终点收集血清,分析OVA特异性抗体反应的IgE水平。结果显示,接受tezepelumab治疗的小鼠体内IgE水平低于未接受治疗的小鼠。

哮喘小鼠模型H&E染色。在实验终点收集肺组织,H&E染色结果显示接受PBS气雾剂的B-hTSLP/hTSLPR plus小鼠肺组织无任何炎症反应。接受OVA的B-hTSLP/hTSLPR plus小鼠支气管周和血管周炎症显著增加。在给予tezepelumab治疗的小鼠中观察到嗜酸性粒细胞浸润显著减少。黑色箭头:炎症细胞;黑色三角形:嗜酸性粒细胞。
更多小鼠实验数据信息欢迎联系我们。
参考文献
[1]. https://doi.org/10.1183/16000617.0067-2021
[2]. https://doi.org/10.1016/j.cell.2021.02.016
[3]. doi: 10.1111/all.14027
[4]. doi: 10.3389/fimmu.2018.01595
[5]. doi: 10.1080/14728222.2020.1783242






 010-56967680
010-56967680 info@bbctg.com.cn
info@bbctg.com.cn 苏公网安备:32068402320845号
苏公网安备:32068402320845号