2022年9月29日,美国参议院通过了美国食品药品监督管理局现代化法案(FDA Modernization Act 2.0),将“动物实验”改为“非临床试验”。这一消息被国内部分解读为“取消对新药进行动物试验的联邦授权”,引起业内的广泛关注和讨论。然而新药评价是一项科学严谨的事情,许多替代方案还在早期研究阶段,在现行的新药审评标准中,动物实验仍然是非临床评价中非常重要的环节。
该法案的提出除了基于动物保护、新技术发展的考虑,日益上涨的猴价可能也是推动因素之一,那么在有限的非人灵长类动物(NHPs)资源下,是否有用于药物安全性评价的替代模型呢?
参照ICH指导原则和FDA指南:
ICH S6(R1)生物制品的临床前安全性评价指导原则中,对关于动物种属的选择指出:“当无相关动物时,应考虑使用表达人源受体的相关转基因动物或者使用同源蛋白。”
今年2月,FDA发布的《缓解COVID-19大流行引起的非人灵长类动物供应限制的非临床研究考虑因素行业指南 》提出:“尽管ICH S6(R1)声明偏向在NHP中试验临床候选药物,但在NHPs供应紧缺的情况下,FDA强烈鼓励使用具有科学依据的合适的替代模型来评估DART终点(如啮齿动物中的特定种属替代物,转基因啮齿动物)。”
对于靶点抗体药物来说,当NHPs不是相关种属,且药物在啮齿类动物具有生理活性,或NHPs供应紧缺的情况下,转基因啮齿动物,尤其是靶点人源化小鼠将是药物更好的非临床安全性评价动物模型选择。
百奥动物靶点人源化小鼠成功助力药物IND申报
靶点人源化小鼠是将小鼠的靶点基因进行的人源基因的替换改造,其具有靶点基因生理学功能、繁殖周期短、研究成本较低等优势,能够用于靶点药物的非临床药效及安全性评估,包括药物PK、一般毒性(单次/多次给药毒性)、免疫毒性、生殖毒性等研究。
截止目前,百奥动物自主研发的靶点人源化小鼠已经助力多家药企基于小鼠的长毒、生殖毒性等安全性评价数据成功获批IND,8款药物已获得NMPA IND临床批件,3款药物获得FDA IND临床批件,其中2款为中美双报产品。热门人源化小鼠品系包括免疫检查点类:B-h4-1BB mice,B-hCCR8 mice,B-hLAG3 mice,B-hCD38 mice,B-hCD40 mice,细胞因子类:B-hIL4/IL4RA mice,B-hIL36R mice,代谢类:B-hGLP1R mice等等。
用于临床前毒理研究的热门人源化小鼠品系
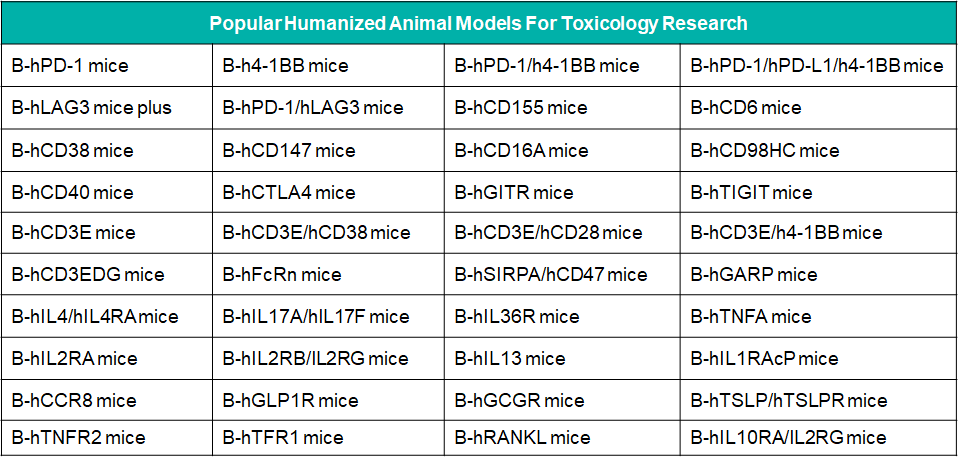
人源化小鼠也可以在一定程度反应患者在临床上的不良反应,下面以B-hCD40小鼠的部分内部试验数据为例:
➤抗CD40抗体Selicrelumab治疗患者及B-hCD40小鼠的irAEs比较
根据已有数据显示,Selicrelumab在其临床治疗患者试验中产生irAEs包括:
1) 细胞因子释放综合征CRS:TNF-α和IL-6升高
2) 血液学毒性:外周淋巴细胞、单核细胞和血小板降低,血液中CD19+ B细胞降低。
3) 肝毒性:血清中肝转氨酶和总胆红素升高(24-48h达到峰值)

图1. (A) 根据文献报道[3],注射Selicrelumab后,临床患者出现明显的血液毒性,血液中外周淋巴细胞和血小板数量减少。ALT和AST的升高提示肝毒性的发生。此外,CD19+B细胞出现显著下降。(B)不同性别的B-hCD40小鼠接受Selicrelumab(类似物,20 mpk)给药,第14天出现与临床一致的不良反应表现。
➤ Selicrelumab(类似物)给药后B-hCD40小鼠的急性期蛋白和肝损伤增加
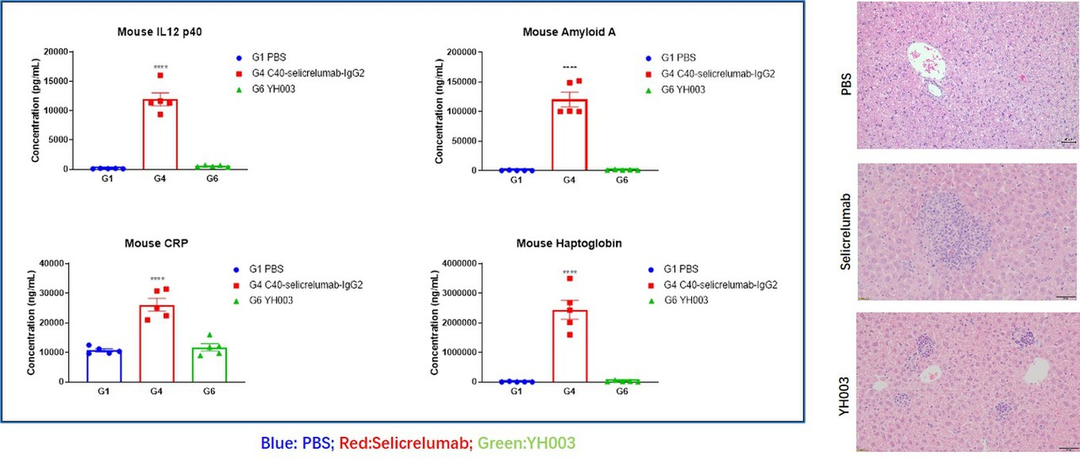
图2. (A) B-hCD40小鼠接受 Selicrelumab (类似物)给药后,急性期蛋白如CRP、淀粉样蛋白A、结合珠蛋白和 IL12P40 增加。(B) 与 PBS 处理的小鼠相比,B-hCD40小鼠淋巴细胞浸润增加,表明肝脏出现病理损伤。
百奥动物自主开发了100多种肿瘤、自免、代谢领域相关人源化小鼠模型,能够用于癌症、COVID-19、HIV、肝炎、关节炎、哮喘、糖尿病、NASH等疾病药物的临床前PK、PD、毒理等研究。
越来越多的人源化小鼠在药物药理药效研究的应用受到业界和监管机构的认可,欢迎点击拨打电话了解更多数据信息
参考资料:
[1] 生物制品非临床安全性评价指导原则
[2] 《缓解COVID-19大流行引起的非人灵长类动物供应限制的非临床研究考虑因素行业指南 》
[3] Vonderheide RH, Flaherty KT, Khalil M, Stumacher MS, Bajor DL, Hutnick NA, Sullivan P, Mahany JJ, Gallagher M, Kramer A, Green SJ, O'Dwyer PJ, Running KL, Huhn RD, Antonia SJ. Clinical activity and immune modulation in cancer patients treated with CP-870,893, a novel CD40 agonist monoclonal antibody. J Clin Oncol. 2007 Mar 1;25(7):876-83.






 010-56967680
010-56967680 info@bbctg.com.cn
info@bbctg.com.cn 苏公网安备:32068402320845号
苏公网安备:32068402320845号