TIM3靶点简介
TIM3(T细胞免疫球蛋白及粘蛋白结构域分子3)又称HAVCR2,属于免疫调节蛋白TIM家族的一员,在人类,TIM家族包括TIM1、TIM3和TIM4,位于染色体5q33.2上。在小鼠中,TIM家族包括TIM1到TIM8,位于染色体11B1.1上。大量证据表明,TIM家族在自身免疫性疾病、感染性疾病、肿瘤免疫监视和免疫逃逸等免疫反应的调节中发挥着不同的作用。TIM3是一类T细胞表面抑制性分子,能够引起癌症与慢性病毒感染过程中T细胞的耗竭。与CTLA4,PD1类似,它也是目前研究最多的免疫治疗的靶点之一。
TIM3作为一种负调控的免疫检查点,于2002年首次被发现,由281个氨基酸组成,并且由一个胞外区、一个单跨膜结构域和一个C-末端细胞质尾部组成。TIM3选择性地表达在分泌IFN-γ的辅助性T细胞(Th1和Th17) 、调节性T细胞(Treg) 、树突状细胞(DCs) 、单核细胞、肥大细胞、NK细胞、肿瘤浸润淋巴细胞(TILs) 上,在肿瘤细胞上亦有表达,如黑色素瘤、胃癌、B细胞淋巴瘤。TIM3作为重要的免疫检查点的机制主要在于TIM3标志着肿瘤浸润CD8+ PD1+ T细胞功能最失调的亚群。同时阻断TIM3和PD1通路的抗体对抑制肿瘤生长、改善肿瘤抗原特异性CD8+T细胞的响应具有协同作用。[1]
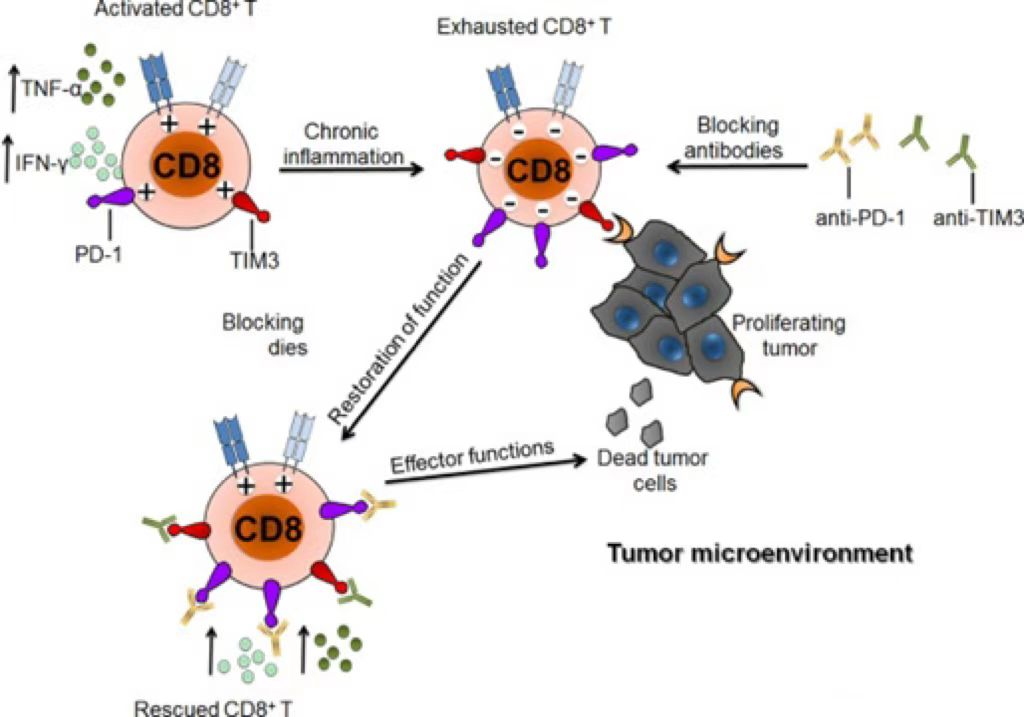
图1:TIM3可以诱导T细胞耗竭[1]
TIM3有多种不同的配体,包括半乳糖凝集素9(Galectin 9)、磷脂酰丝氨酸(PtdSer)、癌胚抗原相关细胞粘附分子1(CEACAM1)以及HMGB1,它们分别与TIM3胞外区IgV结构域的不同位点结合。
当TIM3未与其配体结合时,它被招募到T细胞激活的免疫突触中,与 HLA-B相关转录产物3(BAT3)相互作用,并通过酪氨酸激酶LCK募集维持T细胞活化。可溶性凝集素半乳糖凝集素9(Galectin 9)和粘附分子癌生物抗原相关细胞粘附分子1(CEACAM1),通过酪氨酸激酶ITK触发Tyr256和Tyr263的磷酸化。磷酸化后,BAT3从TIM3中释放出来,从而使TIM3发挥其抑制功能。BAT3敲除的T细胞其共抑制受体的表达升高,并且在自身免疫的背景下表现出降低的致病性,说明BAT3通过负反馈来调节T细胞的功能。FYN与BAT3结合TIM3的同一区域。多数促进抗肿瘤免疫的TIM3靶向抗体干扰CEACAM1或PtdSer与TIM3的结合,从而维持TIM3-BAT3的相互作用[2]。

图2:TIM3的作用机制[2]
TIM3靶点药物研发进展
随着技术进步和研究创新,TIM3是目前研究最多的免疫治疗的靶点之一,靶向TIM3的治疗正处于临床试验/研发阶段,国内外尚无已上市药物,但很多制药企业都有布局,临床III期两个(诺华、GSK各有一个)、临床II期5个(罗氏、百济神州、阿斯利康等)、临床I期8个(礼来、恒瑞等),主要适应症急性髓系白血病(AML)和骨髓增生异常综合症(MDS)、非小细胞肺癌等实体瘤;全球研发TIM3/PD1双特异性抗体的公司不多,研究进入临床试验的只有阿斯利康、罗氏和礼来,其余皆处于临床前。
表1. 部分在研药物临床进展
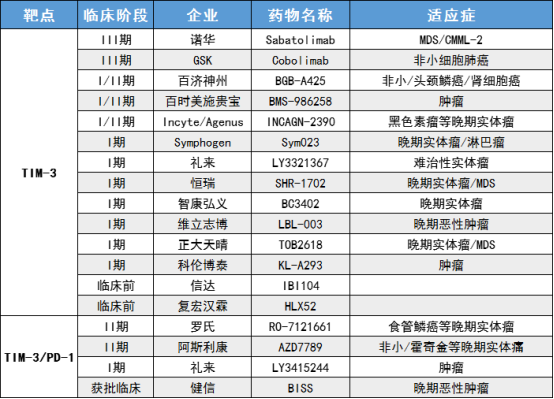
数据来源于科睿唯安
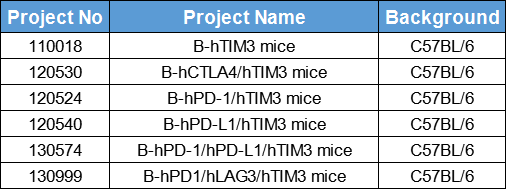
针对TIM3靶点机制研究和新药开发的需求,BioMice百奥动物自主研发了B-hTIM3 mice,同时也扩繁了B-hPD-1/hTIM3 mice,B-hPD-L1/hTIM3 mice,B-hCTLA4/hTIM3 mice双人源化小鼠及B-hPD-1/hPD-L1/hTIM3 mice等三人源化小鼠,相关模型列表见文末,助力靶向TIM3药物开发,为临床前药效评估提供了优质模型。
B-hTIM3 mice
基本信息

蛋白表达分析
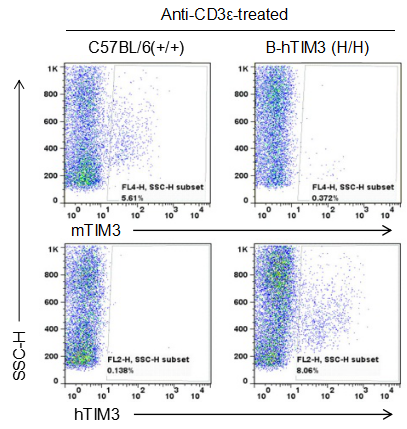
通过流式细胞术对纯合B-hTIM3 小鼠进行种属特异性B-hTIM3 小鼠表达分析。收集野生型C57BL/6和纯合 B-hTIM3 小鼠的腹腔冲洗液细胞,结果显示:小鼠 TIM3 仅在野生型小鼠的非 T 和非 B 细胞中检测到,人 TIM3 仅在纯合 B-hTIM3 小鼠的非 T 和非 B 细胞可检测到。
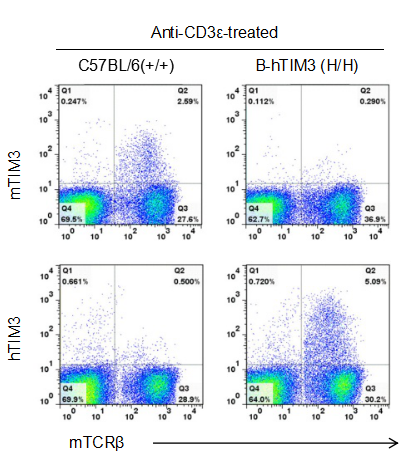
通过流式细胞术对纯合B-hTIM3 小鼠进行种属特异性 TIM3 表达分析。收集野生型C57BL/6和纯合 B-hTIM3 小鼠的脾细胞,结果显示:小鼠 TIM3 仅在野生型小鼠中检测到。人 TIM3 仅在纯合 B-hTIM3 小鼠中检测到。
药效验证
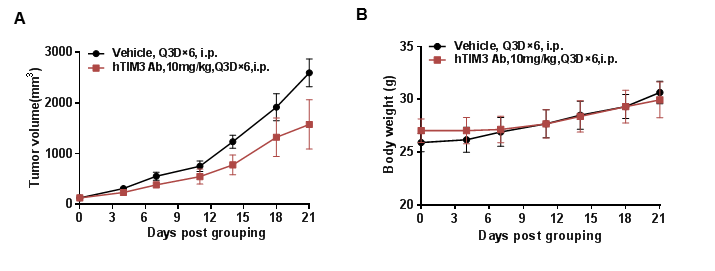
抗人 TIM3 抗体在B-hTIM3 小鼠中的抗肿瘤活性。(A)抗人 TIM3 抗体可抑制B-hTIM3 小鼠中的MC38肿瘤生长。将小鼠结肠癌MC38细胞皮下植入纯合B-hTIM3 小鼠(雄性,7周龄,n=5)。当肿瘤体积达到约100 mm3时,将小鼠分组,此时用抗人 TIM3 抗体处理。(B)给药期间体重变化。如图A所示,抗人 TIM3 抗体可有效抑制B-hTIM3 小鼠的肿瘤生长,表明B-hTIM3 小鼠为抗人 TIM3 抗体的体内评价提供了有力的临床前模型。数值表示为平均值±SEM。
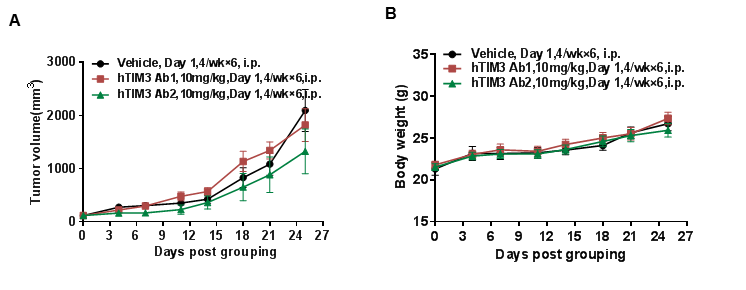
抗人 TIM3 抗体在B-hTIM3 小鼠中的抗肿瘤活性。(A)抗人 TIM3 抗体可抑制B-hTIM3 小鼠中的MC38肿瘤生长。将小鼠结肠癌MC38细胞皮下植入纯合B-hTIM3 小鼠(雌性,4周龄,n=5)。当肿瘤体积达到约100 mm3时,将小鼠分组,此时用抗人 TIM3 抗体处理。(B)给药期间体重变化。如图A所示,抗人 TIM3 抗体可有效抑制B-hTIM3 小鼠的肿瘤生长,表明B-hTIM3 小鼠为抗人 TIM3 抗体的体内评价提供了有力的临床前模型。
B-hCTLA-4/hTIM3 mice
蛋白表达分析
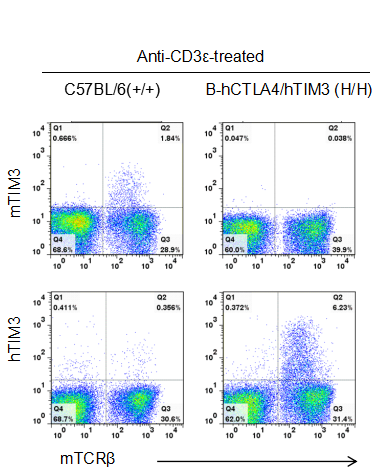
通过流式细胞术对纯合B-hCTLA4/hTIM3 小鼠进行种属特异性 TIM3 表达分析。收集野生型C57BL/6和纯合 B-hCTLA4/hTIM3(H/H) 小鼠的脾细胞,结果显示:小鼠 TIM3 在野生型小鼠中可检测到。人 TIM3 仅在纯合 B-hCTLA4/hTIM3 小鼠中可检测到,但在 WT 小鼠中未检测到。
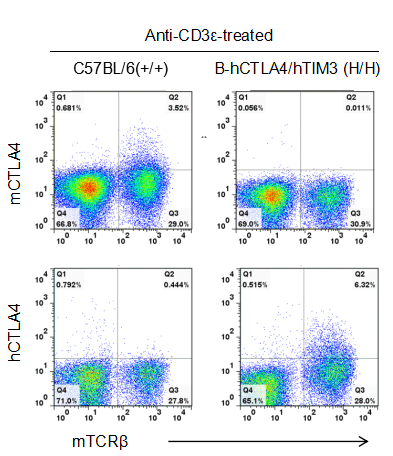
通过流式细胞术对纯合B-hCTLA4/hTIM3 小鼠进行种属特异性CTLA4 表达分析。收集野生型C57BL/6和纯合 B-hCTLA4/hTIM3(H/H) 小鼠的脾细胞,结果显示:小鼠 CTLA4 在野生型小鼠中可检测到。人CTLA4仅在纯合 B-hCTLA4/hTIM3 小鼠中可检测到,但在 WT 小鼠中未检测到。
B-hPD-1/hTIM3 mice
药效验证
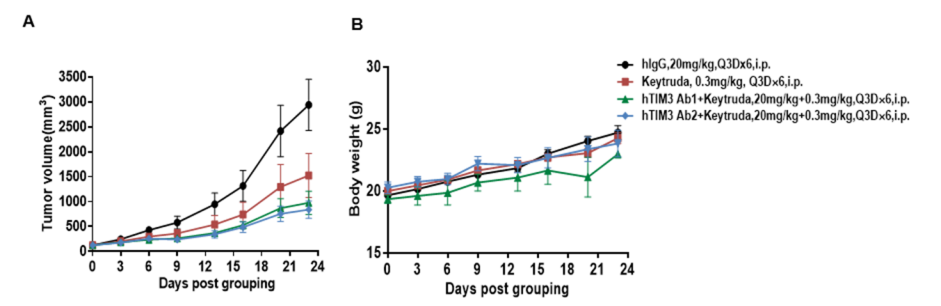
抗人TIM3抗体联合抗人PD-1抗体在B-hPD-1/hTIM3 小鼠中的抗肿瘤药效。(A)抗人TIM3 抗体联合抗人PD-1抗体抑制B-hPD-1/hTIM3 小鼠MC38肿瘤生长。小鼠结肠癌MC38细胞(5×105)皮下植入纯合B-hPD-1/hTIM3小鼠中(雌性,6-8周龄,n=6)。当肿瘤体积达到大约150±50 mm3时,小鼠被分组,然后用抗人 TIM3 抗体联合抗人PD -1抗体Keytruda给药。(B)治疗期间体重变化。如图A所示,抗人TIM3抗体与抗人PD-1抗体联合使用比单独使用组对肿瘤生长具有更强的抑制作用,说明B-hPD-1/hTIM3小鼠为评价人TIM3抗体与人PD-1抗体联合治疗的体内评估提供了一个强有力的临床前模型。
B-hPD-1/hPD-L1/hTIM3 mice
药效验证
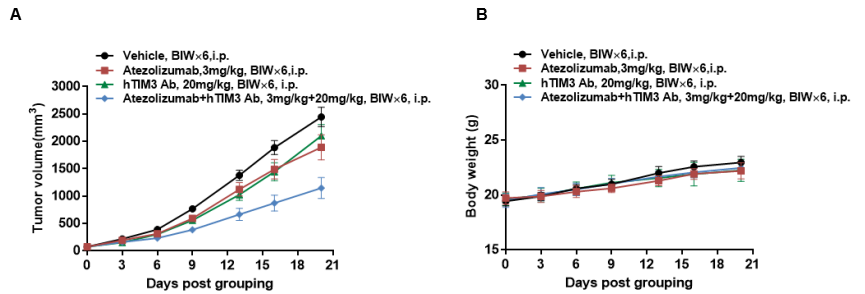
抗人PD-L1抗体(内部合成)联合抗人TIM3抗体在B-hPD-1/hPD-L1/hTIM3 小鼠中的抗肿瘤药效。(A) 纯合B-hPD-1/hPD-L1/hTIM3 小鼠(雌性,7-8周龄,n=6)皮下接种小鼠结肠癌MC38细胞。当肿瘤体积达到约100 mm3时对小鼠进行分组,分组后给抗人PD-L1抗体和抗人 TIM3 抗体进行治疗,剂量和时间表如图 A 所示。(B) 给药期间的体重变化。如图 A 所示,抗人 PD-L1 抗体和抗人 TIM3 抗体联合给药组的抑制作用强于单药组,抗人 PD-L1 抗体联合抗人 TIM3 抗体可抑制 B-hPD-1/hPD-L1/hTIM3 小鼠中的肿瘤细胞生长。结果证明 B-hPD-1/hPD-L1/hTIM3 小鼠可为体内评价抗人PD-L1 和抗人TIM3抗体药效提供有力的临床前研究模型。
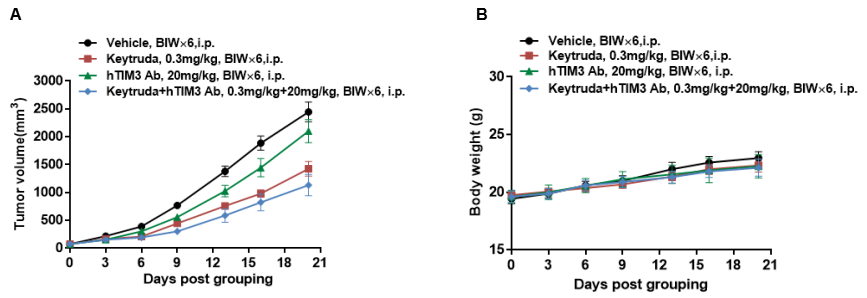
抗人PD-1抗体(内部合成)联合抗人TIM3抗体在B-hPD-1/hPD-L1/hTIM3 小鼠中的抗肿瘤药效。(A) 纯合B-hPD-1/hPD-L1/hTIM3 小鼠(雌性,7-8周龄,n=6)皮下接种小鼠结肠癌MC38细胞。当肿瘤体积达到约100 mm3时对小鼠进行分组,分组后给抗人PD-1抗体和抗人 TIM3 抗体进行治疗,剂量和时间表如图 A 所示。(B) 给药期间的体重变化。如图 A 所示,抗人 PD-1 抗体和抗人 TIM3 抗体联合给药组的抑制作用强于单药组,抗人 PD-1 抗体联合抗人 TIM3 抗体可抑制 B-hPD-1/hPD-L1/hTIM3 小鼠中的肿瘤细胞生长。结果证明 B-hPD-1/hPD-L1/hTIM3 小鼠可为体内评价抗人PD-1 和抗人TIM3抗体药效提供有力的临床前研究模型。
参考资料
[1] Solinas, C., et al., Significance of TIM3 expression in cancer: From biology to the clinic. Semin Oncol, 2019. 46(4-5): p. 372-379.
[2] Wolf, Y., A.C. Anderson, and V.K. Kuchroo, TIM3 comes of age as an inhibitory receptor. Nat Rev Immunol, 2020. 20(3): p. 173-185.
TIM3靶点相关模型列表
想要了解更多人源化小鼠,欢迎来电咨询。






 010-56967680
010-56967680 info@bbctg.com.cn
info@bbctg.com.cn 苏公网安备:32068402320845号
苏公网安备:32068402320845号