炎症性肠炎( Inflammatory Bowel Disease, IBD)是一种病因不明的结肠或胃肠道的非特异性慢性炎症性疾病。因为其易复发,不可根治,曾被称为“绿色癌症”,和普通肠炎有较大区别。普通肠炎一般是急性的,进行抗感染治疗后可以治愈。
IBD临床表现
IBD 可产生多种临床表现,包括但不限于以下几种:
➤ 消化道症状如腹泻、腹痛、便血、肛周脓肿等;
➤ 全身症状如体重减轻、发热、乏力、贫血等;
➤ 肠外表现如关节、皮肤、粘膜、眼部病变等;严重者可出现肠穿孔、肠梗阻、大出血等,甚至癌变。
IBD发病机制
IBD发病原因目前尚未明确,研究表明:易感基因、免疫系统、外界环境和肠道微生物等多种因素均与疾病发生相关。
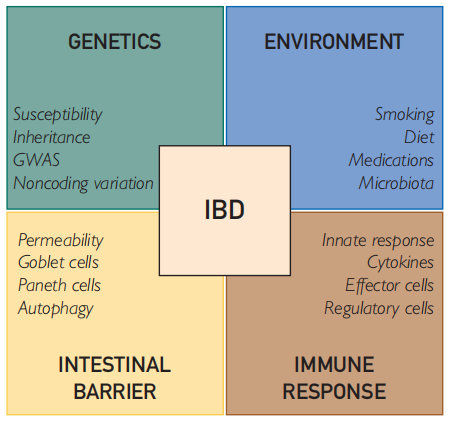
IBD发病因素
其中环境触发因素可通过其对微生物组的影响来介导IBD发病机制。然而,为了使微生物改变导致不适当的和持续的炎症,肠屏障的分离腔和粘膜完整性也受到损害。在IBD粘膜中效应T细胞和调节性T细胞(T-reg)之间的平衡受到了干扰,造成异常的免疫应答和T细胞驱动的过度炎症反应。
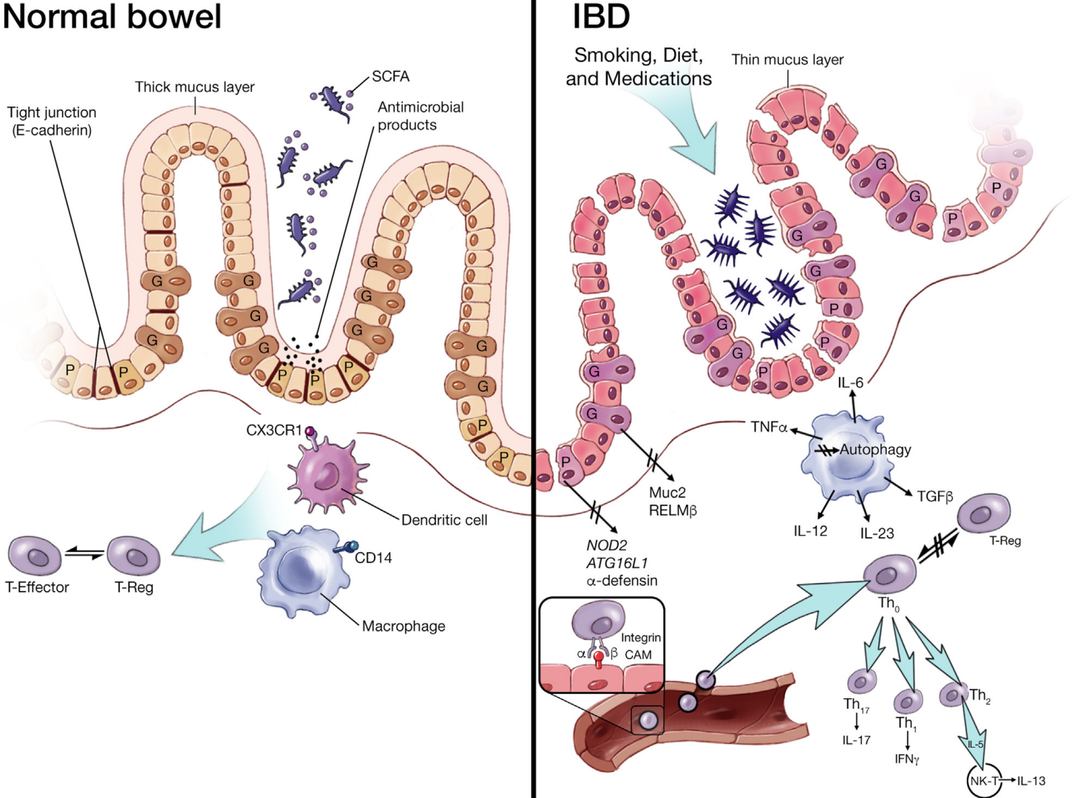
正常肠和炎症性肠病(IBD)的肠黏膜
IBD包括溃疡性结肠炎(ulcerative colitis,UC)和克罗恩病(Crohn’s disease,CD),两者最大的区别是:UC 的炎症只局限于大肠,而 CD 的炎症可以发生于全消化道从口腔到肛门部。
IBD以前在我国属于少见病,但近年来,其发病率逐渐攀升。
IBD疾病模型
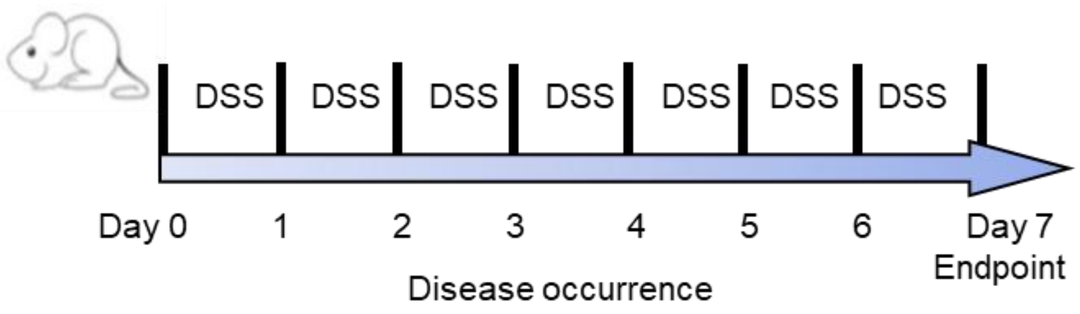
目前有多种临床前小鼠模型用于研究 IBD,基于不同诱导方法得到的疾病模型具有特定的用途。葡聚糖硫酸钠(Dextran Sulfate Sodium Salt,DSS)诱导的小鼠肠炎模型是使用最广泛的化学诱导小鼠 IBD 模型。通过将 DSS 溶于饮用水中诱发急性溃疡性肠炎或者慢性结肠炎,破坏小鼠肠上皮细胞,非特异性免疫细胞释放细胞因子,最终导致黏膜屏障的完整性遭到破坏,动物表现出明显的体重减轻、稀便、便血以及粒细胞浸润现象,在临床症状和病理特征上与人类的溃疡性结肠炎极其相似。
百奥赛图在 C57BL/6 小鼠上建立了稳定的 DSS 诱导 IBD 疾病模型,可用于炎症性肠炎的临床前研究和药效评价。
IBD 小鼠疾病模型用于评价炎症性肠炎药物环孢菌素 A(Cyclosporin A, CsA)的药效
模型制备示意图
临床评分
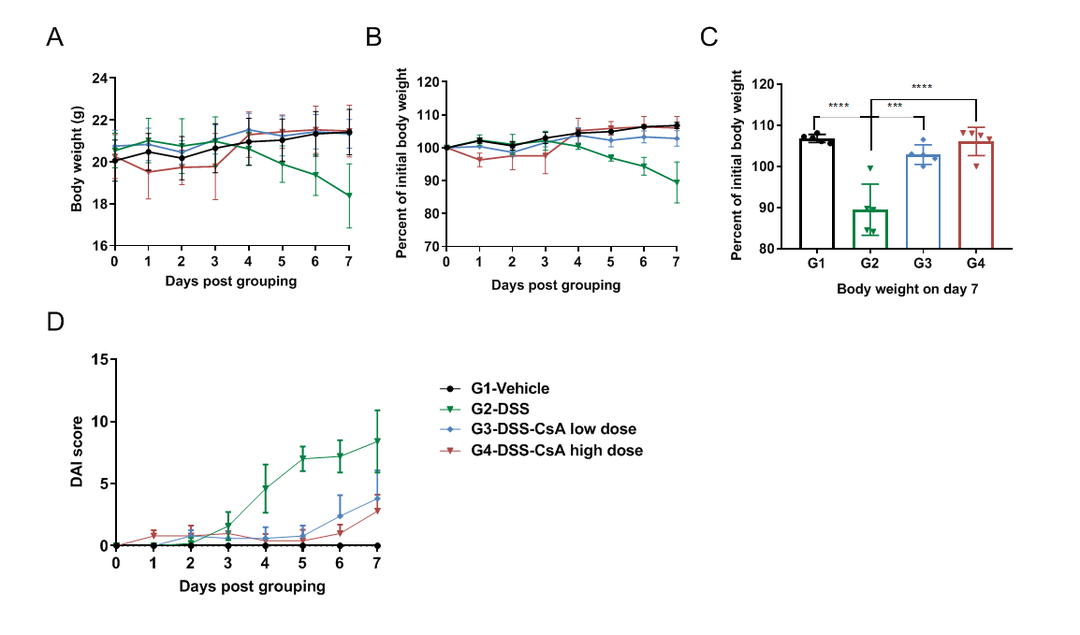
C57BL/6 小鼠连续 7 天饮用含 DSS 的饮用水,全程记录体重变化,并进行临床评分。(A-C)各组动物体重变化趋势。(D)各组动物临床评分。实验数据显示,造模组(G2-DSS)相对于未造模组(G1-Vehicle),动物体重有所下降,且临床评分明显升高;给药组(G3-DSS-CSA low dose 和 G4-DSS-CSA high dose)的动物体重变化不明显,临床评分略有升高。这表明 DSS 诱发 C57BL/6 小鼠炎性肠病疾病模型造模成功,CsA 对小鼠炎性肠病疾病模型的临床症状有缓解,并且呈现剂量依赖效应
大体取材与结肠评价
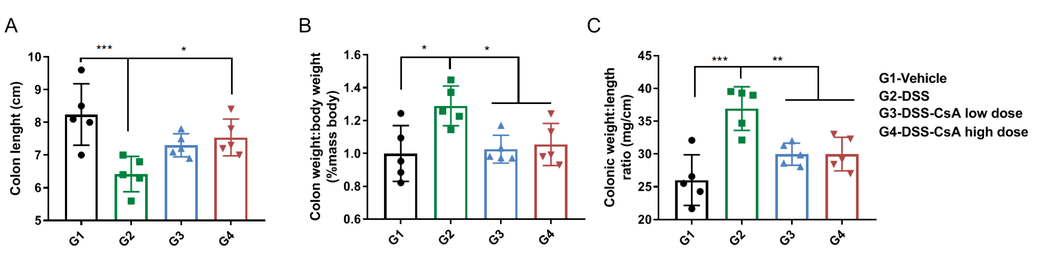
DSS 诱发 C57BL/6 小鼠炎性肠病疾病模型 7 天后,取结肠进行称重和测量长度。(A)结肠长度比较。(B)各组动物结肠重量与体重比值。(C)各组动物结肠重量与结肠长度比值。实验数据显示,造模组(G2-DSS)相对于未造模组(G1-Vehicle),结肠重量和长度明显异常;与造模组相比,给药组的结肠重量下降,结肠长度上升,二者比值显著降低。这表明 CsA 对 DSS 诱发小鼠炎性肠病疾病模型的结肠症状有所缓解。
病理分析
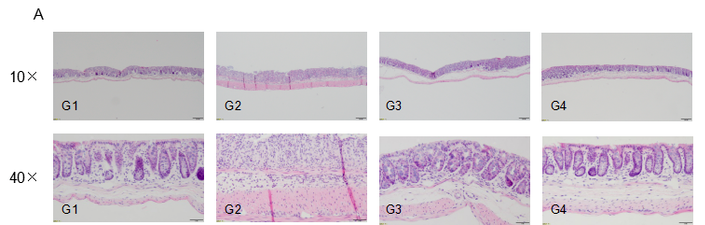
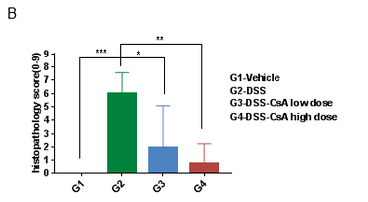
取 DSS 诱发 C57BL/6 小鼠炎性肠病疾病模型的结肠,将组织切片进行病理检测。(A)各组动物结肠 H&E染色图示。(B)各组动物结肠病理评分。实验数据显示,造模组(G2-DSS)相对于未造模组(G1-Vehicle),肠上皮细胞受到破坏,肠道黏膜层完整性遭到破坏,炎性细胞大量浸润;而给药组(G3-DSS-CSA low dose 和 G4-DSS-CSA high dose)的结肠症状明显缓解,且表现出剂量效应。
综合临床评分、大体取材和结肠评价、病理分析结果,表明 DSS 诱发 C57BL/6 小鼠炎性肠病疾病模型造模成功,环孢菌素 A(CsA)能够显著缓解 DSS 诱发炎性肠病结肠病损,且表现出剂量效应。
可提供服务内容

IBD药物评估相关模型列表
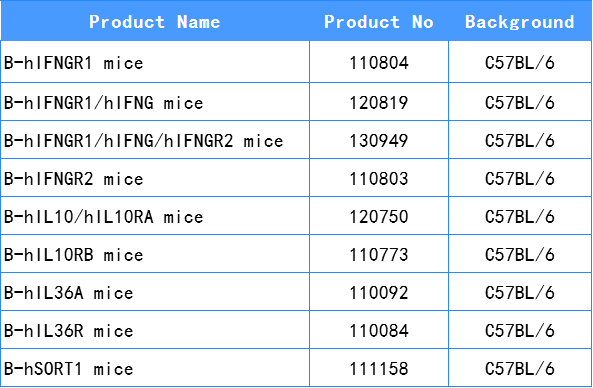
参考资料:
1. Elson, C.O., Sartor, R.B., Tennyson, G.S. & Riddell, R.H. Experimental models of
inflammatory bowel disease. Gastroenterology 109, 1344-1367 (1995).
2. Kiesler, P., Fuss, I.J. & Strober, W. Experimental Models of Inflammatory Bowel Diseases. Cell Mol Gastroenterol Hepatol 1, 154-170 (2015).
3. Mourad, F.H., Yau, Y., Wasinger, V.C. & Leong, R.W. Proteomics in Inflammatory Bowel Disease: Approach Using Animal Models. Dig Dis Sci 62, 2266-2276 (2017).
4. Guilherme Piovezani Ramos, MD, and Konstantinos A. Papadakis, MD.Mechanisms of Disease: Inflammatory Bowel Diseases.Mayo Clin Proc. 2019;94(1):155-165.






 010-56967680
010-56967680 info@bbctg.com.cn
info@bbctg.com.cn 苏公网安备:32068402320845号
苏公网安备:32068402320845号