超重和肥胖已成为全球性健康问题,它是引起包括糖尿病、心血管疾病、肝病以及癌症在内的若干慢性病的重要病因。现在约50%的2型糖尿病、30%的缺血性心脑血管疾病及10%-40%的癌症是由肥胖或超重引起的。中国已经是全球超重和肥胖人数第一的国家,肥胖症存在巨大未被满足的临床需求。
研究进展
目前,降糖药的研发重点已经转向双靶点、三靶点激动剂领域,全球范围内礼来独占鳌头,而国内企业中信达属于第一梯队。
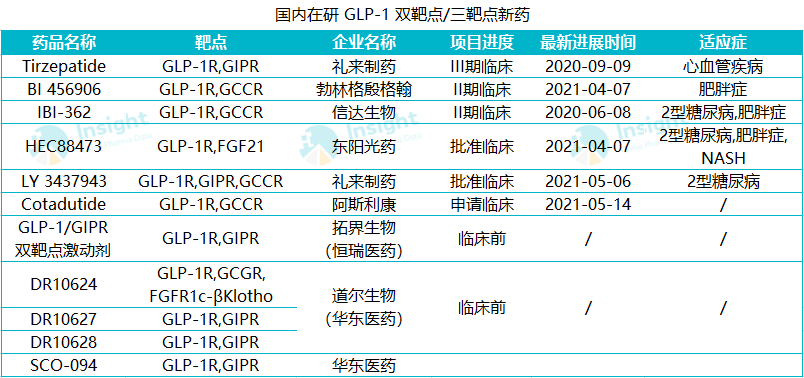
来自 Insight 数据库
IBI362 是信达生物制药与礼来制药共同推进的一款与哺乳动物 OXM 类似的长效合成肽(OXM3),是中国第一个进入临床的具有同类最优潜力的GLP-1R和GCGR双重激动剂分子。
目前,根据 Insight 数据库,IBI362 已在国内启动了 4 项临床,针对肥胖症和 2 型糖尿病的临床试验已经进入 II 期。作为新一代的 GLP-1 药物,IBI362 在后续超重/肥胖受试者中的 II 期临床研究结果值得期待。
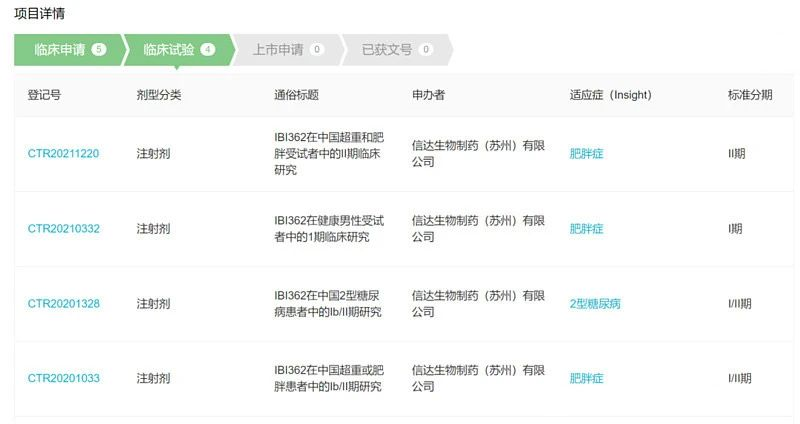
来自 Insight 数据库
此外,阿斯利康(AZN.US)申报1类新药cotadutide注射液临床试验申请,并获得受理。公开资料显示,cotadutide是一款胰高血糖素受体(GCGR)和胰高糖素样肽-1受体(GLP-1R)双重激动剂,全球研发进展至临床2期阶段。目前开发靶向GCGR/GLP-1R的双重激动剂,已成为治疗糖尿病、肥胖、非酒精性脂肪性肝炎(NASH)等疾病的一个新方向。
百奥动物BioMice自主开发了B-hGCGR小鼠和B-hGLP1R小鼠,为糖尿病相关药物研究提供有效模型。
B-hGCGR小鼠
GCGR编码胰高血糖素受体,在控制血糖水平方面很重要。该基因的缺陷是非胰岛素依赖型糖尿病(NIDDM)的一个原因。人胰高血糖素受体(GCGR)通过其内源性配体胰高血糖素激活,在禁食期间触发肝脏释放葡萄糖,使其成为II型糖尿病的潜在药物靶点。
胰高血糖素通过与Gsα型或Gq型G蛋白偶联的7次跨膜II类受体发挥作用。Gsα的受体激活激活腺苷酸环化酶,导致环磷酸腺苷(cAMP)蓄积和蛋白激酶A活性增加,Gq受体激活通过激活磷脂酶C导致细胞内Ca2+增加。
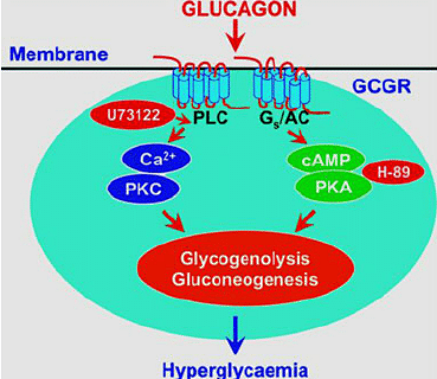
模型示意图和抗体评价方案
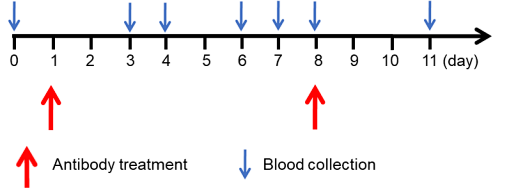
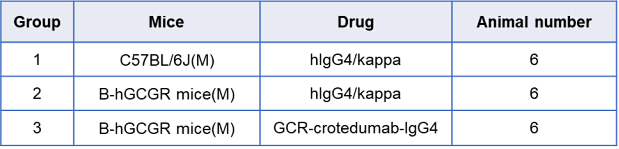
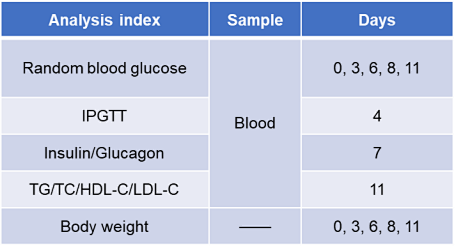
抗人GCGR抗体体内疗效的实验时间表。在第1-8天,通过腹膜内注射给予抗人GCGR抗体-crotedumab(内部合成),每周一次。在示意图和表格中显示的日期采集血液用于分析血糖、胰岛素、胰高血糖素和脂质。
抗人GCGR抗体降低B-hGCGR小鼠的血糖
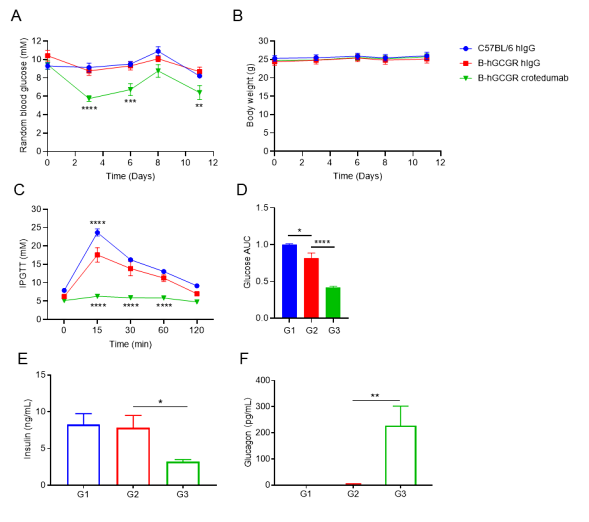
(A)注射crotedumab(内部合成)或同型对照抗体(n = 6)前后多个时间点检测雄性小鼠的随机血糖;(B)体重;(C)第4天OGTT;(D)C图中OGTT曲线下的面积;(E)第7天血清胰岛素水平;(F) 第7天胰高血糖素水平。与注射同型抗体相比,注射抗人GCGR抗体能降低B-hGCGR小鼠的随机血糖、空腹血糖和OGTT;抗体治疗组血清胰岛素水平轻微降低,胰高血糖素水平明显升高;在B-hGCGR小鼠的所有结果与野生型C57BL/6相似。
结果表明,B-hGCGR小鼠的血糖调节功能与野生型C57BL/6相似。抗人GCGR抗体对B-hGCGR小鼠血糖有明显的控制作用。数值用平均值±SEM表示。OGTT,口服葡萄糖耐量试验。
抗人GCGR抗体改善B-hGCGR小鼠的脂质代谢
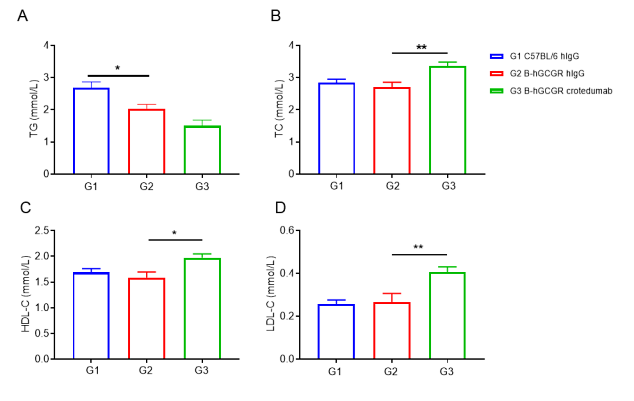
分别用crotedumab(内部合成)或同型对照抗体注射到野生型C57BL/6和B-hGCGR小鼠(雄性,n=6)中。第11天采血分析甘油三酯和胆固醇。(A)、(B)、(C)、(D)依次为血清中TG 、TC、HDL-C、LDL-C水平。与同型对照组相比,抗人GCGR抗体处理组小鼠血清中TG水平降低,TC、HDL-C和LDL-C水平升高。B-hGCGR小鼠的所有结果与野生型C57BL/6相似。
结果表明,B-hGCGR小鼠的脂质代谢与野生型相似。抗人GCGR抗体对B-hGCGR小鼠血脂有明显的控制作用。数值用平均值±SEM表示。TG:甘油三酸酯;TC:总胆固醇;HDL-C:高密度脂蛋白胆固醇;LDL-C:低密度脂蛋白胆固醇。
B-hGLP1R 小鼠
胰高血糖素样肽-1受体(GLP1R)是一种在胰腺β细胞和大脑神经元中发现的受体蛋白。通过增强胰岛素分泌参与血糖水平的控制。在人体中,其由存在于6号染色体上的基因GLP1R合成,属于G蛋白偶联受体的胰高血糖素受体家族成员。
GLP1R由两个结构域组成,一个位于细胞外(ECD),与GLP-1的C-末端螺旋结合,还有一个跨膜(TMD)结构域结合GLP-1的N端区域。在TMD结构域中,有一个极性残基支点调节受体的偏向信号,而跨膜螺旋边界和细胞外表面是偏向激动作用的触发因素。
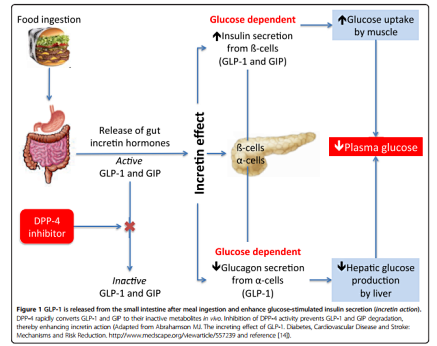
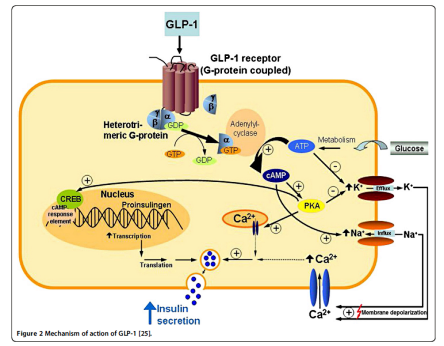
在糖尿病患者中,GLP-1R信号通过上调cAMP,随后激活PKA和cAMP激活的交换蛋白,增强葡萄糖依赖性胰岛素分泌。
蛋白表达分析
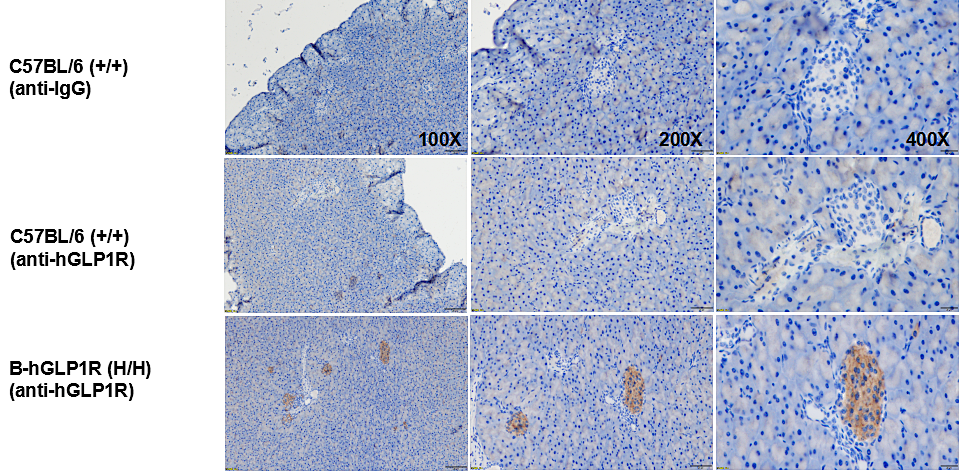
人GLP1R表达的IHC。使用人GLP1R特异性抗体对野生型(+/+)和B-hGLP1R小鼠(H/H)的胰腺组织进行染色。仅B-hGLP1R小鼠(H/H)的胰腺在胰岛细胞中显示hGLP1R阳性信号。
Dulaglutide(杜拉鲁肽)可降低B-hGLP1R小鼠的血糖
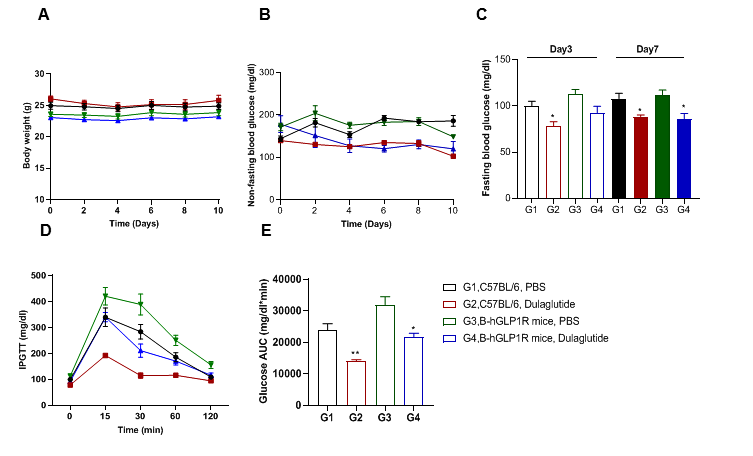
分别用Dulaglutide(内部合成)或PBS注射野生型C57BL/6小鼠和B-hGLP1R小鼠后多时间点采血分析(雄性,7-8w, n=5)。(A)、(B)、(C)、(D) 、(E)依次为体重、非空腹血糖、空腹血糖、IPGTT、 IPGTT曲线下面积。体重在实验过程中无显著变化。与PBS相比,Dulaglutide降低C57BL/6小鼠和B-hGLP1R小鼠的非空腹血糖和空腹血糖。IPGTT结果显示,B-hGLP1R小鼠与野生型小鼠在葡萄糖代谢方面表现出相似的生理反应。值用平均值±SEM表示,IPGTT:腹腔内糖耐量试验。
Dulaglutide(杜拉鲁肽)可减少B-hGLP1R小鼠的摄食量
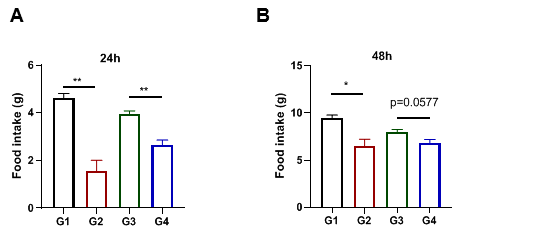
分别监测Dulaglutide治疗24小时和48小时后C57BL/6小鼠和B-hGLP1R小鼠的摄食量(雄性,15w, n=5),计算每个笼的摄食量,并校正每只小鼠的摄食量。(A). 24小时的食物摄入量。(B) 48小时的食物摄入量。Dulaglutide减少C57BL/6和B-hGLP1R小鼠的摄食量。值表示为平均值±SEM。
参考资料
[1]https://www.researchgate.net/figure/Two-classic-G-protein-coupled-glucagon-receptor-mediated-intracellular-signaling-pathways_fig1_256333156
[2]Migyeong Jo, Sang Taek Jung. Engineering therapeutic antibodies targeting G-protein–coupled receptors. Experimental & Molecular Medicine (2016) 48, e207
[3]Gaojie Song, Dehua Yang, Yuxia Wang,et al. Human GLP-1 receptor transmembrane domain structure in complex with allosteric modulators
[4]https://mp.weixin.qq.com/s/LtfWCuk2QWEKMBDpw5JnKw






 010-56967680
010-56967680 info@bbctg.com.cn
info@bbctg.com.cn 苏公网安备:32068402320845号
苏公网安备:32068402320845号